Clear Sky Science · ja
グルコソジエン搭載ナノフェライト(GLONF)による酸化ストレスおよびP53/PCNAシグナルの調節:エーリッヒ実体腫瘍誘発肝毒性における検討
この研究が重要な理由
がん治療はしばしば健康な臓器、特に多くの薬物や腫瘍由来の代謝産物を分解する肝臓にダメージを与えます。本研究は、磁性で誘導できる微小なキャリアにより、糖類由来の抗がん化合物を腫瘍に直接届けつつ肝臓を保護する新しいアプローチを検討しています。読者にとっては、ナノテクノロジーと賢い化学設計が将来的にがん治療をより有効かつ低毒性にする可能性を示す一端が垣間見えます。
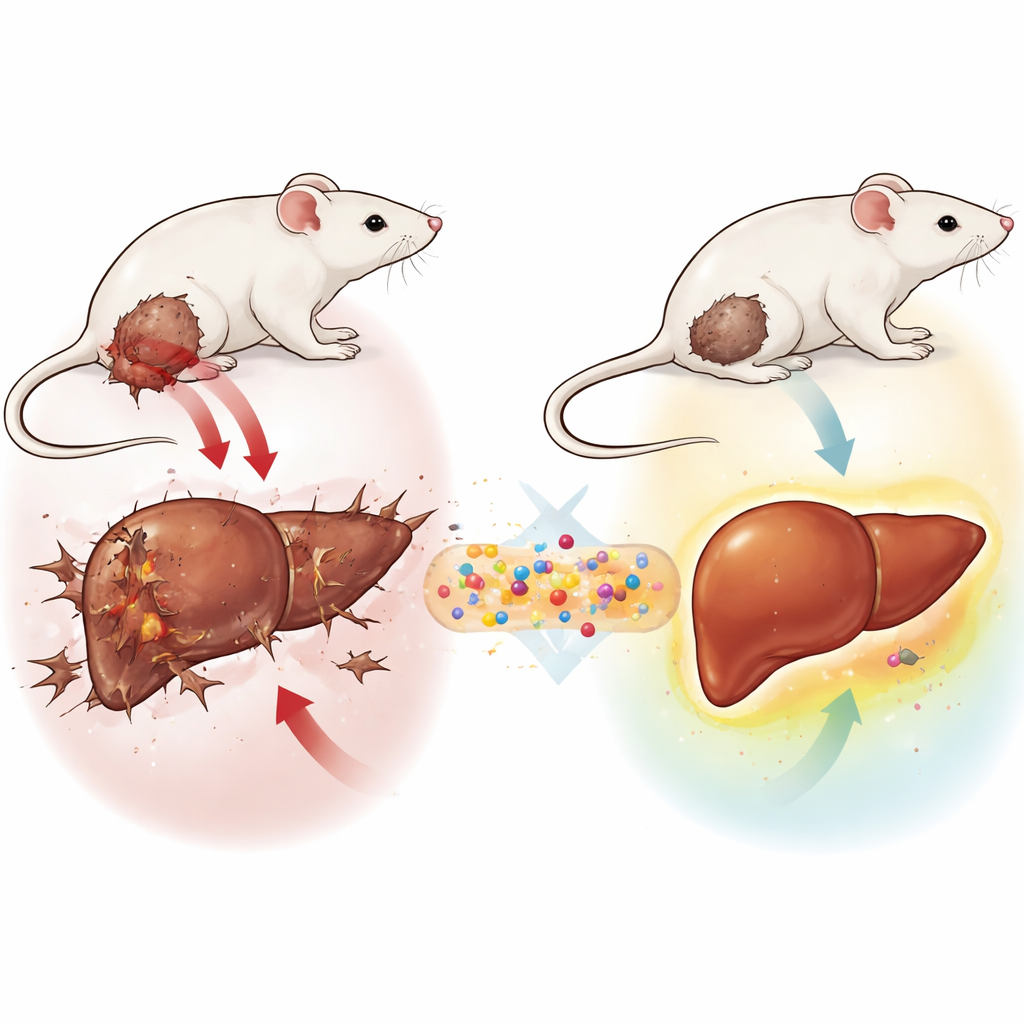
小さな輸送体の大きな役割
研究者らはGLONFと呼ばれる三層構造のナノシステムを構築しました。中心には特殊な鉄系材料からなる磁性ミネラル核があり、その周囲に安全性と安定性から医療材料でよく用いられる天然の糖由来シェルであるキトサンを被せています。最後に、がん細胞のブドウ糖摂取を阻害し、腫瘍周辺の酸性環境を和らげるよう設計された新しい糖誘導体であるグルコソジエンを結合しました。これらの要素は合わせて、磁気で誘導可能で体内を安全に移動し、必要な部位で抗がん剤を放出できる小型の輸送体を形成します。
乳がん様モデルマウスでの評価
GLONFががんの際に肝臓を保護できるかを調べるため、研究チームはエーリッヒ実体腫瘍という確立されたマウスモデルを用いました。この腫瘍はもともと乳組織由来で、皮下で急速に増殖し、侵攻性の高いヒトがんの多くの特徴を模倣します。雌マウスは複数の群に分けられ、健康のままの群、ナノ製剤のみを投与された群、治療を受けずに腫瘍を有する群、腫瘍植入と同時にGLONFを投与された群、腫瘍形成後にGLONFを投与された群が設定されました。研究者らは腫瘍サイズ、肝機能の標準的な血液マーカー、ならびに肝臓内の化学的・顕微鏡的な損傷と修復の指標を測定しました。
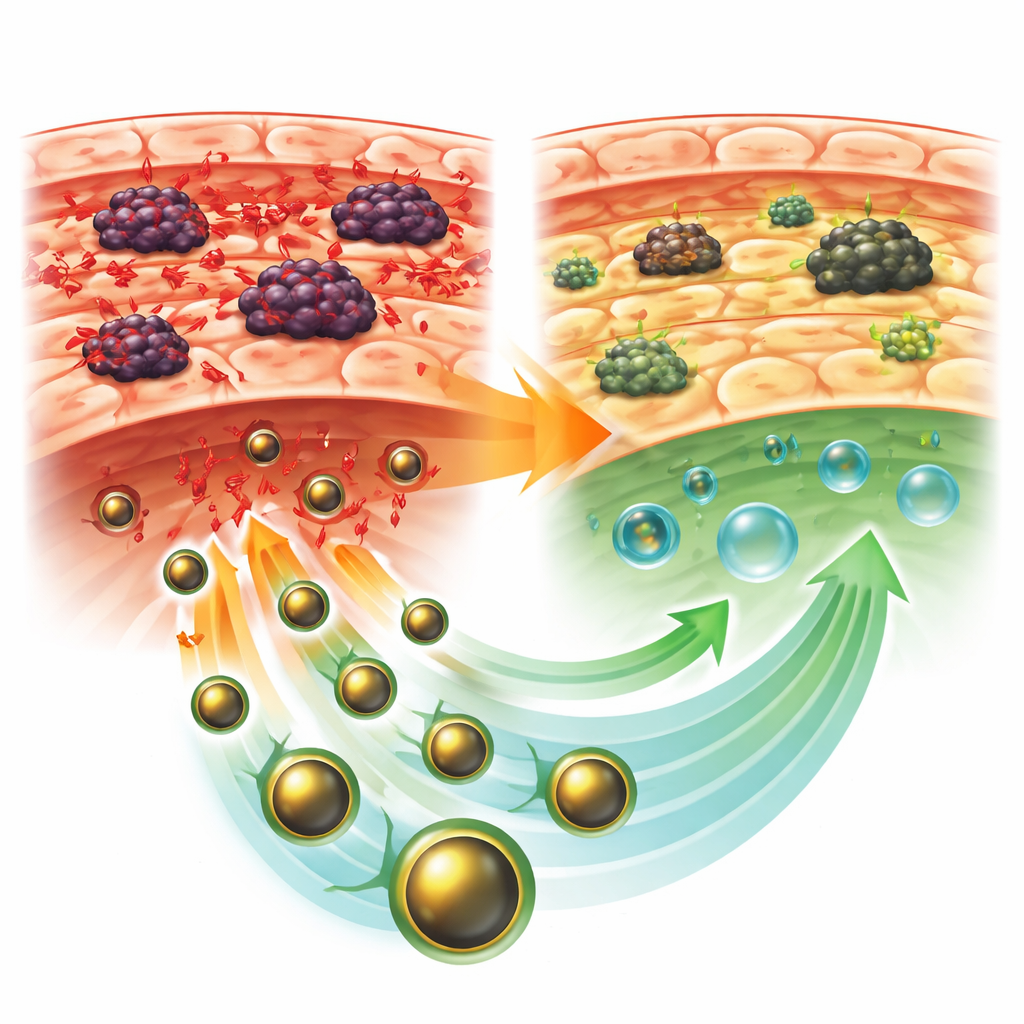
ストレスと損傷から肝臓を守る
治療を受けない腫瘍保有マウスでは、典型的な肝障害像が観察されました。肝細胞が損傷すると血中に漏れ出す酵素が著しく上昇し、有用な血中タンパク質は低下しました。肝臓内では酸化の有害な副産物が増加し、防御的な酵素やグルタチオンといった抗酸化物質は減少しました。組織の切片を顕微鏡で見ると、肝臓の構造が乱れ、細胞の腫脹や壊死、瘢痕様変化、大量の炎症細胞浸潤が確認されました。対照的に、GLONFで処置されたマウスは腫瘍が小さく、肝臓の状態も著しく改善していました。血液検査値は正常に近づき、酸化的損傷は減少し、特に腫瘍形成後にGLONFを投与した群では抗酸化防御が回復していました。
暴走する細胞シグナルの沈静化
研究チームは肝細胞内の二つの重要なタンパク質も解析しました。ひとつは細胞増殖に関連するPCNA、もうひとつはDNA損傷に応答して細胞死を誘導し得るP53です。未治療の腫瘍保有マウスでは、これら両方のマーカーが強く上昇しており、強いストレスと制御不能な修復試行を示していました。GLONF処置により肝組織中のこれらマーカーの量は顕著に低下し、ナノシステムが緊急修復の必要性を減らし、細胞環境の安定化に寄与したことを示唆します。これは生化学的および構造的所見と整合し、酸化ストレスと損傷の総合的な緩和を示しています。
将来のがん医療にとっての意義
まとめると、本研究は磁性応答性を持つ糖類ベースのナノ運搬体GLONFが、マウスにおいて腫瘍を縮小させると同時に肝臓の深刻な損傷を防げる可能性を示しています。標的送達と抗酸化・代謝効果を組み合わせることで、重要な臓器にやさしいがん治療の一形態を提供し得ます。これらの結果はまだ動物実験段階であり臨床応用には程遠いものの、精巧に設計されたナノ構造が将来の治療で腫瘍を攻撃しつつ体の自然なフィルターを保護する助けとなり得ることを示しています。
引用: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
キーワード: ナノ医療, 肝臓保護, 乳がんモデル, 酸化ストレス, 薬物送達