Clear Sky Science · fr
Modulation du stress oxydatif et des voies P53/PCNA par des nanoferrites chargées en glucosodiene (GLONF) dans l’hépatotoxicité induite par la tumeur solide d’Ehrlich
Pourquoi cette recherche est importante
Les traitements du cancer endommagent souvent des organes sains, en particulier le foie, chargé de métaboliser de nombreux médicaments et résidus tumoraux. Cette étude explore un nouveau vecteur extrêmement petit et guidable magnétiquement, qui délivre un composé anticancéreux dérivé du sucre directement vers les tumeurs tout en protégeant le foie des dommages. Pour le lecteur, elle donne un aperçu de la façon dont la nanotechnologie et la chimie intelligente pourraient un jour rendre les traitements du cancer plus efficaces et moins toxiques.
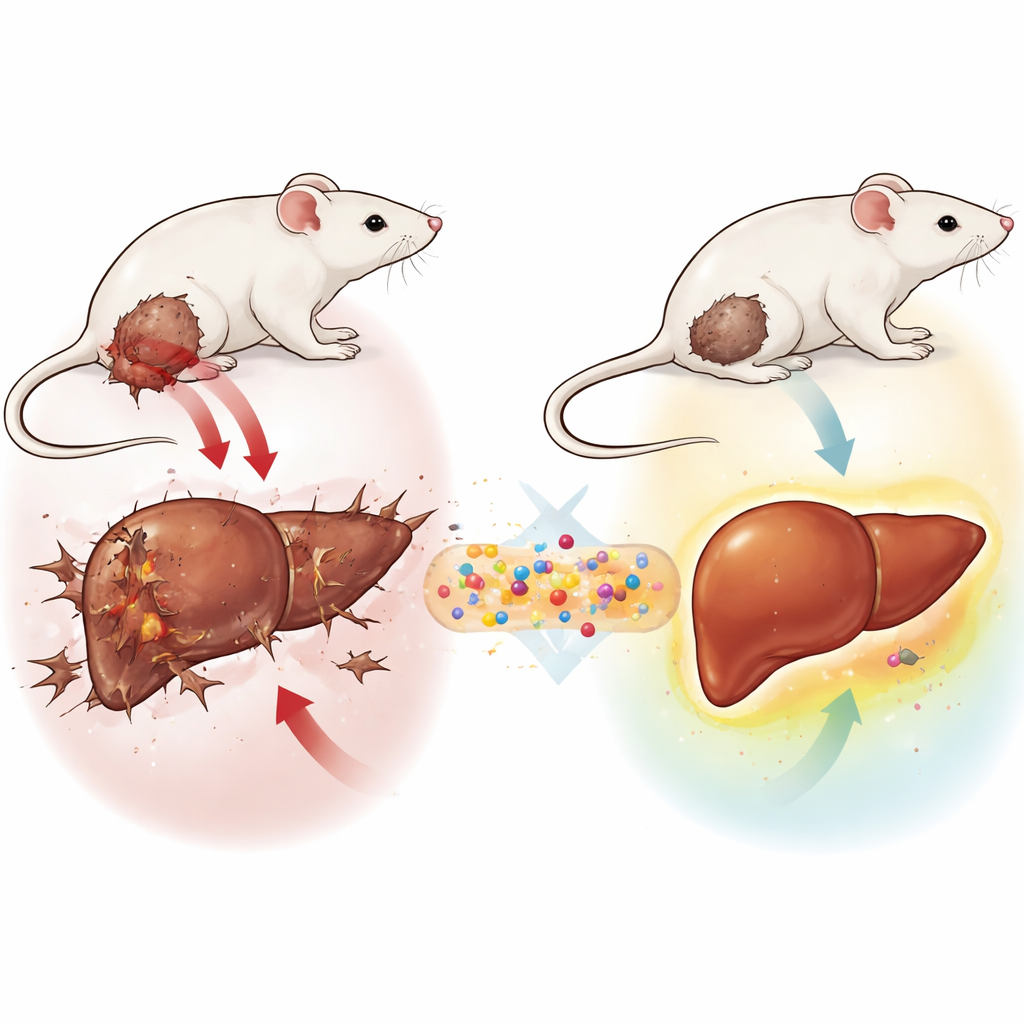
Un minuscule système de livraison à la mission majeure
Les chercheurs ont mis au point un système nano-structuré en trois parties appelé GLONF. En son cœur se trouve un noyau minéral magnétique composé d’un matériau à base de fer particulier. Autour de ce noyau, ils ont ajouté une coque naturelle à base de sucre appelée chitosane, souvent utilisée en biomédecine pour sa sécurité et sa stabilité. Enfin, ils ont greffé une nouvelle molécule dérivée du sucre nommée glucosodiene, conçue pour perturber l’appétit des cellules cancéreuses pour le glucose et pour atténuer l’environnement acide et agressif autour des tumeurs. Ensemble, ces composants forment un véhicule miniature qui peut, en principe, être guidé par des aimants, circuler en toute sécurité dans l’organisme et libérer un agent anticancéreux là où il est le plus nécessaire.
Tests dans un modèle murin de cancer d’apparence mammaire
Pour évaluer si le GLONF pouvait protéger le foie pendant le cancer, l’équipe a utilisé un modèle murin bien établi appelé tumeur solide d’Ehrlich. Cette tumeur, initialement dérivée du tissu mammaire, croît rapidement sous la peau et reproduit de nombreuses caractéristiques des cancers humains agressifs. Des souris femelles ont été réparties en groupes : certaines sont restées saines, certaines n’ont reçu que la nano-formulation, d’autres ont développé la tumeur sans traitement, et d’autres encore ont reçu le GLONF soit au moment de l’implantation tumorale soit après formation de la tumeur. Les scientifiques ont ensuite mesuré la taille des tumeurs, des marqueurs sanguins standard de la santé hépatique, ainsi qu’une série d’indicateurs chimiques et microscopiques de dommages et de réparation au sein du foie.
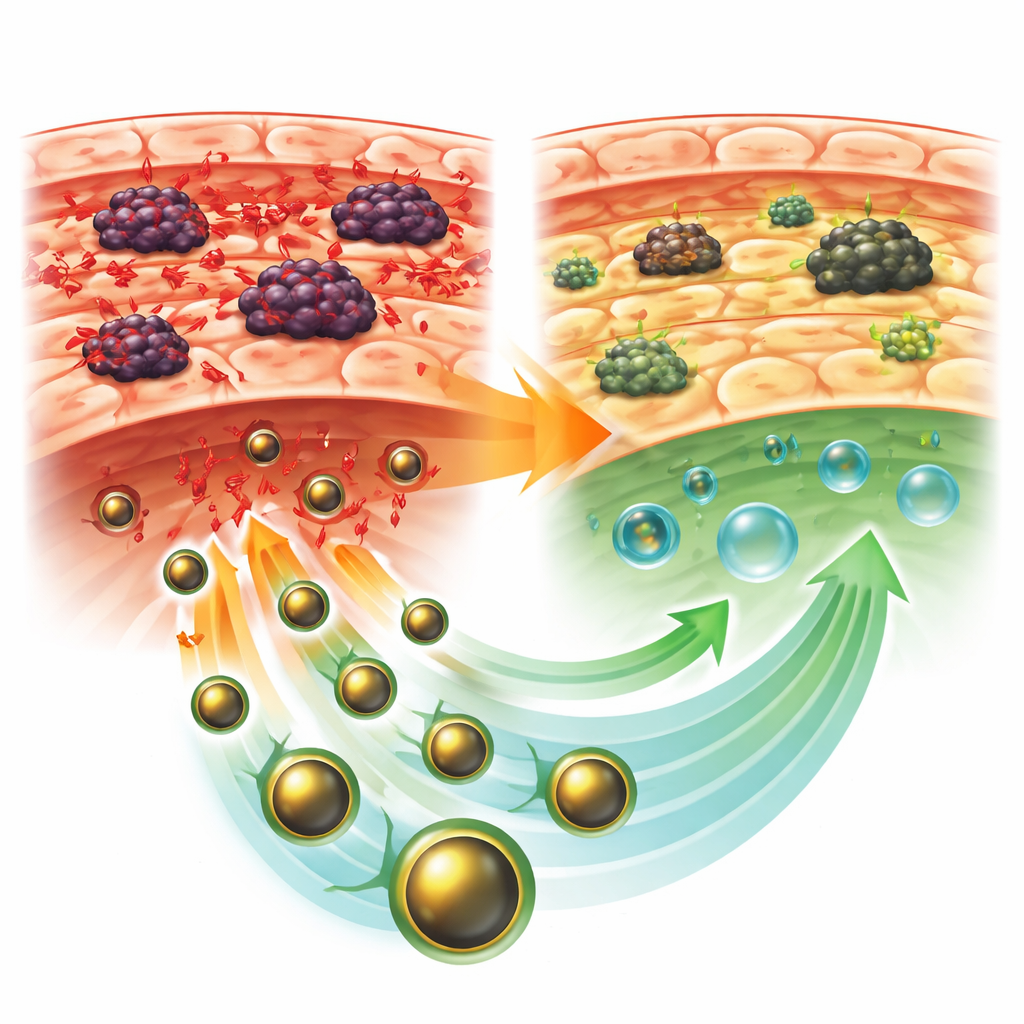
Protéger le foie du stress et des dommages
Les souris porteuses de tumeurs non traitées présentaient un tableau classique de lésion hépatique. Les enzymes fuyant vers le sang lorsque les cellules hépatiques sont endommagées augmentaient fortement, tandis que les protéines sanguines bénéfiques diminuaient. Dans le foie, les niveaux de sous-produits nocifs de l’oxydation étaient accrus et les défenses naturelles, comme les enzymes protectrices et le glutathion, chutaient. Les coupes tissulaires au microscope révélaient une architecture hépatique déformée, avec des cellules enflées et en train de mourir, des transformations fibreuses et une importante infiltration inflammatoire. En revanche, les souris traitées par GLONF présentaient des tumeurs plus petites et des foies sensiblement plus sains. Leurs analyses sanguines revenaient vers la normale, les dommages oxydatifs étaient réduits et les défenses antioxydantes se rétablissaient, surtout lorsque le GLONF était administré après la formation de la tumeur.
Apaiser des signaux cellulaires déchaînés
L’équipe a également examiné deux protéines clés à l’intérieur des cellules hépatiques. L’une, la PCNA, est associée à la prolifération cellulaire, et l’autre, P53, répond aux lésions de l’ADN et peut déclencher la mort cellulaire. Chez les souris porteuses de tumeurs non traitées, ces deux marqueurs étaient fortement augmentés, signalant un stress intense et des tentatives de réparation incontrôlées. Le traitement par GLONF réduisait notablement l’abondance de ces marqueurs dans le tissu hépatique, suggérant que le nano-système diminuait le besoin de réparations d’urgence et contribuait à stabiliser l’environnement cellulaire. Cela concorde avec les observations biochimiques et structurales, indiquant un apaisement coordonné du stress oxydatif et des lésions.
Ce que cela pourrait signifier pour les soins anticancéreux futurs
En synthèse, ce travail montre que le GLONF, un nanovecteur sucré réactif aux champs magnétiques, peut réduire la taille des tumeurs chez la souris tout en protégeant le foie de lésions sévères. En combinant une délivrance ciblée avec des effets antioxydants et métaboliques, ce système offre une voie potentielle pour rendre les traitements anticancéreux moins agressifs pour les organes vitaux. Bien que ces résultats restent précliniques et encore loin d’une application clinique courante, ils démontrent comment des nanostructures soigneusement conçues pourraient aider les thérapies futures à attaquer les tumeurs tout en épargnant les filtres naturels de l’organisme.
Citation: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Mots-clés: nanomédecine, protection du foie, modèle de cancer du sein, stress oxydatif, libération de médicament