Clear Sky Science · zh
印度非HLA基因多态性与乳糜泻的关联
这为何与日常饮食相关
乳糜泻把一种常见的食物主食——小麦,变成引发慢性肠道损伤的触发因子。本研究提出了一个简单但重要的问题:除了最知名的风险基因外,还有哪些遗传特征决定在印度谁会因食用面筋而生病,谁能保持健康,即便两组人携带相似的主要风险基因?
更近地观察面筋与肠道
乳糜泻是一种免疫相关疾病,食用存在于小麦、大麦和黑麦中的蛋白质面筋会损伤小肠。其在欧洲、北美及以小麦为主食的印度部分地区的患病率约为1%。已知的主要遗传风险位于一类免疫系统基因——HLA DQ家族,这些基因帮助免疫细胞识别面筋片段。携带某些等位型的人,尤其是被称为DQ2.5、DQ2.2和DQ8的类型,患病概率明显更高。然而,许多携带这些基因的人从未发病,这表明其他遗传因素也在决定风险中发挥作用。
研究者要寻找的内容
研究团队招募了来自印度不同地区的376名乳糜泻成人患者和736名无病对照成人。从先前的大型基因调查中,他们挑选出63个小的DNA变体,即单核苷酸多态性(SNP),这些位点位于被怀疑影响免疫反应的基因中。首先他们检查了哪些变体在印度血统人群中具有足够的存在频率。经过这一筛选步骤后,在主HLA区域和许多非HLA基因中的51个遗传位点被用于比较患者与健康对照中各等位型的出现频率。
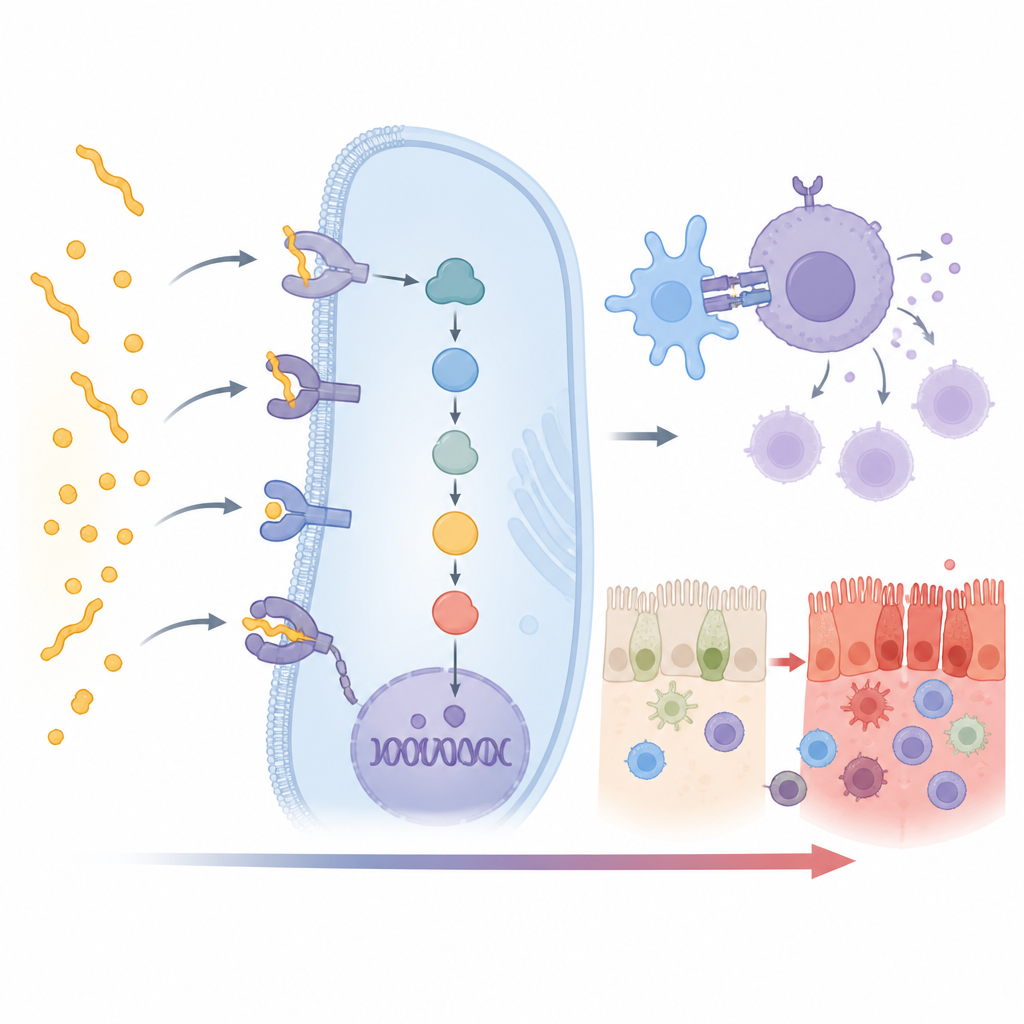
免疫反应中的隐性助力者
正如预期的那样,最强的信号来自HLA DQ2.5类型,DQ2.2和DQ8也显示出较弱但依然明确的关联。更有趣的是,另有15个非HLA基因在该印度人群中也与乳糜泻显著相关。许多基因直接位于将面筋识别转化为全面免疫反应的事件链中。一些基因,如CD247、CD28、CD80和PRKCQ,参与T细胞的启动——驱动疾病的白细胞。另一些基因,如UBASH3A和TNFAIP3,则充当制动器,通常抑制这种活化不至于失控。这些基因的变异可能使免疫反应倾向于增强或减弱。
保护肠道上皮并引导免疫细胞
若干相关基因影响肠道上皮本身的健康或免疫细胞的迁移。CCR3和CCR4帮助引导免疫与炎症细胞进入组织,可能将更多此类细胞导向存在面筋的小肠。GATD3和PARK7与线粒体处理应激的方式有关,可能帮助肠上皮细胞应对炎症和活性氧引起的损伤。INAVA支持维持肠道屏障的紧密连接,而DDX6、PUS10以及一个名为LINC01934的长非编码RNA影响RNA的处理和基因的开关调控。综上,这些变化描绘了一条从面筋接触、经过免疫信号传导直到肠表面受损的路径。
拼接出遗传网络
通过分析不同DNA变体之间的相互作用,研究者发现这些位点呈现出一个紧密相连的网络,而不是许多孤立的效应。某些变体显现为枢纽,与其他位点有大量统计学关联。当团队将这些位点对应到基因时,枢纽角色由若干关键免疫与信号传导基因承担,包括一些HLA II类基因、控制细胞迁移的趋化因子受体以及T细胞活化分子。该网络模式支持这样一种观点:沿同一路径的多个小遗传推力共同决定面筋暴露是否会将个体推向疾病。
这对有风险的人意味着什么
对读者来说,主要结论是印度的乳糜泻风险并非由单一基因决定,而是一簇在免疫细胞与肠道上皮中相互作用的基因共同塑造。经典的HLA风险类型仍然至关重要,但额外的遗传差异——如T细胞如何被激活、信号如何被抑制、免疫细胞如何移动以及肠壁如何维持完整——都会影响最终结果。随着对这些通路理解的加深,它们可用于细化已携带高风险HLA类型人群的遗传风险评分,并最终可能指出在不完全依赖终生严格饮食改变的情况下,平抑对面筋免疫反应的新方法。
引用: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
关键词: 乳糜泻, 面筋, HLA-DQ基因, T细胞活化, 遗传风险