Clear Sky Science · sv
Associationer mellan icke-HLA-genpolymorfismer och celiaki i Indien
Varför detta betyder något för vardagskosten
Celiaki förvandlar en vanlig basvara, vete, till en utlösare av kronisk tarmskada. Denna studie ställer en enkel men viktig fråga: bortom de mest kända riskgenerna, vilka andra ärftliga egenskaper bidrar till att avgöra vem i Indien som blir sjuk av att äta gluten och vem som förblir frisk, även när båda grupperna bär likartade huvudsakliga riskgener?
En närmare titt på gluten och tarmen
Celiaki är ett immunologiskt tillstånd där intag av gluten, ett protein i vete, korn och råg, skadar tunntarmen. Det drabbar omkring 1 procent av befolkningen i Europa, Nordamerika och veteätande regioner i Indien. Den främsta kända genetiska risken ligger i en familj av immunsystemgener som kallas HLA‑DQ, vilka hjälper immunceller att känna igen glutenfragment. Personer som bär vissa varianter, särskilt de som kallas DQ2.5, DQ2.2 och DQ8, har mycket högre sannolikhet att utveckla sjukdomen. Ändå blir många med dessa gener aldrig sjuka, vilket tyder på att andra ärftliga faktorer också formar risken.
Vad forskarna ville ta reda på
Teamet studerade 376 vuxna med celiaki och 736 vuxna utan sjukdomen från olika delar av Indien. Från tidigare stora genetiska undersökningar valde de 63 små DNA‑varianter, så kallade single nucleotide polymorphisms (SNP), i gener som misstänks påverka immunresponsen. Först kontrollerade de vilka av dessa varianter som alls förekommer i användbara frekvenser hos personer av indiskt ursprung. Efter detta screeningsteg testades 51 genetiska platser i både huvud‑HLA‑regionen och många icke‑HLA‑gener för hur ofta varje variant förekom hos patienter jämfört med friska kontroller.
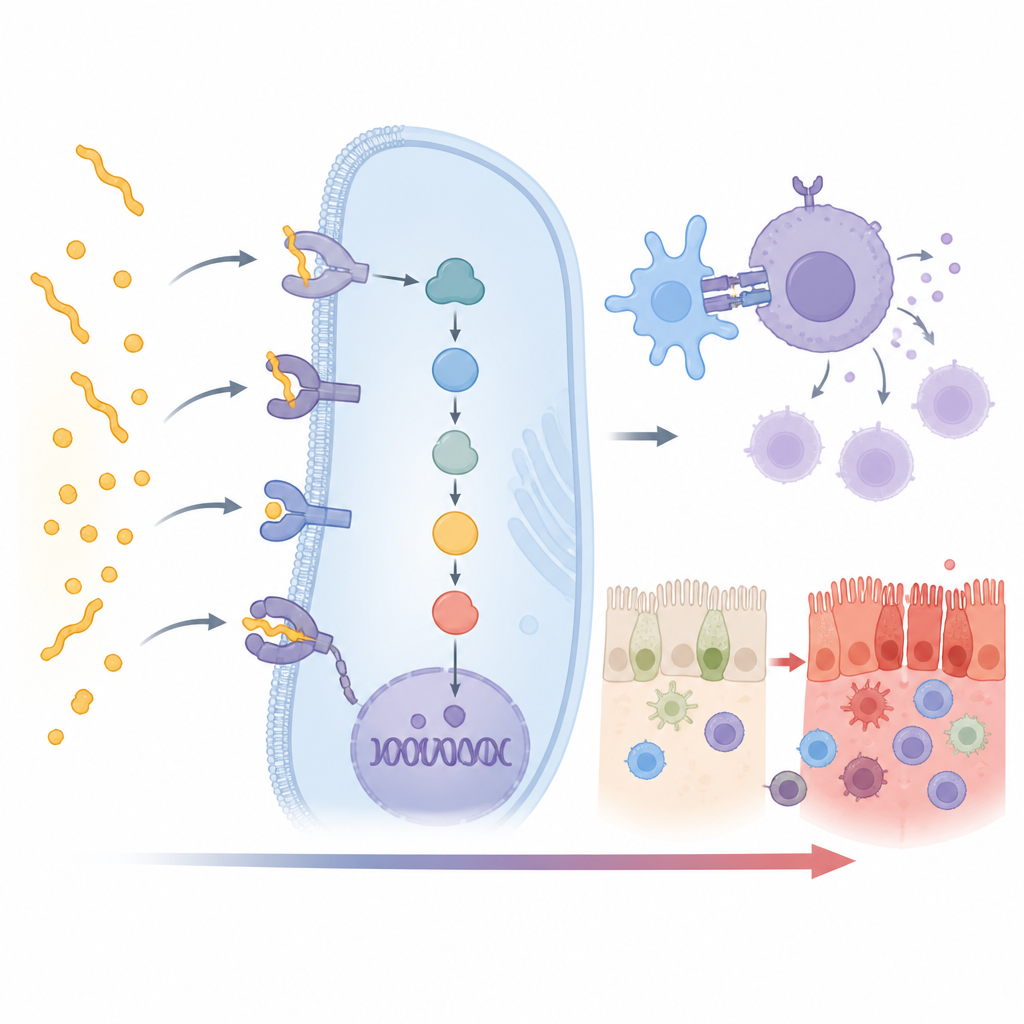
Dolda medhjälpare i immunresponsen
Som förväntat gav formen HLA DQ2.5 den starkaste signalen, med svagare men ändå tydliga samband för DQ2.2 och DQ8. Mer intressant var att 15 ytterligare icke‑HLA‑gener också visade stark koppling till celiaki i denna indiska grupp. Många ligger direkt i händelsekedjan som förvandlar glutenigenkänning till ett fullskaligt immunsvar. Vissa gener, såsom CD247, CD28, CD80 och PRKCQ, hjälper till att slå på T‑cellerna, de vita blodkroppar som driver sjukdomen. Andra, som UBASH3A och TNFAIP3, fungerar som bromsar som normalt hindrar denna aktivering från att löpa amok. Förändringar i dessa gener kan förskjuta balansen mot antingen starkare eller svagare immunreaktioner.
Skydd för tarmens yta och styrning av immunceller
Flera av de associerade generna påverkar själva tarmens slemhinnehälsa eller immuncellernas rörelse. CCR3 och CCR4 hjälper till att styra immuna och inflammatoriska celler in i vävnader, vilket potentiellt leder fler sådana celler till tunntarmen där gluten finns. GATD3 och PARK7 är kopplade till hur mitokondrier hanterar stress och kan hjälpa tarmceller att tåla skada orsakad av inflammation och reaktiva syreradikaler. INAVA stödjer de täta fogarna som håller tarmbarriären tät, medan DDX6, PUS10 och ett långt icke‑kodat RNA kallat LINC01934 påverkar hur RNA bearbetas och hur gener slås av och på. Tillsammans skisserar dessa förändringar en kedja som leder från glutenkontakt, via immunologisk signalering, till skada på tarmytan.
Sätta ihop det genetiska nätverket
Genom att analysera hur de olika DNA‑varianterna interagerar med varandra fann forskarna ett tätt kopplat nätverk av platser snarare än många isolerade effekter. Vissa varianter framträdde som nav, med många statistiska kopplingar till andra. När teamet kartlade motsvarande gener fylldes navroller av viktiga immun‑ och signaleringsgener, inklusive flera HLA klass II‑gener, kemokinreceptorer som styr cellmigration och molekyler för T‑cellsaktivering. Detta nätverksmönster stöder bilden av att många små genetiska bidrag längs samma bana samverkar för att avgöra om glutenexponering får en person att utveckla sjukdomen.
Vad detta betyder för personer i riskzonen
Huvudpoängen för läsaren är att risken för celiaki i Indien inte bestäms av en enda gen utan av en kluster av gener som kommunicerar med varandra i immunceller och i tarmens slemhinna. De klassiska HLA‑risktyperna förblir centrala, men ytterligare ärftliga skillnader i hur T‑celler slås på, hur signaler dämpas, hur immunceller rör sig och hur tarmväggen håller ihop bidrar alla till slutresultatet. När dessa vägar blir bättre kartlagda kan de hjälpa till att förfina genetiska riskscorer för personer som redan bär högrisk‑HLA‑typer och så småningom peka mot nya sätt att dämpa immunresponsen mot gluten utan att enbart förlita sig på strikt livslång kostförändring.
Citering: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Nyckelord: celiaki, gluten, HLA‑DQ‑gener, T‑cellsaktivering, genetisk risk