Clear Sky Science · de
Assoziationen von Nicht‑HLA‑Genpolymorphismen mit Zöliakie in Indien
Warum das für alltägliche Ernährung wichtig ist
Zöliakie verwandelt ein verbreitetes Grundnahrungsmittel, Weizen, in einen Auslöser chronischer Darmschäden. Diese Studie stellt eine einfache, aber wichtige Frage: Abgesehen von den bekanntesten Risikogenen, welche anderen vererbten Merkmale entscheiden, wer in Indien durch Gluten krank wird und wer gesund bleibt, selbst wenn beide Gruppen ähnliche Hauptrisikogene tragen?
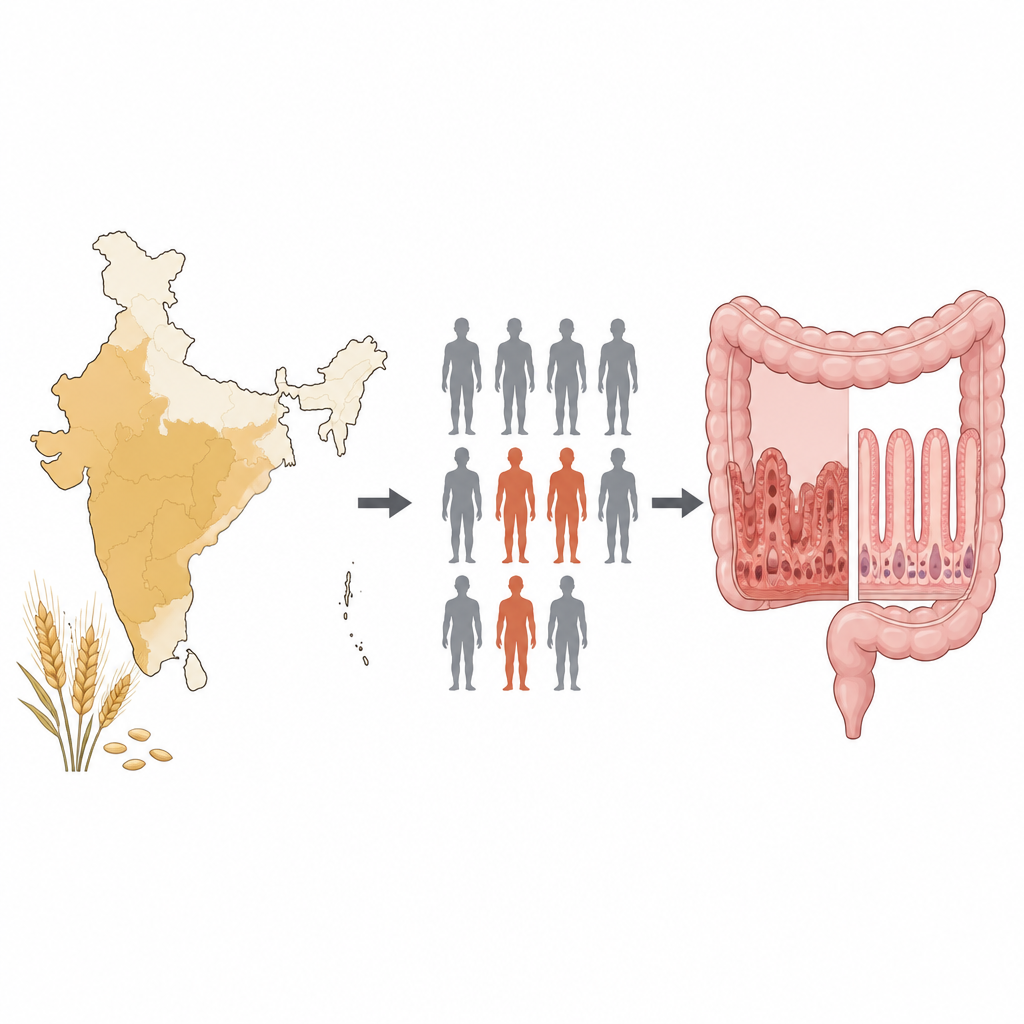
Ein genauerer Blick auf Gluten und den Darm
Zöliakie ist eine Immunerkrankung, bei der der Verzehr von Gluten — einem Protein in Weizen, Gerste und Roggen — den Dünndarm schädigt. Sie betrifft etwa 1 Prozent der Menschen in Europa, Nordamerika und weizenessenden Regionen Indiens. Das wichtigste bekannte genetische Risiko liegt in einer Familie von Immungenen, den HLA‑DQ‑Genen, die Immunzellen helfen, Gluten‑Fragmente zu erkennen. Menschen mit bestimmten Varianten, besonders DQ2.5, DQ2.2 und DQ8, haben ein deutlich erhöhtes Erkrankungsrisiko. Viele Träger dieser Gene erkranken jedoch nie, was darauf hindeutet, dass weitere vererbte Faktoren das Risiko mitbestimmen.
Was die Forschenden herausfinden wollten
Das Team untersuchte 376 Erwachsene mit Zöliakie und 736 gesunde Kontrollpersonen aus verschiedenen Regionen Indiens. Aus früheren großen genetischen Studien wählten sie 63 einzelne DNA‑Veränderungen, sogenannte Single‑Nucleotide‑Polymorphismen (SNPs), in Genen aus, die vermutlich die Immunantwort beeinflussen. Zunächst prüften sie, welche dieser Varianten in Menschen indianischer Abstammung überhaupt in nützlicher Häufigkeit vorkommen. Nach dieser Vorauswahl wurden 51 genetische Stellen sowohl im Haupt‑HLA‑Bereich als auch in vielen Nicht‑HLA‑Genen daraufhin getestet, wie oft jede Variante bei Patienten im Vergleich zu gesunden Kontrollen vorkommt.
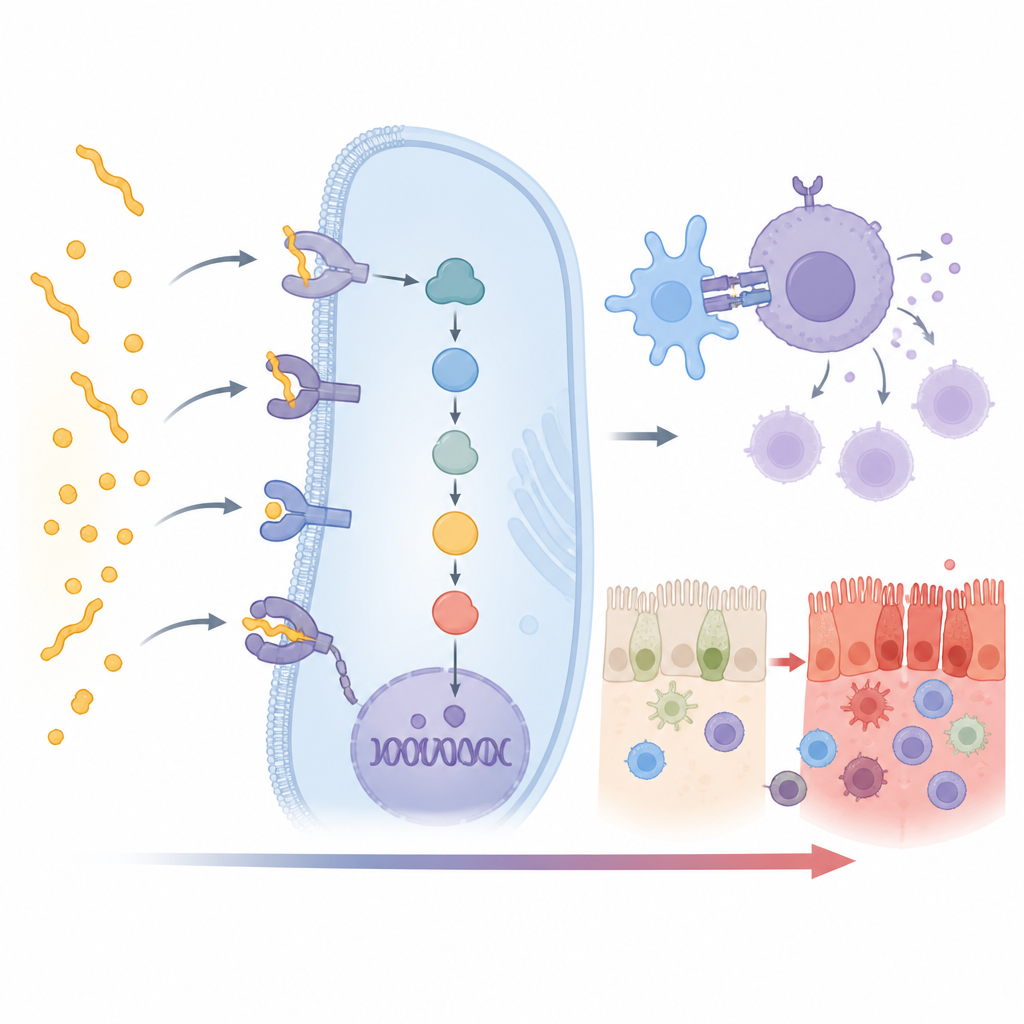
Verborgene Helfer in der Immunantwort
Wie erwartet lieferte die HLA‑DQ2.5‑Variante das stärkste Signal, mit schwächeren, aber noch klaren Verknüpfungen zu DQ2.2 und DQ8. Interessanterweise zeigten 15 zusätzliche Nicht‑HLA‑Gene ebenfalls eine starke Assoziation mit Zöliakie in dieser indischen Gruppe. Viele davon sitzen direkt in der Kaskade, die aus der Glutenerkennung eine umfassende Immunreaktion macht. Einige Gene, wie CD247, CD28, CD80 und PRKCQ, helfen bei der Aktivierung von T‑Zellen — den weißen Blutzellen, die die Erkrankung antreiben. Andere, etwa UBASH3A und TNFAIP3, wirken als Bremsen, die normalerweise verhindern, dass diese Aktivierung außer Kontrolle gerät. Veränderungen in diesen Genen können das Gleichgewicht zugunsten stärkerer oder schwächerer Immunreaktionen verschieben.
Schutz der Darmschleimhaut und Steuerung von Immunzellen
Mehrere der assoziierten Gene beeinflussen die Gesundheit der Darmoberfläche selbst oder die Bewegung von Immunzellen. CCR3 und CCR4 helfen dabei, Immun‑ und Entzündungszellen in Gewebe zu lenken und könnten so mehr dieser Zellen in den Dünndarm führen, wo Gluten vorhanden ist. GATD3 und PARK7 stehen im Zusammenhang damit, wie Mitochondrien mit Stress umgehen, und könnten Darmzellen helfen, Schäden durch Entzündung und reaktive Sauerstoffspezies zu bewältigen. INAVA stützt die Tight Junctions, die die Darmbarriere abdichten, während DDX6, PUS10 und eine lange nichtkodierende RNA namens LINC01934 beeinflussen, wie RNA verarbeitet wird und wie Gene an‑ oder abgeschaltet werden. Zusammengenommen zeichnen diese Veränderungen eine Kette nach, die vom Kontakt mit Gluten über Immun‑Signalwege bis zur Schädigung der Darmoberfläche führt.
Das genetische Netzwerk zusammensetzen
Durch die Analyse, wie die verschiedenen DNA‑Veränderungen miteinander interagieren, fanden die Forschenden eher ein dicht verknüpftes Netzwerk von Stellen als viele isolierte Effekte. Bestimmte Varianten traten als Knotenpunkte auf und zeigten zahlreiche statistische Verbindungen zu anderen. Beim Zuordnen der entsprechenden Gene übernahmen Schlüsselgene der Immunantwort und Signalübertragung diese Hub‑Rollen, darunter mehrere HLA‑Klasse‑II‑Gene, Chemokinrezeptoren, die die Zellmigration steuern, sowie Moleküle der T‑Zell‑Aktivierung. Dieses Netzwerkmuster stützt die Auffassung, dass viele kleine genetische Einflüsse entlang derselben Bahn zusammenwirken und letztlich bestimmen, ob Glutenexposition eine Person in die Krankheit kippen lässt.
Was das für Menschen mit Risiko bedeutet
Für die Leserschaft ist die wichtigste Erkenntnis, dass das Zöliakie‑Risiko in Indien nicht von einem einzigen Gen bestimmt wird, sondern von einem Bündel von Genen, die in Immunzellen und in der Darmwand miteinander kommunizieren. Die klassischen HLA‑Risikotypen bleiben zentral, aber zusätzliche vererbte Unterschiede darin, wie T‑Zellen aktiviert werden, wie Signale gedämpft werden, wie Immunzellen wandern und wie die Darmwand zusammenhält, tragen alle zum Endergebnis bei. Mit besserem Verständnis dieser Signalwege könnten genetische Risikoscores für Menschen mit hohen HLA‑Risikotypen verfeinert werden und langfristig neue Ansätze eröffnen, die Immunreaktion auf Gluten zu beruhigen, ohne ausschließlich auf strikt lebenslange Diätumstellungen angewiesen zu sein.
Zitation: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Schlüsselwörter: Zöliakie, Gluten, HLA‑DQ‑Gene, T‑Zell‑Aktivierung, genetisches Risiko