Clear Sky Science · es
Asociaciones de polimorfismos genéticos no HLA con la enfermedad celíaca en India
Por qué esto importa para las dietas diarias
La enfermedad celíaca convierte un alimento básico común, el trigo, en un desencadenante de lesión crónica del intestino. Este estudio plantea una pregunta simple pero importante: más allá de los genes de riesgo mejor conocidos, ¿qué otros rasgos heredados ayudan a decidir quién en India enferma por comer gluten y quién se mantiene sano, incluso cuando ambos grupos portan genes de riesgo principales similares?
Una mirada más cercana al gluten y el intestino
La enfermedad celíaca es una condición inmunitaria en la que comer gluten, una proteína del trigo, la cebada y el centeno, daña el intestino delgado. Afecta alrededor del 1 por ciento de la población en Europa, Norteamérica y las regiones consumidoras de trigo de India. El principal riesgo genético conocido reside en una familia de genes del sistema inmune llamada HLA DQ, que ayudan a las células inmunitarias a reconocer fragmentos de gluten. Las personas que llevan ciertas variantes, especialmente las denominadas DQ2.5, DQ2.2 y DQ8, tienen mucha más probabilidad de desarrollar la enfermedad. Sin embargo, muchas personas con estos genes nunca enferman, lo que sugiere que otros factores hereditarios también modulan el riesgo.
Qué buscaban los investigadores
El equipo estudió a 376 adultos con enfermedad celíaca y 736 adultos sin la enfermedad procedentes de distintas partes de India. A partir de encuestas genéticas previas a gran escala, eligieron 63 pequeños cambios en el ADN, conocidos como polimorfismos de un solo nucleótido, en genes sospechosos de influir en la respuesta inmune. Primero comprobaron cuáles de estos cambios están presentes en niveles útiles en personas de ascendencia india. Tras este paso de cribado, se probaron 51 sitios genéticos tanto en la región HLA principal como en muchos genes no HLA para ver con qué frecuencia aparecía cada variante en pacientes comparados con controles sanos.
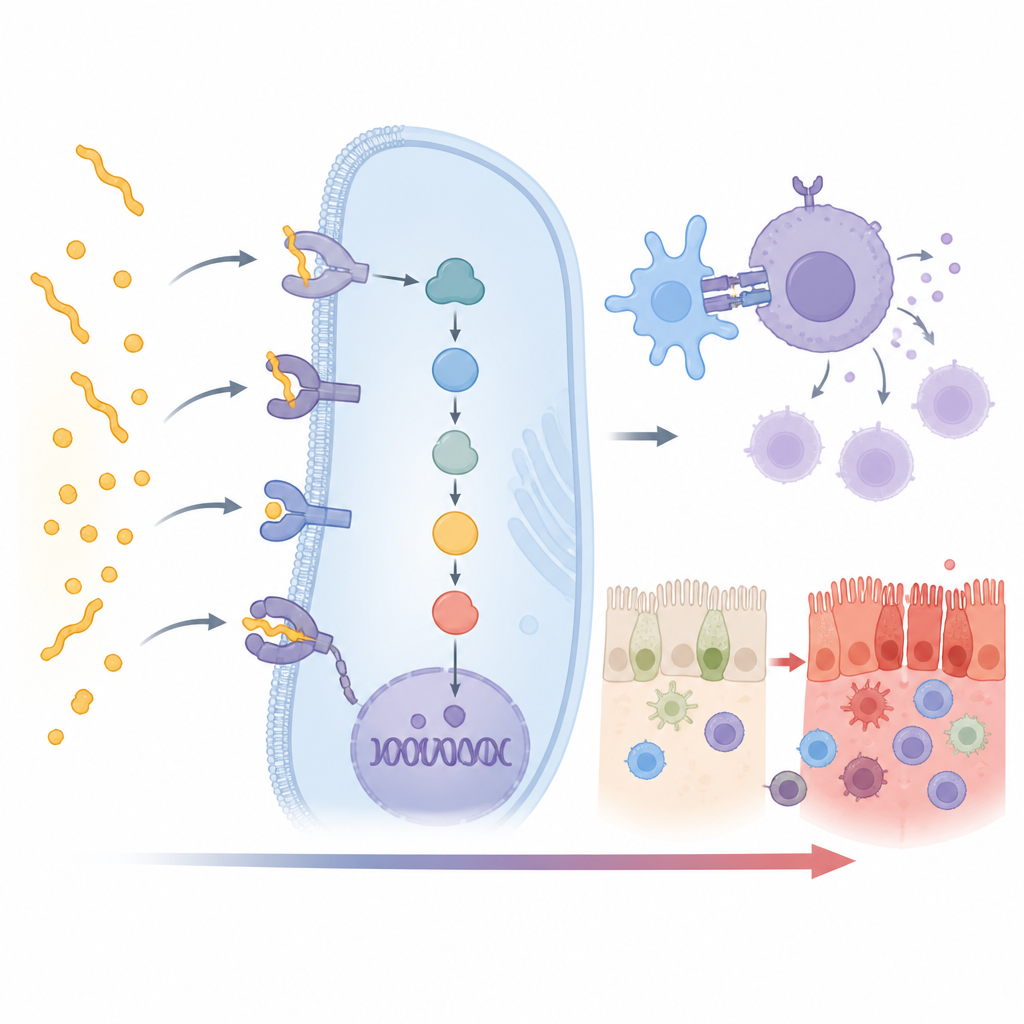
Ayudantes ocultos en la respuesta inmunitaria
Como era de esperar, la señal más fuerte provino de la forma HLA DQ2.5, con vínculos más débiles pero todavía claros con DQ2.2 y DQ8. Más intrigante fue que 15 genes no HLA adicionales también mostraron una asociación fuerte con la enfermedad celíaca en este grupo indio. Muchos se sitúan directamente en la cadena de eventos que convierte el reconocimiento del gluten en un ataque inmunitario pleno. Algunos genes, como CD247, CD28, CD80 y PRKCQ, ayudan a activar los linfocitos T, las células blancas que impulsan la enfermedad. Otros, como UBASH3A y TNFAIP3, actúan como frenos que normalmente evitan que esta activación se descontrole. Los cambios en estos genes pueden inclinar la balanza hacia reacciones inmunitarias más fuertes o más débiles.
Protegiendo el revestimiento intestinal y guiando a las células inmunitarias
Varios de los genes asociados afectan la salud del revestimiento intestinal en sí o el movimiento de las células inmunitarias. CCR3 y CCR4 ayudan a guiar células inmunitarias e inflamatorias hacia los tejidos, potencialmente dirigiendo más de estas células al intestino delgado donde está presente el gluten. GATD3 y PARK7 se vinculan con cómo las mitocondrias gestionan el estrés y pueden ayudar a las células intestinales a soportar el daño causado por la inflamación y los radicales reactivos. INAVA sostiene las uniones estrechas que mantienen sellada la barrera intestinal, mientras que DDX6, PUS10 y un ARN largo no codificante llamado LINC01934 influyen en cómo se procesa el ARN y cómo se activan o desactivan los genes. En conjunto, estos cambios delinean una cadena que va desde el contacto con el gluten, pasando por la señalización inmune, hasta la lesión de la superficie intestinal.
Armando la red genética
Al analizar cómo interactúan los distintos cambios en el ADN, los investigadores encontraron una red de sitios estrechamente vinculados más que muchos efectos aislados. Ciertas variantes emergieron como nodos centrales, mostrando muchas conexiones estadísticas con otras. Cuando el equipo mapeó los genes correspondientes, los papeles de nodo fueron ocupados por genes clave de inmunidad y señalización, incluidos varios genes HLA de clase II, receptores de quimocinas que controlan la migración celular y moléculas de activación de linfocitos T. Este patrón de red apoya la idea de que muchas pequeñas influencias genéticas a lo largo de la misma vía se combinan para determinar si la exposición al gluten empuja a una persona hacia la enfermedad.
Qué significa esto para las personas en riesgo
Para los lectores, la conclusión principal es que el riesgo de enfermedad celíaca en India no lo define un único gen, sino un cúmulo de genes que se comunican entre sí en las células inmunitarias y en el revestimiento intestinal. Los tipos de riesgo HLA clásicos siguen siendo esenciales, pero las diferencias hereditarias adicionales en cómo se activan los linfocitos T, cómo se atenúan las señales, cómo se desplazan las células inmunitarias y cómo se mantiene la pared intestinal contribuyen al resultado final. A medida que se comprendan mejor estas vías, podrían ayudar a afinar las puntuaciones de riesgo genético para personas que ya portan tipos HLA de alto riesgo y, eventualmente, señalar nuevas formas de calmar la respuesta inmunitaria al gluten sin depender únicamente de cambios dietéticos estrictos de por vida.
Cita: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Palabras clave: enfermedad celíaca, gluten, genes HLA-DQ, activación de linfocitos T, riesgo genético