Clear Sky Science · fr
Associations des polymorphismes de gènes non-HLA avec la maladie cœliaque en Inde
Pourquoi cela compte pour les régimes de tous les jours
La maladie cœliaque transforme une alimentation courante, le blé, en déclencheur d’une atteinte chronique de l’intestin. Cette étude pose une question simple mais importante : au-delà des gènes de risque les mieux connus, quels autres traits hérités aident à déterminer qui, en Inde, tombe malade en mangeant du gluten et qui reste en bonne santé, même lorsque les deux groupes portent des gènes de risque principaux similaires ?
Un regard plus précis sur le gluten et l’intestin
La maladie cœliaque est un trouble immunitaire dans lequel la consommation de gluten, une protéine du blé, de l’orge et du seigle, endommage l’intestin grêle. Elle touche environ 1 % des personnes en Europe, en Amérique du Nord et dans les régions indiennes où le blé est consommé. Le principal risque génétique connu réside dans une famille de gènes du système immunitaire appelés HLA DQ, qui aident les cellules immunitaires à reconnaître des fragments de gluten. Les personnes porteuses de certaines formes, en particulier celles appelées DQ2.5, DQ2.2 et DQ8, ont beaucoup plus de chances de développer la maladie. Pourtant, de nombreuses personnes portant ces gènes ne tombent jamais malades, ce qui suggère que d’autres facteurs héréditaires modulent aussi le risque.
Ce que les chercheurs ont voulu découvrir
L’équipe a étudié 376 adultes atteints de maladie cœliaque et 736 adultes sans la maladie, provenant de différentes régions de l’Inde. À partir d’enquêtes génétiques larges antérieures, ils ont sélectionné 63 petites variations d’ADN, appelées polymorphismes mononucléotidiques, dans des gènes suspectés d’affecter la réponse immunitaire. Ils ont d’abord vérifié lesquelles de ces variations sont présentes à des fréquences utiles chez des personnes d’ascendance indienne. Après cette étape de filtrage, 51 sites génétiques dans la région HLA principale et dans de nombreux gènes non-HLA ont été testés pour comparer la fréquence de chaque version chez les malades et chez les témoins sains.
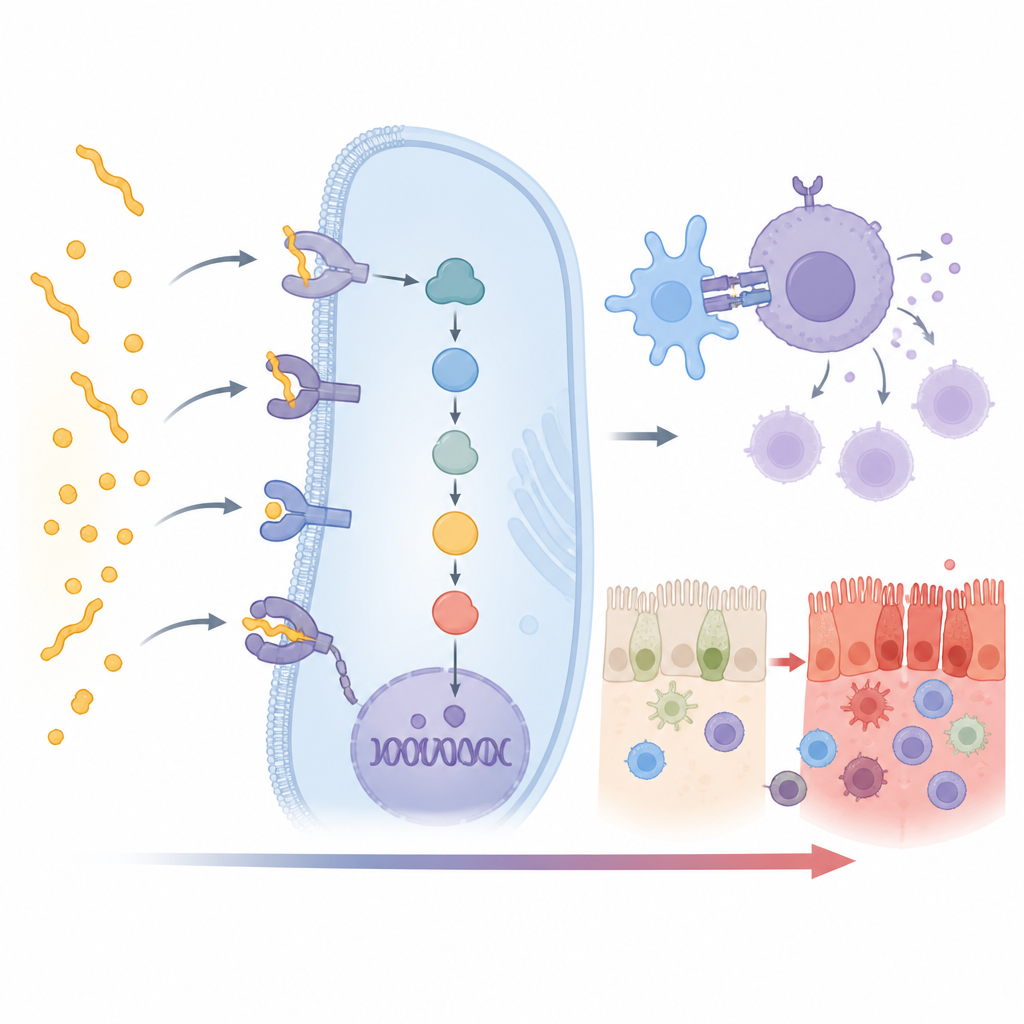
Aides cachées dans la réponse immunitaire
Comme prévu, le signal le plus fort provenait de la forme HLA DQ2.5, avec des liens plus faibles mais nettement présents pour DQ2.2 et DQ8. Plus intrigant, 15 gènes non-HLA supplémentaires ont aussi montré une association marquée avec la maladie cœliaque dans ce groupe indien. Beaucoup se situent directement dans la chaîne d’événements qui transforme la reconnaissance du gluten en une attaque immunitaire à part entière. Certains gènes, tels que CD247, CD28, CD80 et PRKCQ, contribuent à l’activation des lymphocytes T, les globules blancs qui conduisent la maladie. D’autres, comme UBASH3A et TNFAIP3, jouent le rôle de freins qui empêchent normalement cette activation de déraper. Des variations dans ces gènes peuvent faire pencher la balance vers des réactions immunitaires plus fortes ou plus faibles.
Protéger la muqueuse et guider les cellules immunitaires
Plusieurs des gènes associés influencent la santé de la muqueuse intestinale elle-même ou le mouvement des cellules immunitaires. CCR3 et CCR4 aident à guider les cellules immunitaires et inflammatoires dans les tissus, pouvant orienter davantage de ces cellules vers l’intestin grêle où le gluten est présent. GATD3 et PARK7 sont liés à la façon dont les mitochondries gèrent le stress et peuvent aider les cellules intestinales à faire face aux dommages causés par l’inflammation et les espèces réactives de l’oxygène. INAVA soutient les jonctions serrées qui maintiennent l’étanchéité de la barrière intestinale, tandis que DDX6, PUS10 et un ARN non codant long appelé LINC01934 influencent le traitement de l’ARN et la régulation de l’expression génique. Ensemble, ces variations décrivent une chaîne qui va du contact avec le gluten, via la signalisation immunitaire, jusqu’à la lésion de la surface intestinale.
Assembler le réseau génétique
En analysant comment les différentes variations d’ADN interagissent entre elles, les chercheurs ont trouvé un réseau de sites étroitement lié plutôt que de nombreux effets isolés. Certaines variantes ont émergé comme des nœuds centraux, montrant de nombreuses connexions statistiques avec d’autres. Lorsque l’équipe a cartographié les gènes correspondants, des rôles de nœud ont été occupés par des gènes clés du système immunitaire et de la signalisation, y compris plusieurs gènes HLA de classe II, des récepteurs de chimiokines qui contrôlent la migration cellulaire, et des molécules d’activation des lymphocytes T. Ce schéma de réseau soutient l’idée que de nombreuses petites pressions génétiques le long d’une même voie se combinent pour déterminer si l’exposition au gluten fait basculer une personne vers la maladie.
Que cela signifie pour les personnes à risque
Pour les lecteurs, le principal enseignement est que le risque de maladie cœliaque en Inde n’est pas déterminé par un seul gène mais par un ensemble de gènes qui communiquent entre eux dans les cellules immunitaires et la muqueuse intestinale. Les types de risque HLA classiques restent essentiels, mais des différences héréditaires supplémentaires—dans la manière dont les lymphocytes T sont activés, dont les signaux sont atténués, dont les cellules immunitaires se déplacent, et dont la paroi intestinale reste cohésive—s’ajoutent au résultat final. À mesure que ces voies seront mieux comprises, elles pourraient aider à affiner des scores de risque génétique pour les personnes déjà porteuses de types HLA à haut risque et, éventuellement, indiquer de nouvelles façons d’apaiser la réponse immunitaire au gluten sans se reposer uniquement sur des changements diététiques stricts et à vie.
Citation: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Mots-clés: maladie cœliaque, gluten, gènes HLA-DQ, activation des lymphocytes T, risque génétique