Clear Sky Science · ru
Ассоциации полиморфизмов генов, не относящихся к HLA, с целиакией в Индии
Почему это важно для повседневного питания
Целиакия превращает обычный продукт питания — пшеницу — в триггер хронического повреждения кишечника. В этом исследовании поставлен простой, но существенный вопрос: помимо наиболее известных генов риска, какие другие наследственные признаки помогают определить, кто в Индии заболевает от употребления глютена, а кто остаётся здоровым, даже если обе группы несут похожие основные генетические риски?
Ближе к глютену и кишечнику
Целиакия — это иммунное заболевание, при котором употребление глютена, белка, содержащегося в пшенице, ячмене и ржи, повреждает тонкую кишку. Заболеваемость около 1% наблюдается в Европе, Северной Америке и регионах Индии с потреблением пшеницы. Основной известный генетический риск связан с семейством генов иммунной системы HLA‑DQ, которые помогают иммунным клеткам распознавать фрагменты глютена. Люди с определёнными вариантами, особенно DQ2.5, DQ2.2 и DQ8, существенно более склонны к развитию болезни. Вместе с тем многие носители этих вариантов так и не заболевают, что указывает на роль других наследственных факторов.
Что пытались выяснить исследователи
Команда изучила 376 взрослых с целиакией и 736 взрослых без заболевания из разных регионов Индии. Из предыдущих крупных генетических исследований они выбрали 63 небольших изменения в ДНК, известных как одиночные нуклеотидные полиморфизмы, в генах, предположительно влияющих на иммунный ответ. Сначала проверяли, какие из этих изменений вообще встречаются в популяции индийского происхождения на достаточных уровнях. После этого этапа скрининга для тестирования частот в пациентах и в контрольной группе были оставлены 51 генетический сайт в основной HLA‑области и во множестве не‑HLA генов.
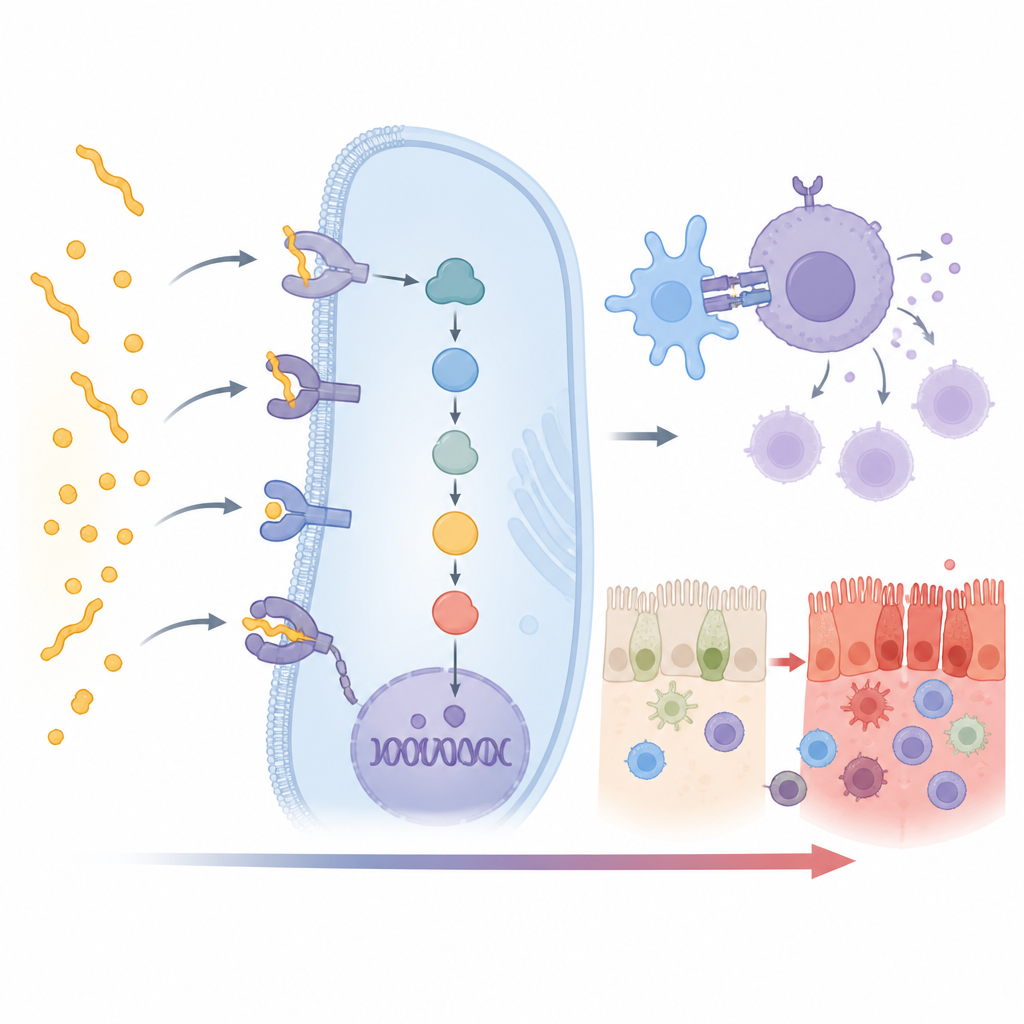
Скрытые участники иммунного ответа
Как и ожидалось, самый сильный сигнал шёл от варианта HLA DQ2.5, с более слабыми, но заметными связями для DQ2.2 и DQ8. Более любопытно, что ещё 15 не‑HLA генов продемонстрировали значимую связь с целиакией в этой индийской выборке. Многие из них вовлечены непосредственно в цепочку событий, переводящих распознавание глютена в полноценную иммунную атаку. Некоторые гены, такие как CD247, CD28, CD80 и PRKCQ, помогают включать T‑клетки — белые кровяные клетки, драйверы болезни. Другие, например UBASH3A и TNFAIP3, действуют как тормоза, которые обычно сдерживают чрезмерную активацию. Изменения в этих генах могут смещать баланс в сторону усиленного или ослабленного иммунного ответа.
Защита слизистой и направление движения иммунных клеток
Несколько ассоциированных генов влияют на здоровье самой кишечной оболочки или на миграцию иммунных клеток. CCR3 и CCR4 помогают направлять иммунные и воспалительные клетки в ткани, потенциально увеличивая приток таких клеток в тонкую кишку, где присутствует глютен. GATD3 и PARK7 связаны с тем, как митохондрии справляются со стрессом, и могут помогать клеткам кишечника выдерживать повреждение, вызванное воспалением и реактивными формами кислорода. INAVA поддерживает плотные контакты, которые удерживают барьер кишечника, в то время как DDX6, PUS10 и длинная некодирующая РНК LINC01934 влияют на обработку РНК и регуляцию генов. В совокупности эти изменения очерчивают цепочку от контакта с глютеном, через иммунную сигнализацию, к повреждению поверхности кишечника.
Сборка генетической сети
Анализируя взаимодействия разных изменений ДНК, исследователи обнаружили не множество разрозненных эффектов, а тесно связанную сеть сайтов. Отдельные варианты проявили себя как узлы с многочисленными статистическими связями с другими. При сопоставлении с соответствующими генами роли узлов заняли ключевые иммунные и сигнальные гены, включая несколько генов HLA класса II, хемокиновые рецепторы, контролирующие миграцию клеток, и молекулы активации T‑клеток. Такая сетевая картина подтверждает идею, что множество небольших генетических «толчков» вдоль одного пути суммируются и определяют, приведёт ли контакт с глютеном к болезни.
Что это значит для людей с повышенным риском
Главный вывод для читателей: риск целиакии в Индии определяется не одним геном, а кластером генов, взаимодействующих друг с другом в иммунных клетках и в слизистой кишечника. Классические типы риска HLA остаются ключевыми, но дополнительные наследственные различия в том, как включаются T‑клетки, как тормозятся сигналы, как перемещаются иммунные клетки и как удерживается целостность кишечной стенки — всё это вносит вклад в итоговый результат. По мере того как эти пути будут лучше изучены, они могут помочь уточнить генетические шкалы риска для людей, уже несущих высокорисковые HLA‑типы, и в перспективе указать на новые способы смирения иммунного ответа на глютен без опоры исключительно на строгую пожизненную диету.
Цитирование: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Ключевые слова: целиакия, глютен, гены HLA‑DQ, активация T‑клеток, генетический риск