Clear Sky Science · it
Associazioni di polimorfismi genici non-HLA con la malattia celiaca in India
Perché questo conta per le diete quotidiane
La malattia celiaca trasforma un alimento comune, il frumento, in un fattore scatenante di danno cronico all’intestino. Questo studio pone una domanda semplice ma importante: oltre ai geni di rischio più noti, quali altri caratteri ereditari contribuiscono a decidere chi in India si ammala mangiando glutine e chi resta sano, anche quando entrambi i gruppi portano versioni simili dei geni di rischio principali?
Uno sguardo più ravvicinato al glutine e all’intestino
La malattia celiaca è una condizione immunitaria in cui l’assunzione di glutine, una proteina presente in frumento, orzo e segale, danneggia l’intestino tenue. Colpisce circa l’1 percento delle persone in Europa, Nord America e nelle regioni indiane dove si consuma frumento. Il principale rischio genetico noto risiede in una famiglia di geni del sistema immunitario chiamata HLA DQ, che aiutano le cellule immunitarie a riconoscere frammenti di glutine. Le persone che portano certe varianti, specialmente quelle nominate DQ2.5, DQ2.2 e DQ8, hanno una probabilità molto più alta di sviluppare la malattia. Tuttavia molte persone con questi geni non si ammalano mai, il che suggerisce che anche altri fattori ereditari modulano il rischio.
Cosa hanno cercato i ricercatori
Il gruppo ha studiato 376 adulti con malattia celiaca e 736 adulti senza la malattia provenienti da diverse aree dell’India. Da indagini genetiche maggiori precedenti hanno selezionato 63 piccole variazioni del DNA, note come polimorfismi a singolo nucleotide, in geni sospettati di influenzare la risposta immunitaria. Per prima cosa hanno verificato quali di queste variazioni sono presenti a livelli utili nella popolazione di origine indiana. Dopo questa fase di screening, 51 siti genetici sia nella regione HLA principale sia in diversi geni non-HLA sono stati testati per confrontare la frequenza di ciascuna versione nei pazienti rispetto ai controlli sani.
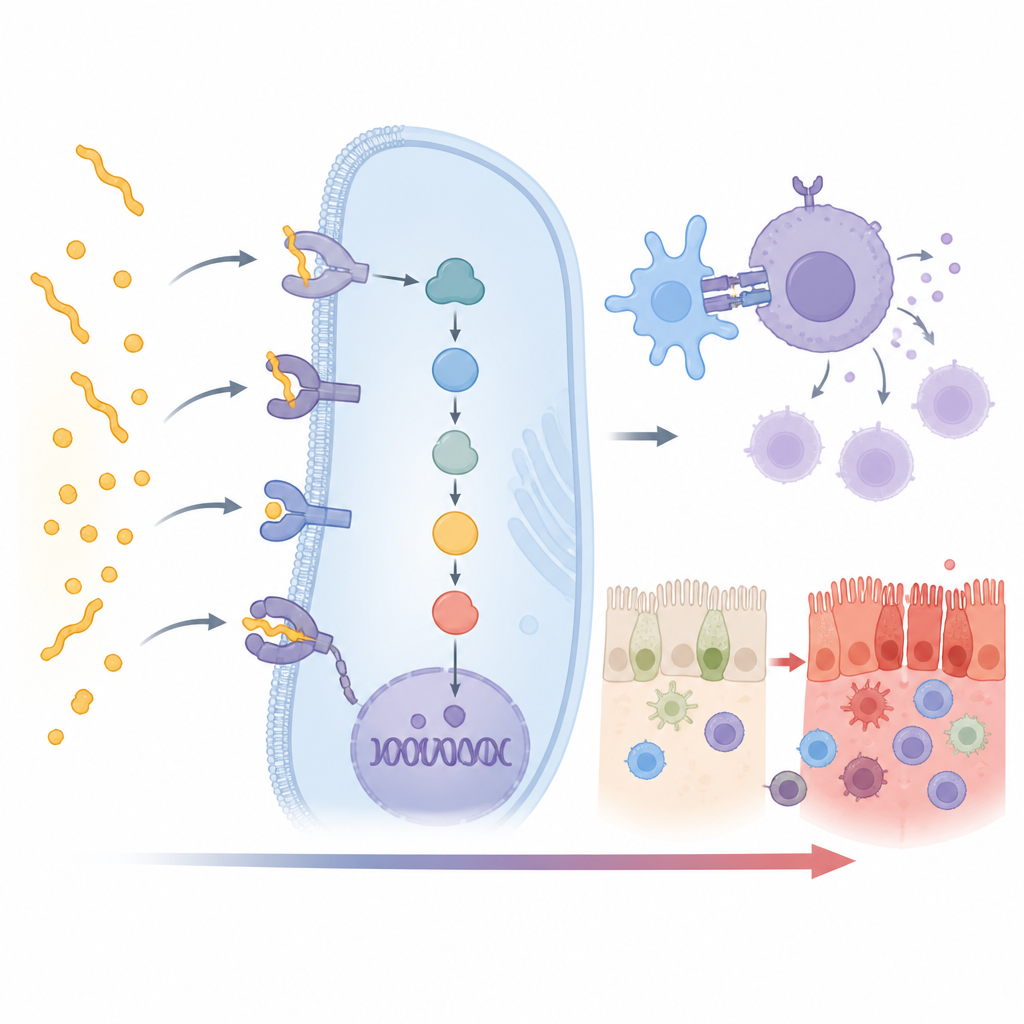
Alleati nascosti nella risposta immunitaria
Come previsto, il segnale più forte è venuto dalla forma HLA DQ2.5, con legami più deboli ma comunque chiari per DQ2.2 e DQ8. Più intrigante, 15 geni non-HLA aggiuntivi hanno mostrato un forte collegamento con la malattia celiaca in questo gruppo indiano. Molti si collocano direttamente nella catena di eventi che trasforma il riconoscimento del glutine in un attacco immunitario conclamato. Alcuni geni, come CD247, CD28, CD80 e PRKCQ, contribuiscono all’attivazione dei linfociti T, i globuli bianchi che guidano la malattia. Altri, come UBASH3A e TNFAIP3, fungono da freni che normalmente impediscono a questa attivazione di sfuggire al controllo. Variazioni in questi geni possono spostare l’equilibrio verso reazioni immunitarie più forti o più deboli.
Proteggere la mucosa intestinale e indirizzare le cellule immunitarie
Diversi dei geni associati influenzano la salute stessa dell’epitelio intestinale o il movimento delle cellule immunitarie. CCR3 e CCR4 aiutano a dirigere cellule immunitarie e infiammatorie nei tessuti, potenzialmente convogliando più cellule verso l’intestino tenue dove è presente il glutine. GATD3 e PARK7 sono collegati al modo in cui i mitocondri gestiscono lo stress e possono aiutare le cellule intestinali a far fronte al danno causato dall’infiammazione e dalle specie reattive dell’ossigeno. INAVA sostiene le giunzioni strette che mantengono sigillata la barriera intestinale, mentre DDX6, PUS10 e un lungo RNA non codificante chiamato LINC01934 influenzano come l’RNA viene processato e come i geni vengono accesi o spenti. Nel loro insieme, queste variazioni delineano una catena che va dal contatto con il glutine, attraverso la segnalazione immunitaria, fino al danno della superficie intestinale.
Ricostruire la rete genetica
Analizzando come le diverse variazioni del DNA interagiscono tra loro, i ricercatori hanno trovato una rete di siti strettamente collegati piuttosto che molti effetti isolati. Alcune varianti sono emerse come nodi centrali, mostrando molte connessioni statistiche con altre. Quando il team ha mappato i geni corrispondenti, i ruoli di nodo centrale erano presi da geni chiave dell’immunità e della segnalazione, inclusi vari geni della classe II HLA, recettori chemiotattici che controllano la migrazione cellulare e molecole di attivazione dei linfociti T. Questo schema di rete sostiene l’idea che molti piccoli scossoni genetici lungo la stessa via si combinino per determinare se l’esposizione al glutine spinge una persona verso la malattia.
Cosa significa per le persone a rischio
Per il lettore, la conclusione principale è che il rischio di malattia celiaca in India non è fissato da un singolo gene ma da un gruppo di geni che comunicano tra loro nelle cellule immunitarie e nell’epitelio intestinale. I tipi di rischio HLA classici restano essenziali, ma differenze ereditarie aggiuntive su come i linfociti T vengono attivati, come i segnali vengono attenuati, come le cellule immunitarie si muovono e come la parete intestinale resta integra contribuiscono tutte al risultato finale. Man mano che queste vie saranno meglio comprese, potranno aiutare a perfezionare punteggi di rischio genetico per chi già porta i tipi HLA ad alto rischio e, in futuro, indicare nuove strategie per modulare la risposta immunitaria al glutine senza fare affidamento esclusivo su diete rigorose e permanenti.
Citazione: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Parole chiave: malattia celiaca, glutine, geni HLA-DQ, attivazione dei linfociti T, rischio genetico