Clear Sky Science · nl
Associaties van non-HLA genpolymorfismen met coeliakie in India
Waarom dit belangrijk is voor dagelijkse voeding
Coeliakie verandert een alledaags voedingsmiddel, tarwe, in een prikkel voor chronische darmbeschadiging. Deze studie stelt een eenvoudige maar belangrijke vraag: naast de bekendste risicogenen, welke andere erfelijke kenmerken helpen bepalen wie in India ziek wordt van het eten van gluten en wie gezond blijft, zelfs wanneer beide groepen vergelijkbare hoofdrisicogenen dragen?
Een nadere blik op gluten en de darm
Coeliakie is een immuunaandoening waarbij het eten van gluten, een eiwit in tarwe, gerst en rogge, de dunne darm beschadigt. Het treft ongeveer 1 procent van de mensen in Europa, Noord-Amerika en tarweetende regio's van India. Het belangrijkste bekende genetische risico ligt bij een familie van immuunsysteemgenen die HLA DQ heet, die immuuncellen helpen fragmenten van gluten te herkennen. Mensen die bepaalde vormen dragen, vooral DQ2.5, DQ2.2 en DQ8, lopen veel meer kans de ziekte te ontwikkelen. Toch worden veel mensen met deze genen nooit ziek, wat suggereert dat ook andere erfelijke factoren het risico beïnvloeden.
Wat de onderzoekers wilden vinden
Het team onderzocht 376 volwassenen met coeliakie en 736 volwassenen zonder de ziekte uit verschillende delen van India. Op basis van eerdere grote genetische onderzoeken kozen ze 63 kleine DNA-veranderingen, bekend als single nucleotide polymorfismen, in genen die vermoedelijk de immuunrespons beïnvloeden. Eerst controleerden ze welke van deze veranderingen überhaupt in nuttige frequenties aanwezig zijn bij mensen van Indiase afkomst. Na deze screeningsstap werden 51 genetische locaties in zowel de hoofd-HLA-regio als in veel non-HLA-genen getest op hoe vaak elke variant voorkwam bij patiënten vergeleken met gezonde controles.
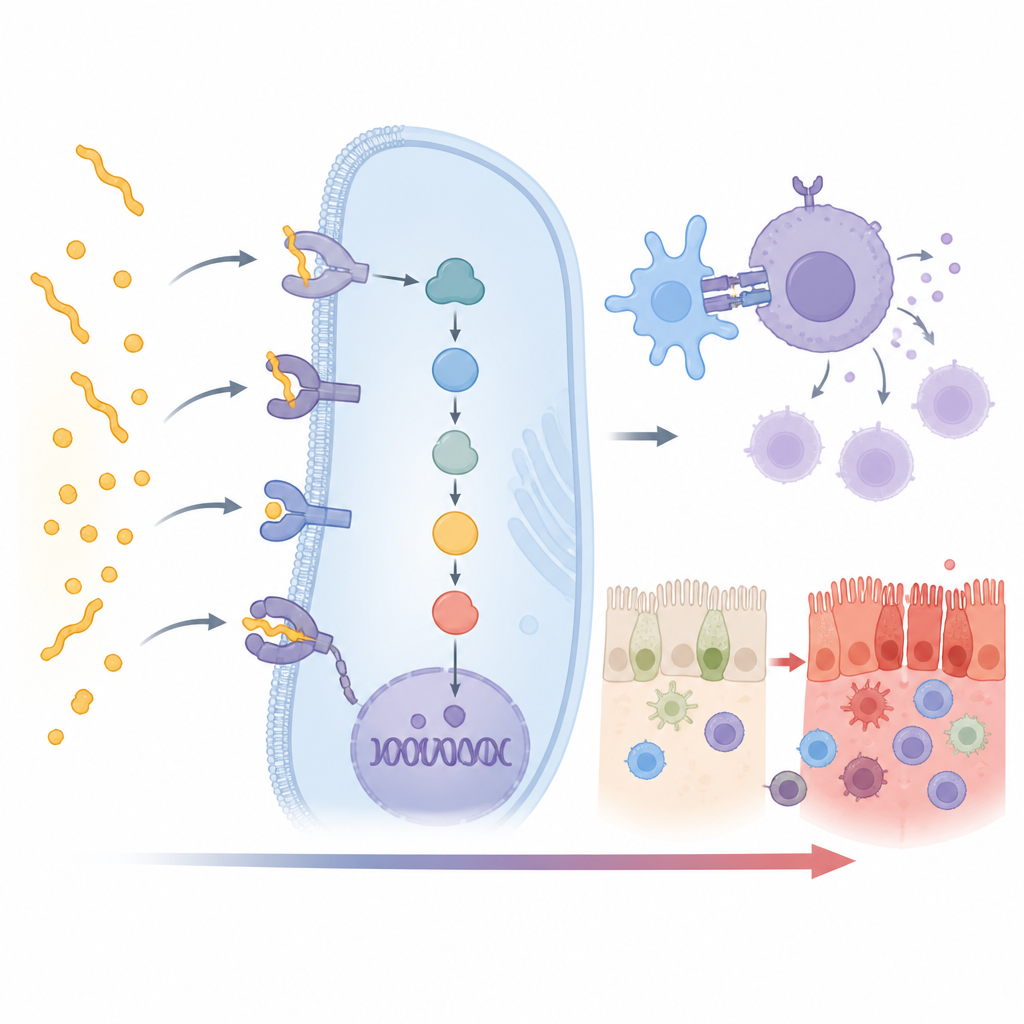
Verborgen helpers in de immuunrespons
Zoals verwacht kwam het sterkste signaal van de HLA DQ2.5-vorm, met zwakkere maar duidelijke verbanden met DQ2.2 en DQ8. Intrigerender was dat 15 aanvullende non-HLA-genen ook een sterk verband lieten zien met coeliakie in deze Indiase groep. Veel van deze genen bevinden zich direct in de keten van gebeurtenissen die glutenherkenning omzet in een volledige immuunaanval. Sommige genen, zoals CD247, CD28, CD80 en PRKCQ, helpen T-cellen te activeren, de witte bloedcellen die de ziekte aandrijven. Andere, zoals UBASH3A en TNFAIP3, fungeren als remmen die normaal voorkomen dat deze activatie uit de hand loopt. Veranderingen in deze genen kunnen het evenwicht doen doorslaan naar sterkere of zwakkere immuunreacties.
Bescherming van de darmwand en het sturen van immuuncellen
Verschillende van de geassocieerde genen beïnvloeden de gezondheid van de darmwand zelf of de beweging van immuuncellen. CCR3 en CCR4 helpen immuun- en ontstekingscellen naar weefsels te leiden, waarbij mogelijk meer van zulke cellen richting de dunne darm worden gestuurd waar gluten aanwezig is. GATD3 en PARK7 worden gekoppeld aan hoe mitochondriën omgaan met stress en kunnen darmcellen helpen schade door ontsteking en reactieve zuurstofsoorten te weerstaan. INAVA ondersteunt de tight junctions die de intestinale barrière gesloten houden, terwijl DDX6, PUS10 en een lange niet-coderende RNA genaamd LINC01934 invloed hebben op hoe RNA wordt verwerkt en hoe genen aan- en uitgezet worden. Samen tekenen deze veranderingen een keten uit die loopt van contact met gluten, via immuunsignalen, naar letsel van het darmslijmvlies.
Het samenvoegen van het genetische netwerk
Door te analyseren hoe de verschillende DNA-veranderingen met elkaar interageren, vonden de onderzoekers een sterk verbonden netwerk van loci in plaats van veel geïsoleerde effecten. Bepaalde varianten traden op als knooppunten en toonden veel statistische verbindingen met andere varianten. Toen het team de overeenkomstige genen in kaart bracht, namen sleutelimmuun- en signaalgenen knooppuntrollen in, waaronder meerdere HLA klasse II-genen, chemokine-receptoren die celmigratie sturen, en moleculen voor T-cel activatie. Dit netwerkpatroon ondersteunt de opvatting dat veel kleine genetische verschuivingen langs dezelfde route samen bepalen of glutenblootstelling iemand naar ziekte doet doorslaan.
Wat dit betekent voor mensen met risico
De belangrijkste conclusie voor lezers is dat het risico op coeliakie in India niet door één gen wordt bepaald, maar door een cluster van genen die met elkaar communiceren in immuuncellen en in de darmwand. De klassieke HLA-riscotypes blijven essentieel, maar aanvullende erfelijke verschillen in hoe T-cellen worden aangeschakeld, hoe signalen worden gedempt, hoe immuuncellen zich verplaatsen en hoe de darmwand intact blijft, dragen allemaal bij aan de uiteindelijke uitkomst. Naarmate deze paden beter worden begrepen, kunnen ze helpen om genetische risicoscores voor mensen die al hoge-risico HLA-typen dragen te verfijnen en mogelijk uiteindelijk wijzen op nieuwe manieren om de immuunreactie op gluten te kalmeren zonder uitsluitend te steunen op strikte levenslange dieetveranderingen.
Bronvermelding: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Trefwoorden: coeliakie, gluten, HLA-DQ genen, T-cel activatie, genetisch risico