Clear Sky Science · ja
インドにおけるセリアック病と非HLA遺伝子多型の関連
日常の食事にとってなぜ重要か
セリアック病は、身近な食材である小麦を慢性的な腸の損傷の引き金に変えてしまう病気だ。本研究は単純だが重要な問いを投げかける:最もよく知られたリスク遺伝子に加えて、同じ主要リスク遺伝子を持つ人のうち誰がグルテンで病気になるか、誰が健康を保てるかを左右する他の遺伝的要因は何か、という点である。
グルテンと腸を詳しく見る
セリアック病は、小麦、大麦、ライ麦に含まれるタンパク質であるグルテンを摂取することで小腸が損なわれる免疫疾患である。ヨーロッパ、北米、そして小麦を多く食べるインドの地域ではおよそ1%の人が罹患している。既知の主要な遺伝的リスクはHLA‑DQと呼ばれる免疫系遺伝子群にあり、これらは免疫細胞がグルテン断片を認識するのを助ける。特にDQ2.5、DQ2.2、DQ8と呼ばれる型を持つ人は病気を発症する確率が高い。しかしこれらの型を持つ多くの人は発症しないことから、他の遺伝的要因もリスクを形作っていることが示唆される。
研究者が明らかにしようとしたこと
研究チームはインド各地のセリアック病の成人376人と疾病のない成人736人を対象に調べた。以前の大規模遺伝調査に基づき、免疫応答に影響すると考えられる63個の一塩基多型(SNP)を候補として選んだ。まずインド人集団で実用的な頻度で存在するかを確認するスクリーニングを行い、その結果を踏まえて、主要なHLA領域と多数の非HLA遺伝子を含む51の遺伝座について、患者と健常対照で各対立遺伝子がどの程度出現するかを比較した。
免疫応答における隠れた助け手
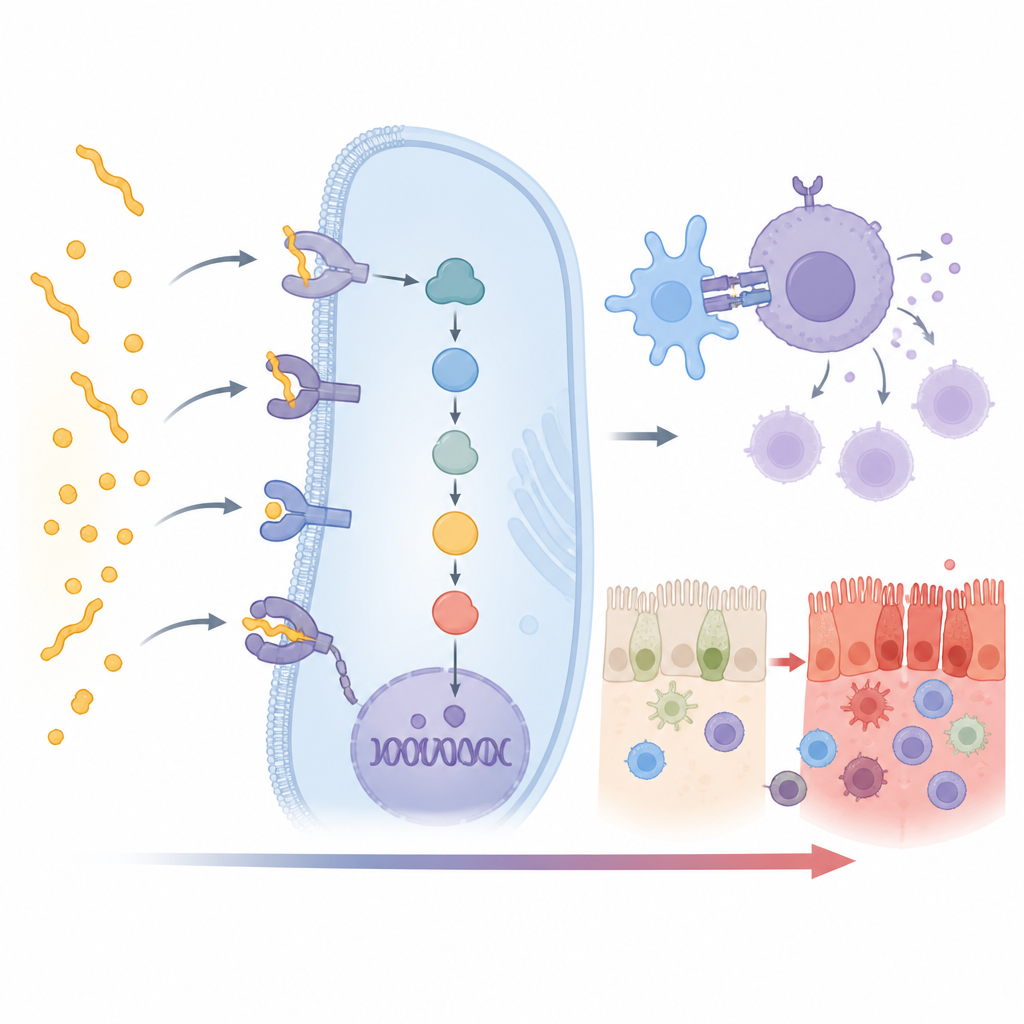
想定どおり最も強い信号はHLA DQ2.5型から得られ、DQ2.2やDQ8も弱めだが明確な関連を示した。より興味深いことに、15の非HLA遺伝子もこのインド集団でセリアック病と強く関連していた。多くはグルテンの認識を完全な免疫攻撃に変換する一連の過程に直接関与する。たとえばCD247、CD28、CD80、PRKCQといった遺伝子は、病気を駆動するT細胞のスイッチを入れる働きを助ける。他方でUBASH3AやTNFAIP3のような遺伝子は通常その活性化が暴走しないようにブレーキを掛ける。これら遺伝子の変化は免疫反応をより強く、またはより弱く傾ける可能性がある。
腸粘膜の保護と免疫細胞の誘導
関連する遺伝子のうちいくつかは腸の上皮そのものの健康や免疫細胞の移動に影響を与える。CCR3やCCR4は免疫・炎症細胞を組織へと誘導する役割があり、小腸により多くのこうした細胞を引き寄せることでグルテンの存在する場所に炎症を集中させる可能性がある。GATD3やPARK7はミトコンドリアのストレス処理に関連し、炎症や活性酸素による損傷に腸細胞が対処するのを助けるかもしれない。INAVAは腸の密着結合を支持してバリアを保つ役割を持ち、DDX6、PUS10、長鎖ノンコーディングRNAのLINC01934はRNA処理や遺伝子のオン/オフ制御に影響を与える。これらが連携して、グルテン接触から免疫シグナルを経て腸表面の傷害へと至る一連の流れを描き出す。
遺伝子ネットワークの組み立て
研究者らは異なるDNA変異が互いにどのように相互作用するかを解析することで、多くの孤立した効果というよりは緊密に結びついた部位のネットワークを見いだした。特定の変異がハブとして浮かび上がり、他の多くの変異と統計的に多くの結びつきを示した。これらのハブに対応する遺伝子をマッピングすると、主要なHLAクラスII遺伝子、細胞移動を制御するケモカイン受容体、T細胞活性化分子などの重要な免疫・シグナル伝達遺伝子が中心的役割を担っていた。このネットワーク様式は、多数の小さな遺伝的要素が同じ経路上で合わさって、グルテン曝露が個人を病気に傾けるかどうかを決めるという見方を支持する。
リスクのある人々にとっての意味
読者が得るべき主な結論は、インドにおけるセリアック病のリスクは単一の遺伝子で決まるものではなく、免疫細胞と腸粘膜内で互いに作用する遺伝子群によって形成されているという点だ。古典的なHLAリスク型は依然として重要だが、T細胞がどのようにオンになるか、シグナルがどのように抑えられるか、免疫細胞がどのように動くか、腸壁がどのように保たれるかといった追加の遺伝的差異が最終的な結果に寄与する。これらの経路がよりよく理解されれば、高リスクHLA型を既に持つ人々の遺伝リスクスコアを洗練する手助けになりうるし、厳格な生涯にわたる食事制限に頼らずにグルテンへの免疫応答を和らげる新たな手段を示す可能性もある。
引用: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
キーワード: セリアック病, グルテン, HLA‑DQ遺伝子, T細胞活性化, 遺伝的リスク