Clear Sky Science · ar
ارتباط تعدد أشكال الجينات غير المرتبطة بـ HLA بمرض السيلياك في الهند
لماذا هذا مهم في النظام الغذائي اليومي
يجعل مرض السيلياك من الغذاء الشائع، القمح، عاملاً مهيِّجاً لتلف مزمن في الأمعاء. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهم: بعيداً عن جينات الخطر المعروفة جيداً، ما الصفات الوراثية الأخرى التي تساعد في تقرير من في الهند يمرض من أكل الغلوتين ومن يبقى صحياً، حتى عندما يحمل كلا المجموعتين نفس جينات الخطر الرئيسية؟
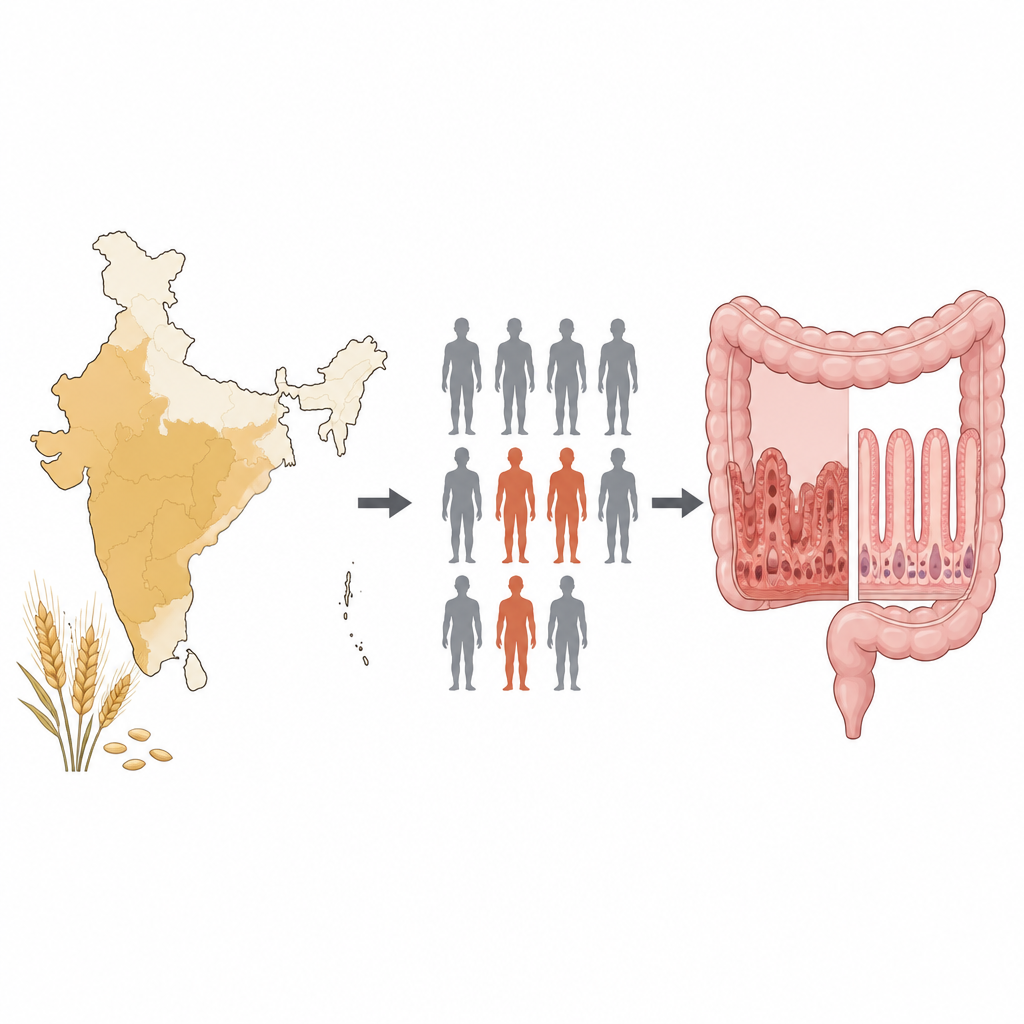
نظرة أقرب على الغلوتين والأمعاء
مرض السيلياك هو حالة مناعية يسبب فيها أكل الغلوتين—بروتين موجود في القمح والشعير ونخيل—تلفاً في الأمعاء الدقيقة. يصيب نحو 1 في المئة من الناس في أوروبا وأمريكا الشمالية ومناطق الهند التي تتناول القمح. الخطر الوراثي المعروف الرئيسي يكمن في عائلة من جينات الجهاز المناعي تُسمى HLA-DQ، التي تساعد الخلايا المناعية على تمييز أجزاء من الغلوتين. الأشخاص الذين يحملون أشكالاً معينة، خاصةً DQ2.5 وDQ2.2 وDQ8، هم أكثر عرضة بكثير لتطور المرض. ومع ذلك، يظل العديد من حاملين هذه الجينات دون مرض، ما يشير إلى أن عوامل وراثية أخرى تُشكّل الخطر أيضاً.
ما الذي سعى الباحثون لاكتشافه
درَس الفريق 376 بالغاً مصابين بمرض السيلياك و736 بالغاً غير مصابين من مناطق مختلفة في الهند. ومن دراسات جينية كبيرة سابقة، اختاروا 63 تغييراً صغيراً في الحمض النووي، تُعرف بالمتغايرات أحادية النوكليوتيد، في جينات يُشتبه في أنها تؤثر في الاستجابة المناعية. أولاً تحققوا أي من هذه التغيرات موجودة بمعدلات مفيدة في الأشخاص من أصل هندي. بعد خطوة الفرز هذه، اختُبرت 51 موضعاً وراثياً في كل من المنطقة الرئيسية لـ HLA والعديد من الجينات غير المرتبطة بـ HLA لمعرفة تكرار كل نسخة في المرضى مقارنة بالمجموعات الضابطة السليمة.
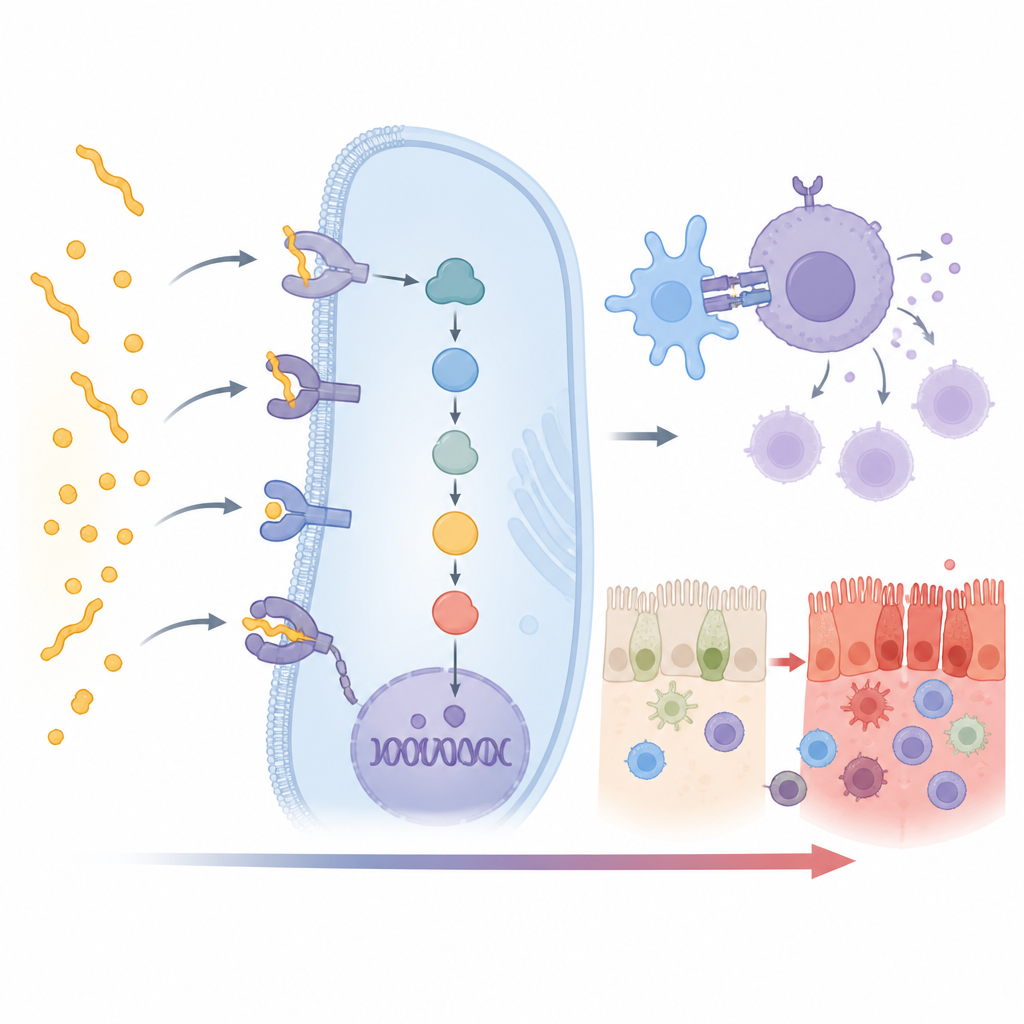
مساعدون خفيون في الاستجابة المناعية
كما كان متوقعاً، جاءت الإشارة الأقوى من شكل HLA DQ2.5، مع روابط أضعف لكنها واضحة أيضاً لـ DQ2.2 وDQ8. والأكثر إثارة للاهتمام أن 15 جيناً إضافياً خارج منطقة HLA أظهرت أيضاً ارتباطاً قوياً بمرض السيلياك في هذه العينة الهندية. كثير منها يقع مباشرة في سلسلة الأحداث التي تحول تمييز الغلوتين إلى هجوم مناعي كامل. بعض الجينات، مثل CD247 وCD28 وCD80 وPRKCQ، تساعد على تشغيل الخلايا التائية، وهي خلايا الدم البيضاء التي تقود المرض. أخرى، مثل UBASH3A وTNFAIP3، تعمل كفرامل تُبقي هذا التنشيط تحت السيطرة عادةً. قد تميل التغيرات في هذه الجينات بالتالي بالكفة نحو ردود مناعية أقوى أو أضعف.
حماية بطانة الأمعاء وتوجيه الخلايا المناعية
العديد من الجينات المرتبطة تؤثر في صحة بطانة الأمعاء نفسها أو في حركة الخلايا المناعية. تساعد CCR3 وCCR4 في توجيه الخلايا المناعية والالتهابية إلى الأنسجة، مما قد يزيد من توجّه هذه الخلايا إلى الأمعاء الدقيقة حيث يتواجد الغلوتين. ترتبط GATD3 وPARK7 بكيفية تعامل الميتوكوندريا مع الإجهاد وقد تساعد خلايا الأمعاء على مواجهة الضرر الناتج عن الالتهاب والأكسدة التفاعلية. يدعم INAVA الوصلات الضيقة التي تحافظ على ختم الحاجز المعوي، بينما يؤثر DDX6 وPUS10 وRNA طويل غير مرمَّز يدعى LINC01934 في كيفية معالجة الـ RNA وكيف تُشغَّل الجينات أو تُسكَّت. معاً، تحدد هذه التغيرات سلسلة تبدأ من ملامسة الغلوتين، عبر الإشارات المناعية، وصولاً إلى إصابة سطح الأمعاء.
تركيب الشبكة الوراثية
من خلال تحليل كيفية تداخل التغيرات في الحمض النووي مع بعضها، وجد الباحثون شبكة مترابطة بإحكام من المواضع بدلاً من تأثيرات معزولة كثيرة. برزت متغيرات معينة كنقاط مركزية، أظهرت اتصالات إحصائية عديدة مع غيرها. وعندما رسم الفريق خريطة الجينات المقابلة، اتخذت أدوار المحاور جينات مناعية وإشارية رئيسية، بما في ذلك عدة جينات HLA من الفئة II، ومستقبلات الكموكائن التي تتحكم في هجرة الخلايا، وجزيئات تنشيط الخلايا التائية. يدعم نمط الشبكة هذا الفكرة القائلة إن العديد من التعديلات الوراثية الصغيرة على طول نفس المسار تتضافر لتحدد ما إذا كان التعرض للغلوتين سيدفع الشخص نحو المرض.
ماذا يعني هذا للأشخاص المعرضين للخطر
الخلاصة للقارئ هي أن خطر مرض السيلياك في الهند لا تحدده جينة واحدة بل مجموعة من الجينات التي تتواصل مع بعضها في الخلايا المناعية وفي بطانة الأمعاء. تظل أنواع HLA الكلاسيكية ذات أهمية، لكن اختلافات وراثية إضافية تحدد كيفية تشغيل الخلايا التائية، وكيف تُكَبَّت الإشارات، وكيف تتحرك الخلايا المناعية، وكيف تبقى جدار الأمعاء متماسكاً، وكلها تسهم في النتيجة النهائية. ومع تحسن فهم هذه المسارات، قد تساعد في تحسين درجات المخاطر الجينية للأشخاص الذين يحملون أصلاً أنواع HLA عالية المخاطر وقد تشير في النهاية إلى طرق جديدة لتهدئة الاستجابة المناعية تجاه الغلوتين دون الاعتماد فقط على تغييرات غذائية صارمة مدى الحياة.
الاستشهاد: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
الكلمات المفتاحية: مرض السيلياك, الغلوتين, جينات HLA-DQ, تنشيط الخلايا التائية, الخطر الوراثي