Clear Sky Science · pl
Powiązania polimorfizmów genów nie-HLA z celiakią w Indiach
Dlaczego to ma znaczenie dla codziennej diety
Celiakia zmienia powszechny składnik diety, pszenicę, w czynnik wywołujący przewlekłe uszkodzenie jelit. W badaniu postawiono proste, ale istotne pytanie: poza najlepiej poznanymi genami ryzyka, które inne cechy dziedziczne pomagają zadecydować, kto w Indiach choruje po spożyciu glutenu, a kto pozostaje zdrowy, nawet gdy obie grupy mają podobne główne geny ryzyka?
Bliższe spojrzenie na gluten i jelito
Celiakia to choroba immunologiczna, w której spożywanie glutenu — białka obecnego w pszenicy, jęczmieniu i życie — uszkadza jelito cienkie. Choruje na nią około 1 procent populacji w Europie, Ameryce Północnej i regionach Indii, gdzie je się pszenicę. Główne znane ryzyko genetyczne leży w rodzinie genów układu odpornościowego zwanych HLA DQ, które pomagają komórkom odpornościowym rozpoznawać fragmenty glutenu. Osoby noszące określone allele, szczególnie DQ2.5, DQ2.2 i DQ8, mają znacznie większe prawdopodobieństwo rozwoju choroby. Jednak wiele osób z tymi genami nigdy nie choruje, co sugeruje, że inne czynniki dziedziczne również kształtują ryzyko.
Co badacze chcieli ustalić
Zespół przebadał 376 dorosłych z celiakią i 736 dorosłych bez choroby z różnych części Indii. Na podstawie wcześniejszych dużych badań genetycznych wybrano 63 drobne zmiany w DNA, znane jako polimorfizmy pojedynczego nukleotydu, w genach podejrzewanych o wpływ na odpowiedź immunologiczną. Najpierw sprawdzono, które z tych zmian występują na użytecznym poziomie u osób pochodzenia indyjskiego. Po tym etapie przesiewowym przetestowano 51 miejsc genetycznych zarówno w głównym regionie HLA, jak i w wielu genach nie-HLA, porównując częstość występowania poszczególnych wariantów u pacjentów i u zdrowych osób kontrolnych.
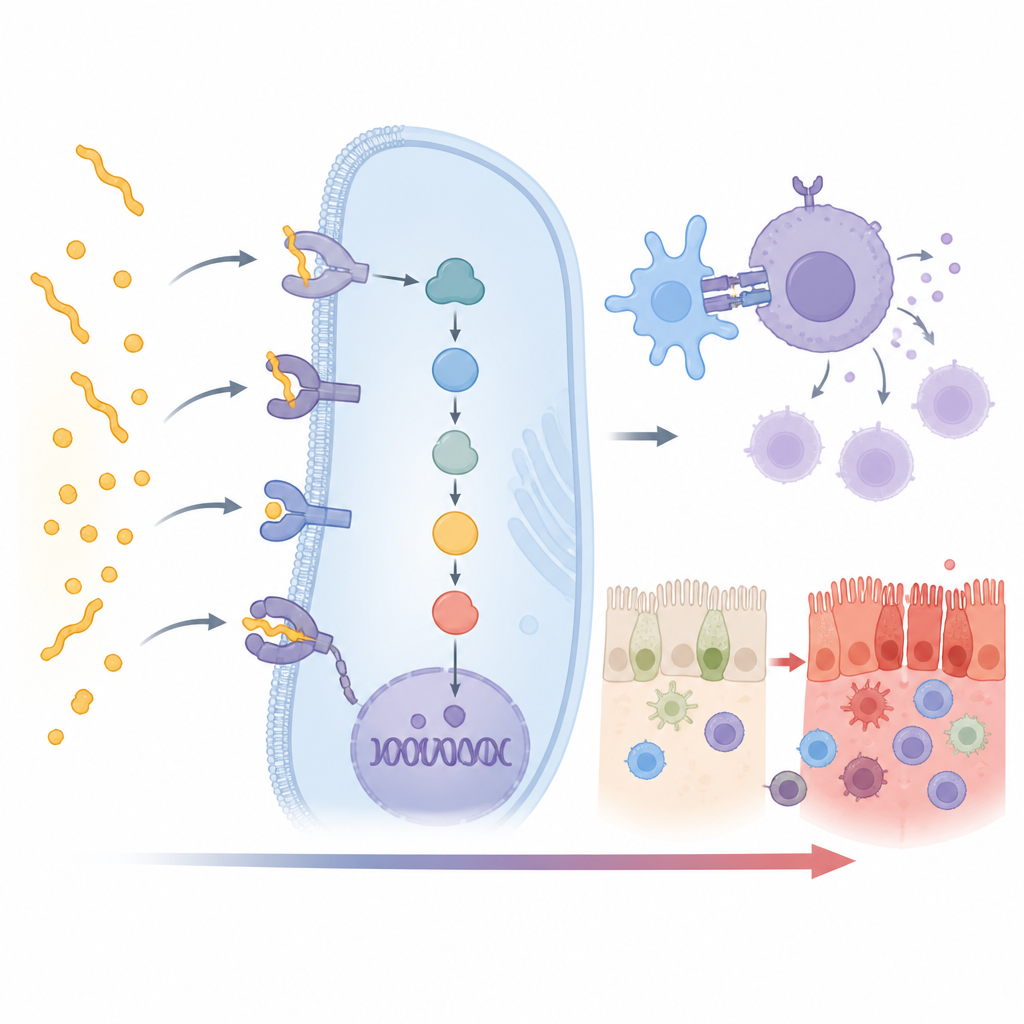
Ukryci współuczestnicy odpowiedzi immunologicznej
Jak się spodziewano, najsilniejszy sygnał pochodził od allelu HLA DQ2.5, z wyraźniejszymi, choć słabszymi powiązaniami dla DQ2.2 i DQ8. Co ciekawsze, 15 dodatkowych genów nie-HLA wykazało silne powiązanie z celiakią w tej indyjskiej grupie. Wiele z nich leży bezpośrednio w łańcuchu zdarzeń przekształcających rozpoznanie glutenu w pełnowymiarowy atak immunologiczny. Niektóre geny, takie jak CD247, CD28, CD80 i PRKCQ, pomagają w włączaniu limfocytów T — białych krwinek napędzających chorobę. Inne, jak UBASH3A i TNFAIP3, działają jako hamulce, które normalnie powstrzymują nadmierną aktywację. Zmiany w tych genach mogą przechylać równowagę w kierunku silniejszych lub słabszych reakcji immunologicznych.
Ochrona wyściółki jelita i kierowanie komórkami odpornościowymi
Kilka z powiązanych genów wpływa na zdrowie samej wyściółki jelitowej lub na ruch komórek odpornościowych. CCR3 i CCR4 pomagają kierować komórki odpornościowe i zapalne do tkanek, potencjalnie powodując napływ większej liczby takich komórek do jelita cienkiego, gdzie obecny jest gluten. GATD3 i PARK7 są związane z tym, jak mitochondria radzą sobie ze stresem i mogą pomagać komórkom jelitowym w znoszeniu uszkodzeń wywołanych zapaleniem i reaktywnymi formami tlenu. INAVA wspiera połączenia ścisłe, które utrzymują szczelność bariery jelitowej, podczas gdy DDX6, PUS10 i długa niekodująca RNA o nazwie LINC01934 wpływają na przetwarzanie RNA i regulację ekspresji genów. Razem te zmiany rysują łańcuch prowadzący od kontaktu z glutenem, przez sygnalizację immunologiczną, do uszkodzenia powierzchni jelita.
Składanie sieci genetycznej
Analizując, jak różne zmiany w DNA wchodzą w interakcje ze sobą, badacze odkryli ciasno powiązaną sieć miejsc, a nie wiele odizolowanych efektów. Pewne warianty wyróżniały się jako węzły, wykazując liczne połączenia statystyczne z innymi. Po zmapowaniu odpowiadających im genów, role węzłów przejęły kluczowe geny odpowiedzi immunologicznej i szlaków sygnalizacyjnych, w tym kilka genów klasy II HLA, receptory chemokin kontrolujące migrację komórek oraz cząsteczki aktywacji limfocytów T. Taki wzór sieci wspiera pogląd, że wiele małych genetycznych popychów wzdłuż tej samej ścieżki łączy się, by określić, czy ekspozycja na gluten przechyli osobę w stronę choroby.
Co to oznacza dla osób zagrożonych
Dla czytelników główny wniosek jest taki, że ryzyko celiakii w Indiach nie jest determinowane przez pojedynczy gen, lecz przez klaster genów, które komunikują się ze sobą w komórkach odpornościowych i w wyściółce jelitowej. Klasyczne typy ryzyka HLA nadal pozostają kluczowe, ale dodatkowe dziedziczne różnice w tym, jak włączane są limfocyty T, jak sygnały są tłumione, jak komórki odpornościowe się przemieszczają i jak trzyma się ściana jelita, wszystkie przyczyniają się do ostatecznego wyniku. W miarę lepszego poznawania tych szlaków mogą one pomóc dopracować genetyczne skale ryzyka dla osób, które już noszą wysokiego ryzyka typy HLA, i w końcu wskazać nowe sposoby łagodzenia odpowiedzi immunologicznej na gluten bez polegania wyłącznie na rygorystycznej, dożywotniej diecie.
Cytowanie: Ramakrishna, B.S., Singh, A., Srinivasan, P. et al. Associations of non-HLA gene polymorphisms with celiac disease in India. Sci Rep 16, 14918 (2026). https://doi.org/10.1038/s41598-026-45159-z
Słowa kluczowe: choroba trzewna, gluten, geny HLA-DQ, aktywacja limfocytów T, ryzyko genetyczne