Clear Sky Science · zh
PD-1 突变对帕博利珠单抗结合的影响:来自分子动力学与 MM-GBSA 分析的见解
这对癌症治疗为何重要
像帕博利珠单抗这样的免疫治疗药物已改变多种癌症的治疗格局,然而仅有一部分患者从中获益——且部分早期有效的患者随后会出现复发。本研究针对这一临床谜题提出了一个聚焦问题:如果 PD-1(帕博利珠单抗旨在阻断的免疫“关闭开关”)出现细微变化,会发生什么?作者通过先进的计算机模拟而非患者样本,描绘了 PD-1 中罕见基因变异如何可能削弱或增强药物结合力,从而提供了为何治疗有时失败的线索,以及未来检测或药物如何改进的方向。
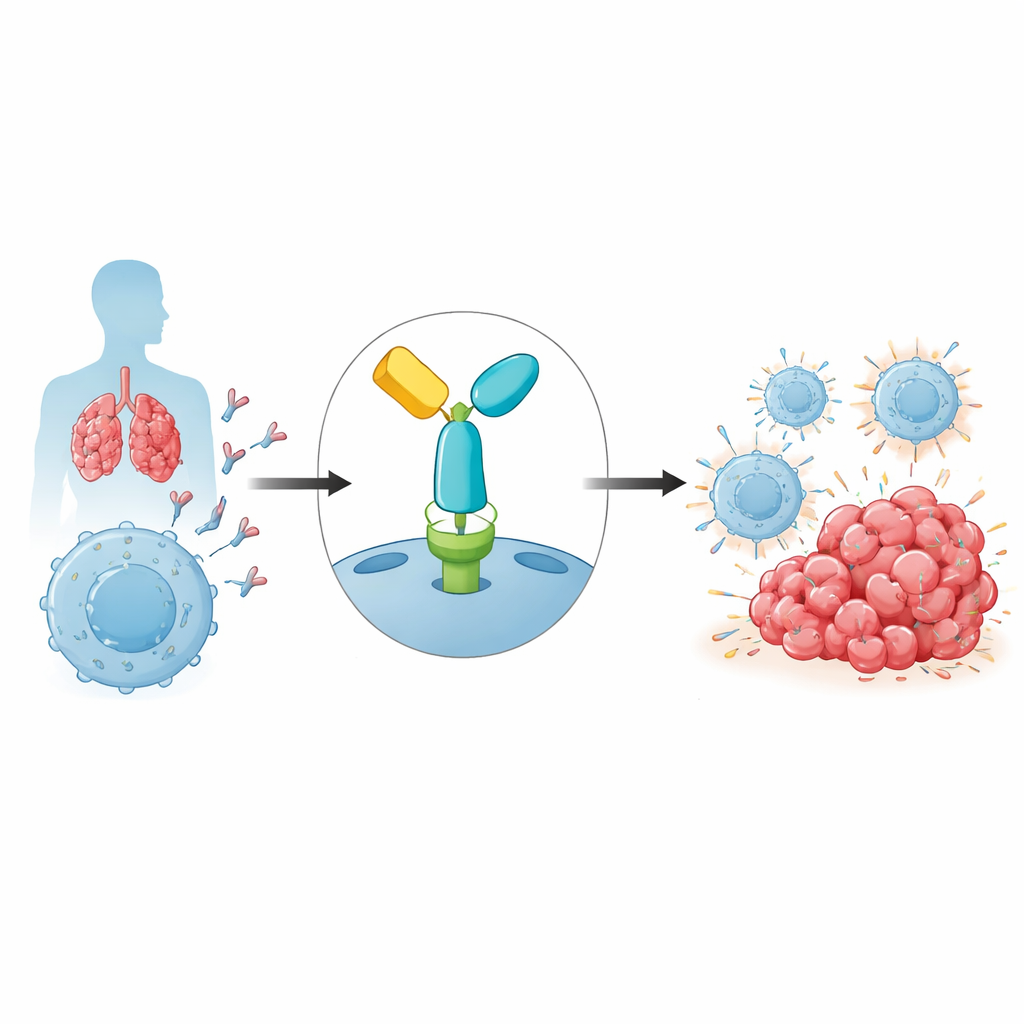
肿瘤利用的免疫刹车
我们的免疫系统依靠 T 细胞识别并清除异常细胞,包括癌细胞。为了避免误伤,T 细胞携带称为免疫检查点的安全开关。其中最重要的之一是 PD-1,这是一种位于 T 细胞表面的受体,当其与其他细胞表面的配体 PD-L1 结合时,会抑制免疫活性。肿瘤常通过展示 PD-L1 来利用这一通路,实际上是告诉附近的 T 细胞停止作用。帕博利珠单抗是一种针对 PD-1 的抗体药物,能结合 PD-1 并阻断该抑制性相互作用,重新激活 T 细胞,使其更有效地攻击肿瘤细胞。尽管该策略在黑色素瘤和肺癌等癌症中带来了持久缓解,但耐药现象普遍存在,其原因仍在逐步被解析。
将计算机作为分子显微镜
研究人员没有在细胞上做实验,而是转向了 PD-1 与帕博利珠单抗复合物的详尽计算模型。他们以该复合物的高分辨率晶体结构为起点,识别出关键接触点——PD-1 上与药物形成氢键、类似润滑的疏水接触或离子“盐桥”的单个氨基酸残基。随后,借助分子动力学模拟,他们观察这些接触在 50 亿分之一秒内的行为,并计算每个残基对维持复合物稳定性的贡献。这使他们能够确定 PD-1 上 16 个对强结合尤为重要的“热点”位点。
影响巨大的罕见基因改变
接着,团队在大型蛋白质数据库中搜索这些热点位点的自然发生变异(突变),发现了 40 种变体,以及另一个先前在实验中报道会破坏帕博利珠单抗结合的突变。在排除掉被预测会损害 PD-1 整体结构的变体后,剩下 28 种“可能良性”的突变——这类变化应当不会破坏 PD-1 的功能,但可能会微妙地改变其与药物的相互作用。对于每一种,他们构建了三维突变体模型并进行了同类型的分子动力学模拟,随后用一种能量计算方法(MM-GBSA)估算帕博利珠单抗与突变体相比于正常版本的结合强度变化。
当关键锚点丢失时
模拟显示,在 28 种突变中有 23 种会削弱帕博利珠单抗结合,有些程度相当显著,而五种实际上增强了结合力。其中三种突变在预测上造成最大亲和力损失:位于 PD-1 第 85 位和 89 位的替换(Asp85Gly、Asp85Asn 和 Pro89Arg)。在正常蛋白中,Asp85 作为静电锚点,与抗体上的精氨酸形成稳固的盐桥和氢键;Pro89 则帮助形成与若干抗体残基紧密的疏水接触簇。Asp85 的突变去除了该位点的负电荷或氢键能力,有效破坏了锚点并使周围接触网络失稳。Pro89Arg 将一个中性且与结构相匹配的残基替换为带正电的残基,扰乱了疏水簇并削弱了其稳定贡献。相比之下,少数位于其他位置的突变在模型中微妙地重塑了界面,可能增强结合力。
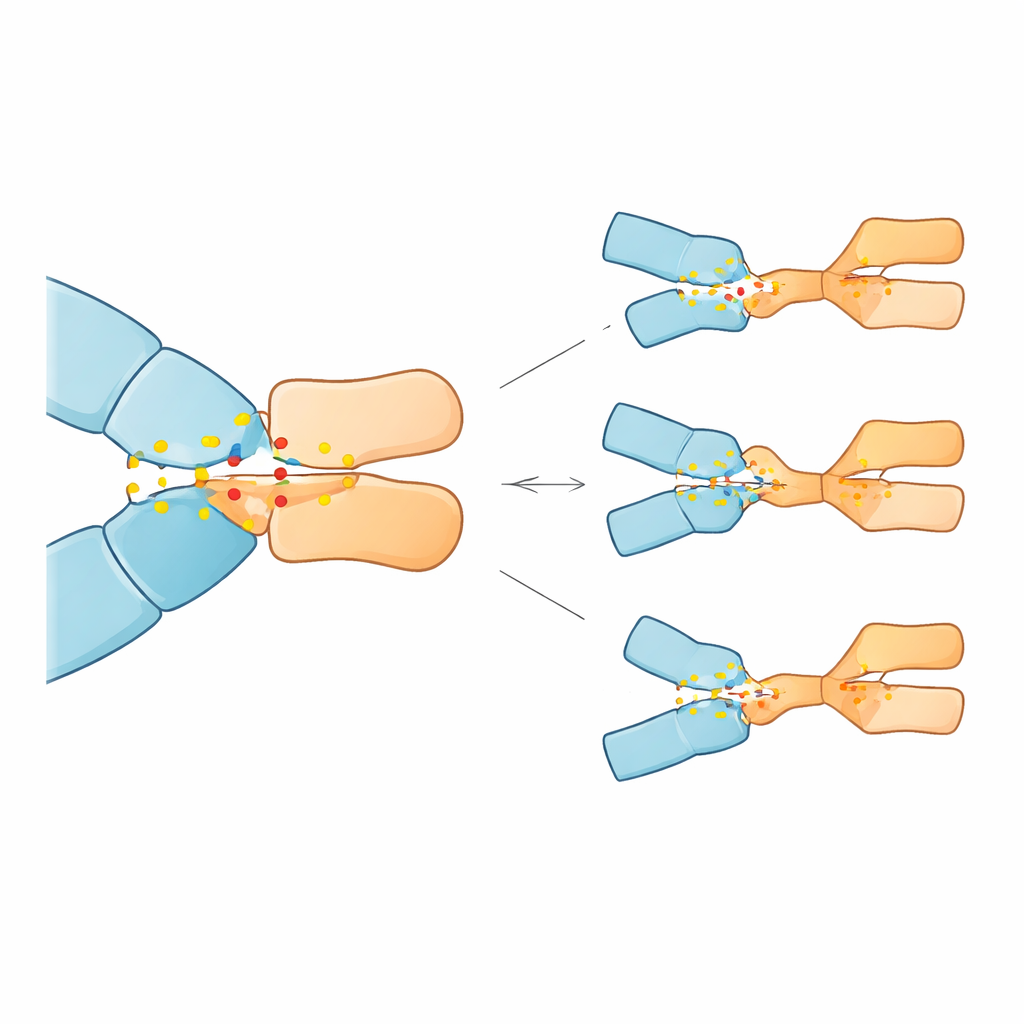
这对患者可能意味着什么
这些发现表明,即使是 PD-1 基因中非常罕见的改变,如果发生在关键接触点,可能也会降低帕博利珠单抗与其靶点的结合,从而削弱其激活 T 细胞抗癌的能力。虽然该研究完全基于计算,还需要实验和临床数据来验证,但它提供了一条路线图:诸如第 85 位和 89 位的特定 PD-1 变体将来可能作为生物标志,用来提示哪些患者更可能发生耐药,或指导在多种针对 PD-1 的药物之间做选择。更广泛地说,该研究展示了深入的计算机模拟如何阐明为何强效免疫疗法在某些人身上成功而在另一些人身上失效的细微分子原因。
引用: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
关键词: PD-1 突变, 帕博利珠单抗耐药, 癌症免疫治疗, 免疫检查点抑制剂, 分子动力学模拟