Clear Sky Science · fr
L'impact des mutations de PD-1 sur la liaison au pembrolizumab : enseignements tirés de la dynamique moléculaire et de l'analyse MM-GBSA
Pourquoi c'est important pour le traitement du cancer
Les médicaments d'immunothérapie comme le pembrolizumab ont transformé la prise en charge de nombreux cancers, mais seule une fraction des patients en bénéficie — et certains répondent initialement puis rechutent. Cette étude pose une question ciblée derrière ce mystère clinique : que se passe-t-il si des modifications subtiles apparaissent dans PD-1, l'« interrupteur d'arrêt » du système immunitaire que le pembrolizumab est conçu pour bloquer ? En utilisant des simulations informatiques avancées plutôt que des échantillons de patients, les auteurs cartographient comment des altérations génétiques rares de PD-1 pourraient affaiblir ou renforcer l'accrochage du médicament, fournissant des indices sur les raisons possibles de l'échec thérapeutique et sur la manière dont de futurs tests ou médicaments pourraient mieux faire.
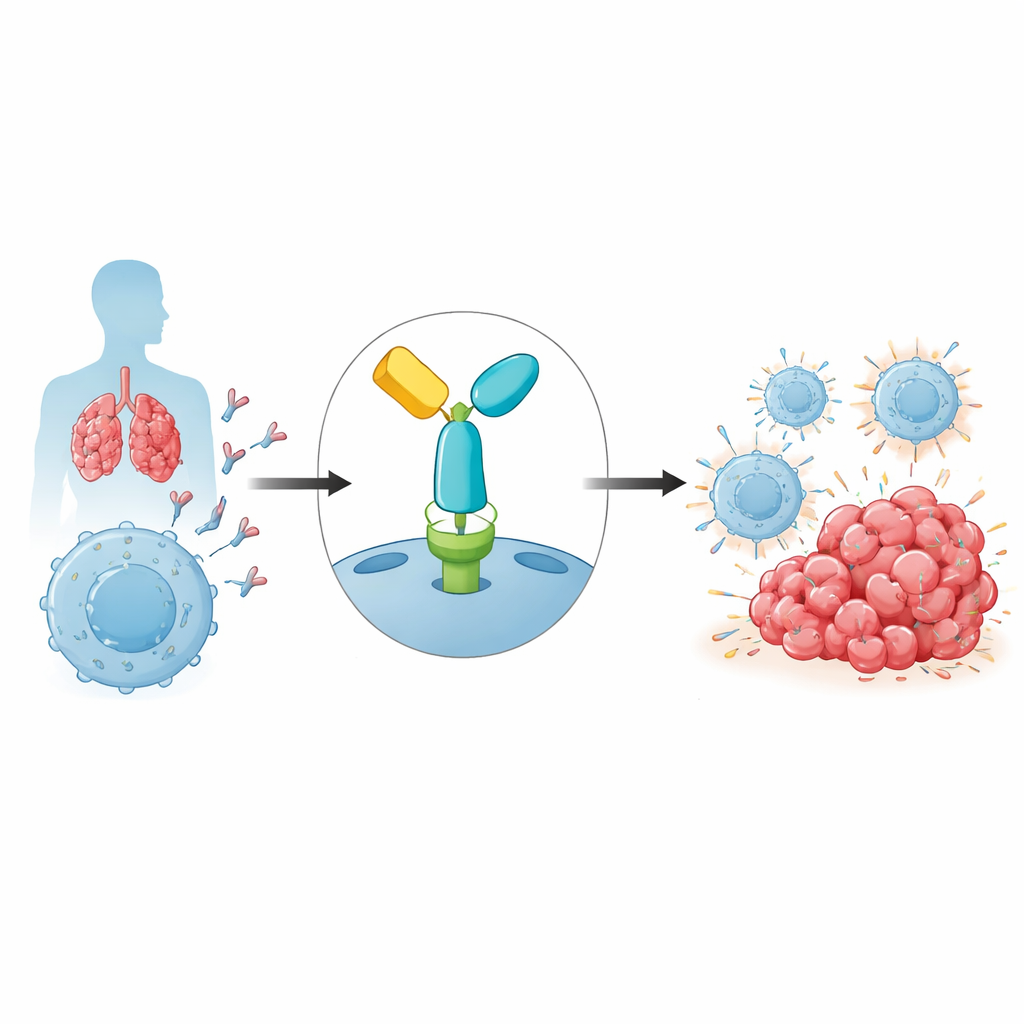
Le frein immunitaire exploité par les tumeurs
Notre système immunitaire s'appuie sur les cellules T pour reconnaître et attaquer les cellules anormales, y compris les cellules cancéreuses. Pour éviter des dégâts collatéraux, les cellules T portent des dispositifs de sécurité appelés points de contrôle immunitaires. L'un des plus importants est PD-1, un récepteur à la surface des cellules T qui, lorsqu'il est engagé par son partenaire PD-L1 sur d'autres cellules, atténue l'activité immunitaire. Les tumeurs exploitent fréquemment cette voie en exprimant PD-L1, indiquant efficacement aux cellules T voisines de se retirer. Le pembrolizumab est un anticorps qui se lie à PD-1 et bloque cette interaction inhibitrice, réactivant les cellules T pour qu'elles puissent attaquer plus efficacement les cellules tumorales. Bien que cette stratégie ait conduit à des rémissions durables dans des cancers tels que le mélanome et le cancer du poumon, la résistance est courante et ses causes restent en cours d'élucidation.
Utiliser l'informatique comme microscope moléculaire
Plutôt que de réaliser des expériences de laboratoire sur des cellules, les chercheurs se sont tournés vers des modèles informatiques détaillés de la protéine PD-1 associée au pembrolizumab. Ils ont commencé par une structure cristalline haute résolution de ce complexe et identifié les points de contact clés — des acides aminés individuels de PD-1 qui forment des liaisons hydrogène, des contacts hydrophobes « graisseux » ou des « ponts salins » ioniques avec le médicament. Ensuite, à l'aide de simulations de dynamique moléculaire, ils ont observé le comportement de ces contacts pendant cinquante milliardièmes de seconde et calculé la contribution de chaque résidu au maintien du complexe. Cela leur a permis d'identifier 16 positions « points chauds » sur PD-1 particulièrement importantes pour une forte liaison.
Modifications génétiques rares mais aux effets disproportionnés
Ensuite, l'équipe a recherché dans une vaste base de données de protéines des changements naturels (mutations) à ces positions critiques et a trouvé 40 variantes, plus une mutation supplémentaire signalée antérieurement pour perturber la liaison au pembrolizumab dans des tests de laboratoire. Après avoir éliminé les variantes prédites pour altérer la structure globale de PD-1, il restait 28 mutations « vraisemblablement bénignes » — des modifications qui devraient laisser PD-1 fonctionnel mais pourraient modifier subtilement son interaction avec les médicaments. Pour chacune d'elles, ils ont construit un modèle tridimensionnel mutant et exécuté le même type de simulation de dynamique moléculaire, suivie d'un calcul d'énergie (MM-GBSA) pour estimer la force de liaison du pembrolizumab par rapport à la version normale.
Quand des ancres clés disparaissent
Les simulations ont révélé que 23 des 28 mutations affaiblissaient la liaison au pembrolizumab, parfois de façon spectaculaire, tandis que cinq la renforçaient en réalité. Trois mutations se sont distinguées par la plus grande perte d'affinité prévue : des substitutions aux positions 85 et 89 de PD-1 (Asp85Gly, Asp85Asn et Pro89Arg). Dans la protéine normale, Asp85 agit comme une ancre électrostatique, formant un pont salin robuste et des liaisons hydrogène avec une arginine de l'anticorps ; Pro89 contribue à former un ensemble de contacts hydrophobes serrés avec plusieurs résidus de l'anticorps. Les mutations d'Asp85 ont supprimé la charge négative ou la capacité à former des liaisons hydrogène à ce site, rompant effectivement l'ancre et déstabilisant le réseau de contacts environnant. Le changement Pro89Arg a remplacé un résidu neutre et adapté en forme par un résidu chargé positivement, perturbant le noyau hydrophobe et réduisant sa contribution stabilisatrice. En revanche, quelques autres mutations à des positions différentes ont subtilement remodelé l'interface de manière à pouvoir améliorer la liaison, du moins dans le modèle.
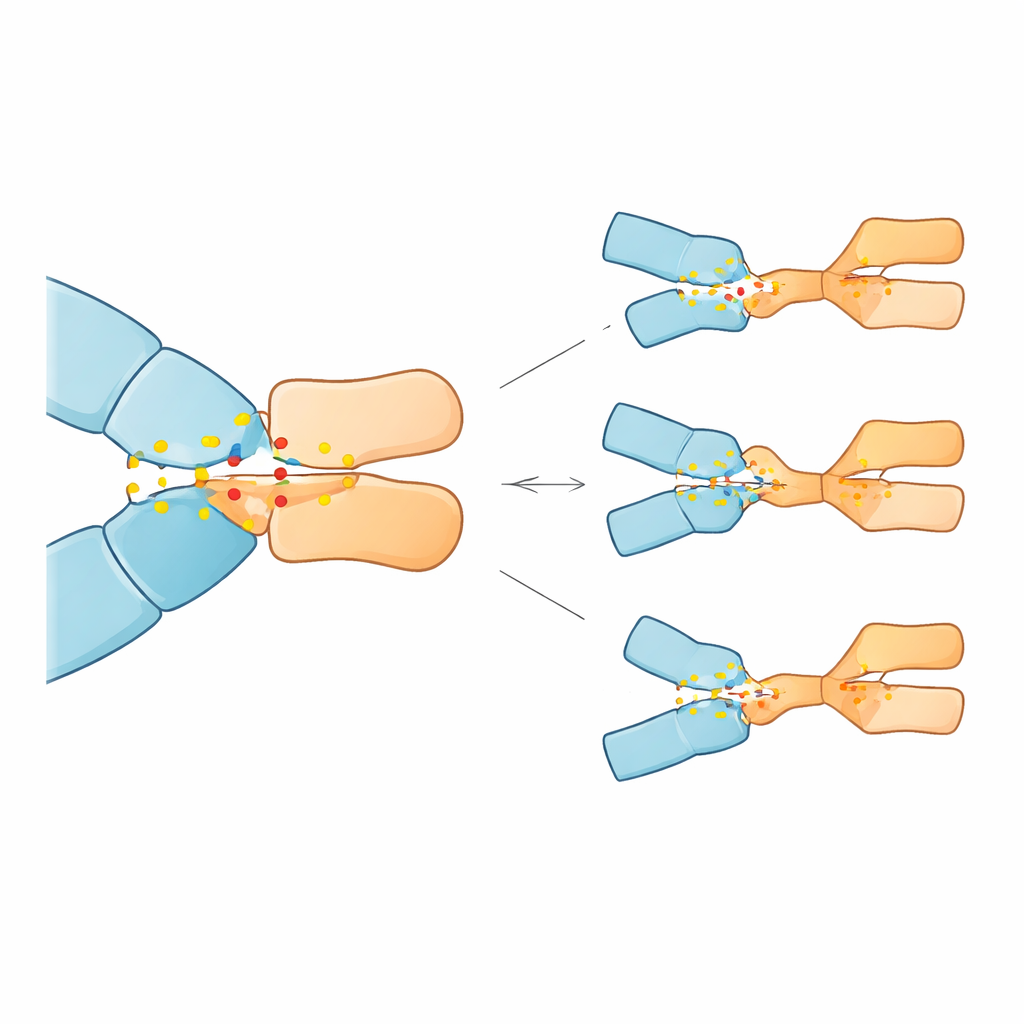
Ce que cela pourrait signifier pour les patients
Ces résultats suggèrent que même des changements très rares dans le gène PD-1, s'ils surviennent à des points de contact cruciaux, pourraient réduire l'aptitude du pembrolizumab à s'accrocher à sa cible et ainsi atténuer sa capacité à libérer les cellules T contre le cancer. Bien que le travail soit entièrement computationnel et nécessite une confirmation expérimentale et clinique, il offre une feuille de route : des variantes spécifiques de PD-1, comme celles aux positions 85 et 89, pourraient un jour servir de biomarqueurs pour signaler des patients à risque accru de résistance ou pour orienter le choix entre différents médicaments ciblant PD-1. Plus largement, l'étude illustre comment des simulations informatiques approfondies peuvent éclairer les raisons moléculaires fines pour lesquelles des immunothérapies puissantes réussissent chez certains patients mais échouent chez d'autres.
Citation: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Mots-clés: Mutations de PD-1, résistance au pembrolizumab, immunothérapie du cancer, inhibiteurs de points de contrôle immunitaires, simulation de dynamique moléculaire