Clear Sky Science · ru
Влияние мутаций PD-1 на связывание пембролизумаба: выводы молекулярной динамики и MM-GBSA анализа
Почему это важно для лечения рака
Лекарства-иммунотерапии, такие как пембролизумаб, преобразили подход к лечению многих видов рака, однако лишь часть пациентов получает от них пользу — и некоторые из тех, кто ответил на терапию сначала, затем рецидивируют. В этом исследовании поставлен конкретный вопрос, лежащий в основе этой клинической загадки: что происходит, если в PD-1, «выключателе» иммунитета, на который нацелен пембролизумаб, возникают тонкие изменения? Используя передовые компьютерные симуляции вместо образцов пациентов, авторы прослеживают, как редкие генетические изменения в PD-1 могут ослаблять или, наоборот, усиливать сцепление с лекарством, давая подсказки о том, почему лечение иногда не срабатывает и как будущие тесты или препараты могли бы быть эффективнее.
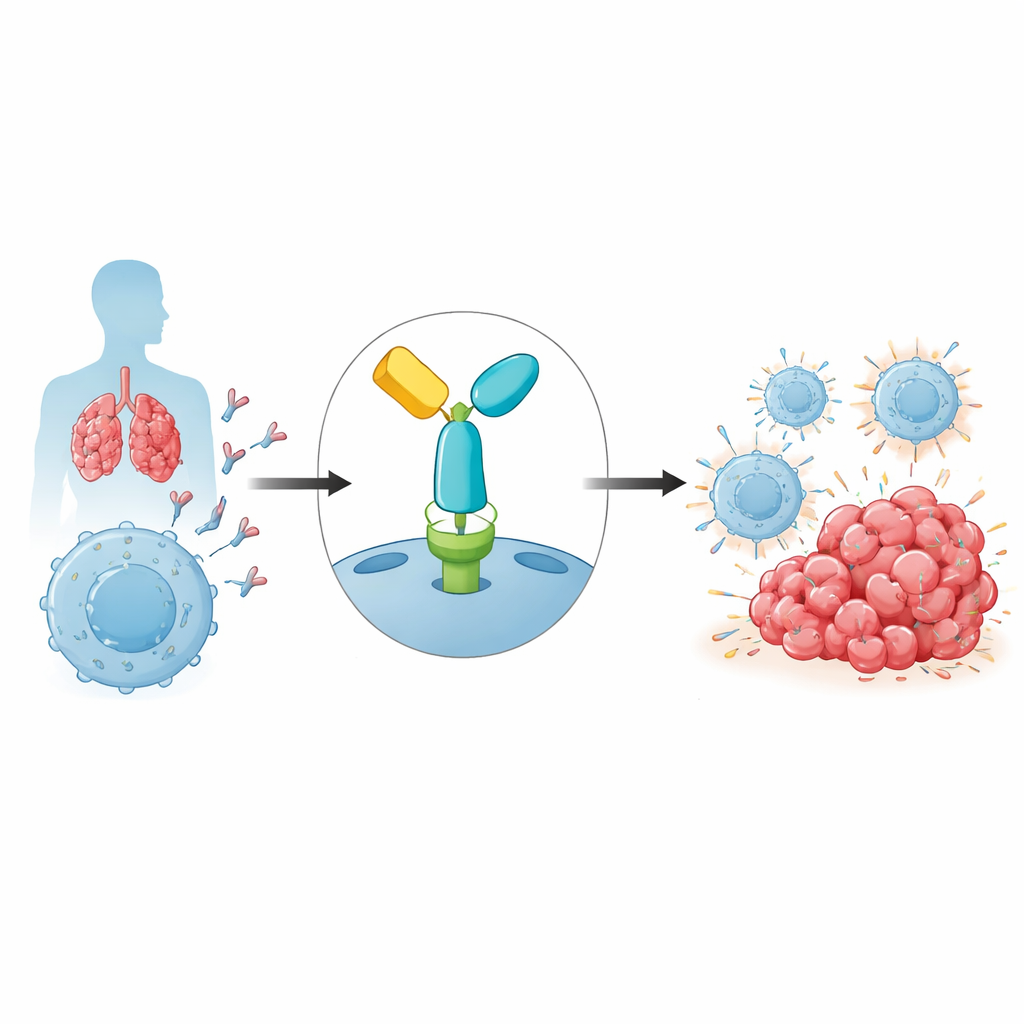
Тормоз иммунитета, которым пользуются опухоли
Наш иммунитет опирается на Т-клетки, которые распознают и атакуют аномальные клетки, включая раковые. Чтобы избежать побочного повреждения, Т-клетки снабжены предохранительными переключателями — иммунными контрольными точками. Одна из важнейших — PD-1, рецептор на Т-клетках, который при взаимодействии со своим партнером PD-L1 на других клетках подавляет иммунную активность. Опухоли часто эксплуатируют этот путь, выставляя PD-L1 и фактически приказывая близлежащим Т-клеткам «успокоиться». Пембролизумаб — это антитело, которое связывается с PD-1 и блокирует это ингибирующее взаимодействие, реактивируя Т-клетки, чтобы они могли эффективнее атаковать опухолевые клетки. Хотя эта стратегия привела к длительным ремиссиям при таких раках, как меланома и рак легкого, резистентность встречается часто, и причины этого пока полностью не ясны.
Компьютеры как молекулярный микроскоп
Вместо лабораторных экспериментов на клетках исследователи обратились к детализированным компьютерным моделям комплекса PD-1 с пембролизумабом. Они начали с высокоразрешающей кристаллической структуры комплекса и выявили ключевые точки контакта — отдельные аминокислоты PD-1, образующие водородные связи, гидрофобные контакты или ионные «соляные мостики» с препаратом. Затем, с помощью молекулярно-динамических симуляций, они проследили, как эти контакты вели себя в течение 50 миллиардных долей секунды, и рассчитали, какой вклад каждая остаточная аминокислота вносит в поддержание комплекса. Это позволило выделить 16 «горячих точек» в PD-1, особенно важных для прочного связывания.
Редкие генетические изменения с непропорциональным эффектом
Далее команда обыскала большую базу данных белков в поисках 자연ных изменений (мутаций) в этих горячих точках и нашла 40 вариантов, плюс одну дополнительную мутацию, ранее отмеченную как нарушающая связывание пембролизумаба в лабораторных тестах. Отфильтровав варианты, которые, как прогнозировалось, повреждают общую структуру PD-1, исследователи получили 28 «вероятно доброкачественных» мутаций — изменений, которые должны оставить PD-1 функциональным, но могут тонко изменить его взаимодействие с лекарством. Для каждой из них они построили трёхмерную модель мутанта и провели те же молекулярно-динамические симуляции, за которыми последовал расчёт энергии методом MM-GBSA, чтобы оценить, насколько сильно пембролизумаб будет связываться по сравнению с нормальной версией.
Когда ключевые якоря теряются
Симуляции показали, что 23 из 28 мутаций ослабляли связывание пембролизумаба, иногда весьма значительно, в то время как пять мутаций усиливали его. Три мутации выделялись как вызывающие наибольшую предсказанную потерю сродства: замены в положениях 85 и 89 PD-1 (Asp85Gly, Asp85Asn и Pro89Arg). В нормальном белке Asp85 действует как электростатический якорь, образуя прочный соляной мост и водородные связи с аргинином на антителе; Pro89 формирует кластер плотных гидрофобных контактов с несколькими остатками антитела. Мутации Asp85 удаляли отрицательный заряд или способность к водородным связям в этой позиции, фактически разрушая якорь и дестабилизируя окружающую сеть контактов. Замена Pro89Arg заменила нейтральный, подогнанный по форме остаток на положительно заряженный, нарушив гидрофобный кластер и уменьшив его стабилизирующий вклад. Напротив, несколько других мутаций в других позициях слегка перестраивали интерфейс так, что в модели это могло улучшить связывание.
Что это может значить для пациентов
Эти результаты предполагают, что даже очень редкие изменения в гене PD-1, если они возникают в критических точках контакта, могут снизить способность пембролизумаба прочно прикрепляться к своей мишени и, следовательно, ослабить его способность высвобождать Т-клетки против рака. Поскольку работа полностью вычислительная и требует экспериментального и клинического подтверждения, она все же предлагает дорожную карту: специфические варианты PD-1, такие как изменения в позициях 85 и 89, могут со временем служить биомаркерами для выявления пациентов с более высоким риском резистентности или для выбора между различными препаратами, нацеленными на PD-1. В более широком плане исследование демонстрирует, как глубокие компьютерные симуляции могут прояснить молекулярные причины, по которым мощная иммунотерапия у одних людей оказывается успешной, а у других — нет.
Цитирование: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Ключевые слова: мутации PD-1, резистентность к пембролизумабу, иммунотерапия рака, ингибиторы иммунных контрольных точек, молекулярно-динамическое моделирование