Clear Sky Science · it
L’impatto delle mutazioni di PD-1 sul legame con pembrolizumab: evidenze da dinamica molecolare e analisi MM-GBSA
Perché questo è importante per il trattamento del cancro
Farmaci immunoterapici come il pembrolizumab hanno trasformato la cura di molti tumori, ma solo una parte dei pazienti ne beneficia — e alcuni di quelli che rispondono inizialmente poi vanno in recidiva. Questo studio indaga una domanda mirata alla base di quel mistero clinico: cosa accade se nel recettore PD-1, l’“interruttore off” del sistema immunitario che pembrolizumab è progettato per bloccare, si verificano cambiamenti sottili? Usando avanzate simulazioni al computer anziché campioni di pazienti, gli autori tracciano come rare alterazioni genetiche in PD-1 possano indebolire o rafforzare la presa del farmaco, offrendo indizi sul perché il trattamento a volte fallisca e su come test futuri o molecole diverse possano funzionare meglio.
Il freno immunitario che i tumori sfruttano
Il nostro sistema immunitario si affida alle cellule T per riconoscere e attaccare cellule anomale, compresi i tumori. Per evitare danni collaterali, le cellule T sono dotate di interruttori di sicurezza chiamati checkpoint immunitari. Uno dei più importanti è PD-1, un recettore sulle cellule T che, quando viene attivato dal suo partner PD-L1 su altre cellule, attenua l’attività immunitaria. I tumori spesso sfruttano questa via mostrando PD-L1, praticamente dicendo alle cellule T vicine di fermarsi. Il pembrolizumab è un anticorpo che si lega a PD-1 e blocca questa interazione inibitoria, riattivando le cellule T in modo che possano attaccare più efficacemente le cellule tumorali. Sebbene questa strategia abbia portato a remissioni prolungate in tumori come il melanoma e il carcinoma polmonare, la resistenza è comune e le ragioni sono ancora in parte da chiarire.
Usare il computer come microscopio molecolare
Invece di condurre esperimenti di laboratorio sulle cellule, i ricercatori si sono rivolti a modelli computazionali dettagliati della proteina PD-1 in complesso con pembrolizumab. Sono partiti da una struttura cristallina ad alta risoluzione di questo complesso e hanno identificato i punti di contatto chiave — singoli amminoacidi di PD-1 che formano legami a idrogeno, contatti idrofobici o ponti salini ionici con il farmaco. Poi, usando simulazioni di dinamica molecolare, hanno osservato come questi contatti si comportavano in un arco di 50 miliardesimi di secondo e hanno calcolato quanto ciascun residuo contribuiva a mantenere il complesso stabile. Questo ha permesso di individuare 16 posizioni «hot spot» su PD-1 particolarmente importanti per un legame forte.
Mutazioni rare con effetti sproporzionati
Successivamente, il team ha cercato in un ampio database proteico cambiamenti naturalmente presenti (mutazioni) in quelle posizioni hot spot e ha trovato 40 varianti, più una mutazione aggiuntiva precedentemente segnalata per interrompere il legame con pembrolizumab in test di laboratorio. Dopo aver eliminato le varianti previste danneggiare la struttura globale di PD-1, sono rimaste 28 mutazioni «probabilmente benigne» — cambiamenti che dovrebbero lasciare PD-1 funzionale ma che potrebbero alterare sottilmente le interazioni con i farmaci. Per ciascuna hanno costruito un modello tridimensionale del mutante e hanno eseguito lo stesso tipo di simulazione di dinamica molecolare, seguita da un metodo di calcolo energetico (MM-GBSA) per stimare quanto fortemente pembrolizumab si legherebbe rispetto alla versione normale.
Quando si perdono ancore chiave
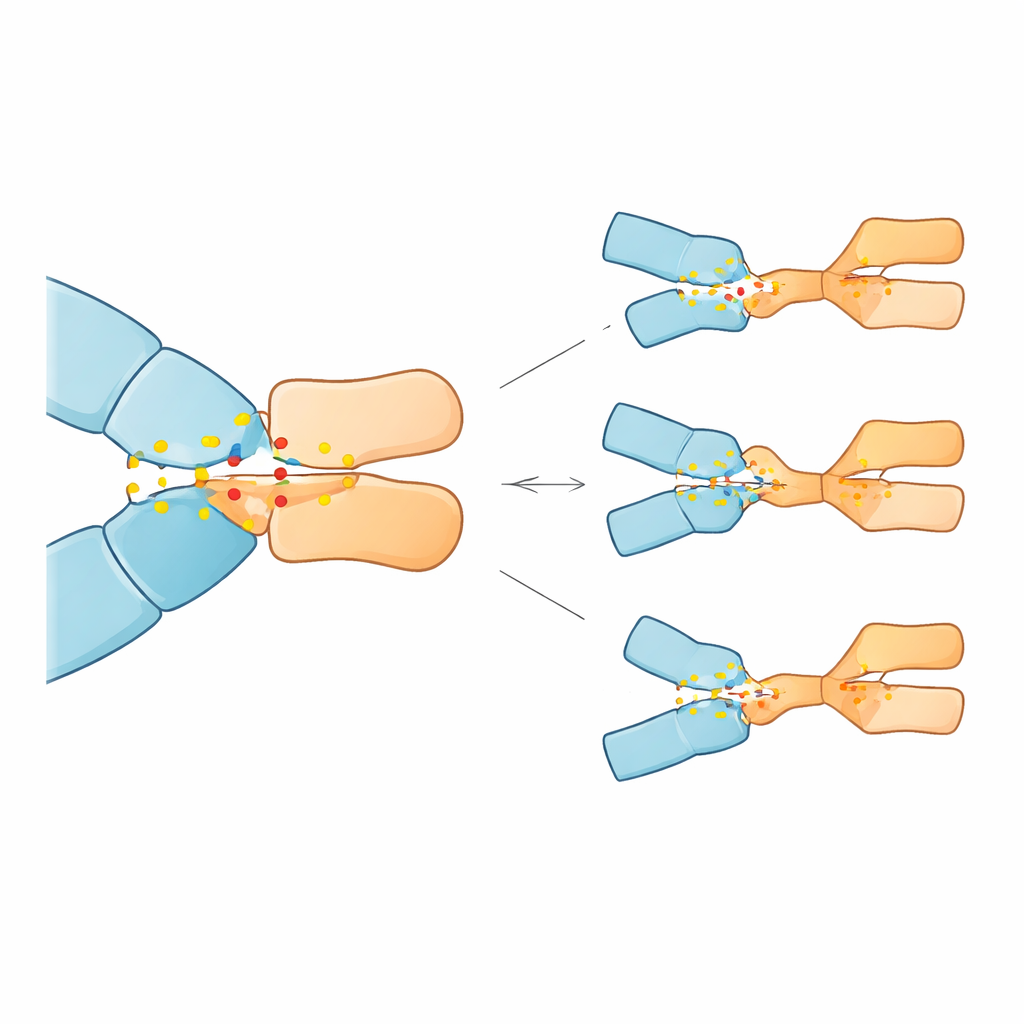
Le simulazioni hanno rivelato che 23 delle 28 mutazioni indebolivano il legame con pembrolizumab, alcune in modo piuttosto drammatico, mentre cinque lo rafforzavano effettivamente. Tre mutazioni si sono distinte per aver causato la maggiore perdita prevista di affinità: sostituzioni nelle posizioni 85 e 89 di PD-1 (Asp85Gly, Asp85Asn e Pro89Arg). Nella proteina normale, Asp85 funge da ancora elettrostatica, formando un solido ponte salino e legami a idrogeno con un arginina sull’anticorpo; Pro89 contribuisce a formare un ammasso di contatti idrofobici aderenti con diversi residui dell’anticorpo. Le mutazioni di Asp85 rimuovevano la carica negativa o la capacità di formare legami a idrogeno in quel sito, rompendo effettivamente l’ancora e destabilizzando la rete di contatti circostanti. La sostituzione Pro89Arg ha rimpiazzato un residuo neutro e sagomato con uno carico positivamente, perturbando il gruppo idrofobico e riducendone il contributo stabilizzante. Invece, poche altre mutazioni in posizioni diverse hanno rimodellato sottilmente l’interfaccia in modi che, almeno nel modello, potrebbero favorire il legame.
Cosa potrebbe significare per i pazienti
Questi risultati suggeriscono che anche cambiamenti molto rari nel gene PD-1, se presenti in punti di contatto cruciali, potrebbero ridurre l’efficacia con cui pembrolizumab si ancora al suo bersaglio e quindi attenuare la sua capacità di liberare le cellule T contro il cancro. Pur essendo un lavoro interamente computazionale che richiede conferme sperimentali e cliniche, offre una mappa: varianti specifiche di PD-1, come quelle nelle posizioni 85 e 89, potrebbero un giorno servire da biomarcatori per segnalare pazienti a maggior rischio di resistenza o per guidare la scelta tra diversi farmaci che mirano a PD-1. Più in generale, lo studio illustra come simulazioni computerizzate approfondite possano chiarire le ragioni molecolari di dettaglio per cui potenti immunoterapie funzionano in alcuni individui ma cedono in altri.
Citazione: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Parole chiave: Mutazioni di PD-1, resistenza a pembrolizumab, immunoterapia oncologica, inibitori dei checkpoint immunitari, simulazione di dinamica molecolare