Clear Sky Science · es
El impacto de las mutaciones en PD-1 sobre la unión de pembrolizumab: perspectivas a partir de dinámica molecular y análisis MM-GBSA
Por qué esto importa para el tratamiento del cáncer
Fármacos de inmunoterapia como pembrolizumab han transformado el tratamiento de muchos cánceres, pero solo una fracción de los pacientes se beneficia, y algunos que responden inicialmente recaen después. Este estudio plantea una pregunta concreta detrás de ese misterio clínico: ¿qué ocurre si se producen cambios sutiles en PD-1, el “interruptor de apagado” inmunitario que pembrolizumab está diseñado para bloquear? Mediante el uso de simulaciones informáticas avanzadas en lugar de muestras de pacientes, los autores cartografían cómo alteraciones genéticas poco frecuentes en PD-1 podrían debilitar o reforzar el agarre del fármaco, ofreciendo pistas sobre por qué el tratamiento a veces falla y cómo futuras pruebas o fármacos podrían mejorar.
El freno inmune que explotan los tumores
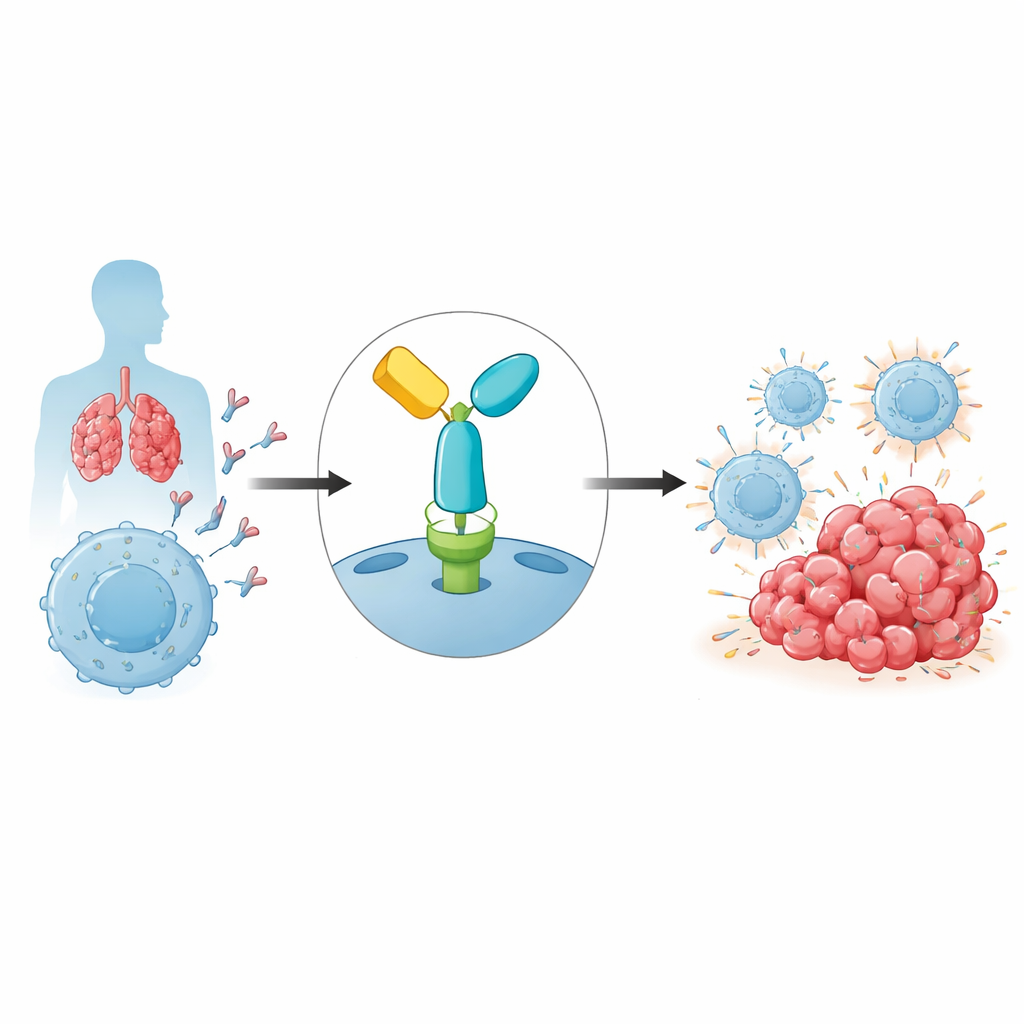
Nuestro sistema inmunitario depende de las células T para reconocer y atacar células anómalas, incluido el cáncer. Para evitar daños colaterales, las células T incorporan interruptores de seguridad llamados puntos de control inmunitarios. Uno de los más importantes es PD-1, un receptor en las células T que, cuando se activa por su pareja PD-L1 en otras células, atenúa la actividad inmune. Los tumores explotan con frecuencia esta vía mostrando PD-L1, lo que equivale a decir a las células T cercanas que se mantengan inactivas. Pembrolizumab es un anticuerpo que se une a PD-1 y bloquea esta interacción inhibitoria, reactivando las células T para que puedan atacar las células tumorales con mayor eficacia. Aunque esta estrategia ha producido remisiones duraderas en cánceres como el melanoma y el de pulmón, la resistencia es común y las razones todavía se están desentrañando.
Usar ordenadores como microscopio molecular
En lugar de realizar experimentos de laboratorio con células, los investigadores recurrieron a modelos informáticos detallados de la proteína PD-1 unida a pembrolizumab. Partieron de una estructura cristalográfica de alta resolución de este complejo e identificaron los puntos de contacto clave: aminoácidos individuales en PD-1 que forman enlaces de hidrógeno, contactos hidrofóbicos tipo “grasiento” o puentes iónicos (puentes salinos) con el fármaco. Luego, mediante simulaciones de dinámica molecular, observaron cómo se comportaban estos contactos durante 50 mil millones de segundos fraccionarios (50 nanosegundos) y calcularon cuánto contribuía cada residuo a mantener el complejo intacto. Esto les permitió señalar 16 posiciones “punto caliente” en PD-1 que son especialmente importantes para una unión fuerte.
Cambios genéticos raros con efectos desproporcionados
A continuación, el equipo buscó en una gran base de datos de proteínas cambios naturales (mutaciones) en esas posiciones críticas y encontró 40 variantes, más una mutación adicional previamente reportada por alterar la unión de pembrolizumab en ensayos de laboratorio. Tras filtrar las variantes predichas como dañinas para la estructura global de PD-1, quedaron 28 mutaciones “probablemente benignas”: cambios que deberían dejar a PD-1 funcional pero que podrían alterar sutilmente cómo interactúa con los fármacos. Para cada una de ellas construyeron un modelo tridimensional mutante y realizaron el mismo tipo de simulación de dinámica molecular, seguido por un cálculo energético (MM-GBSA) para estimar con qué fuerza se uniría pembrolizumab en comparación con la versión normal.
Cuando se pierden anclas clave
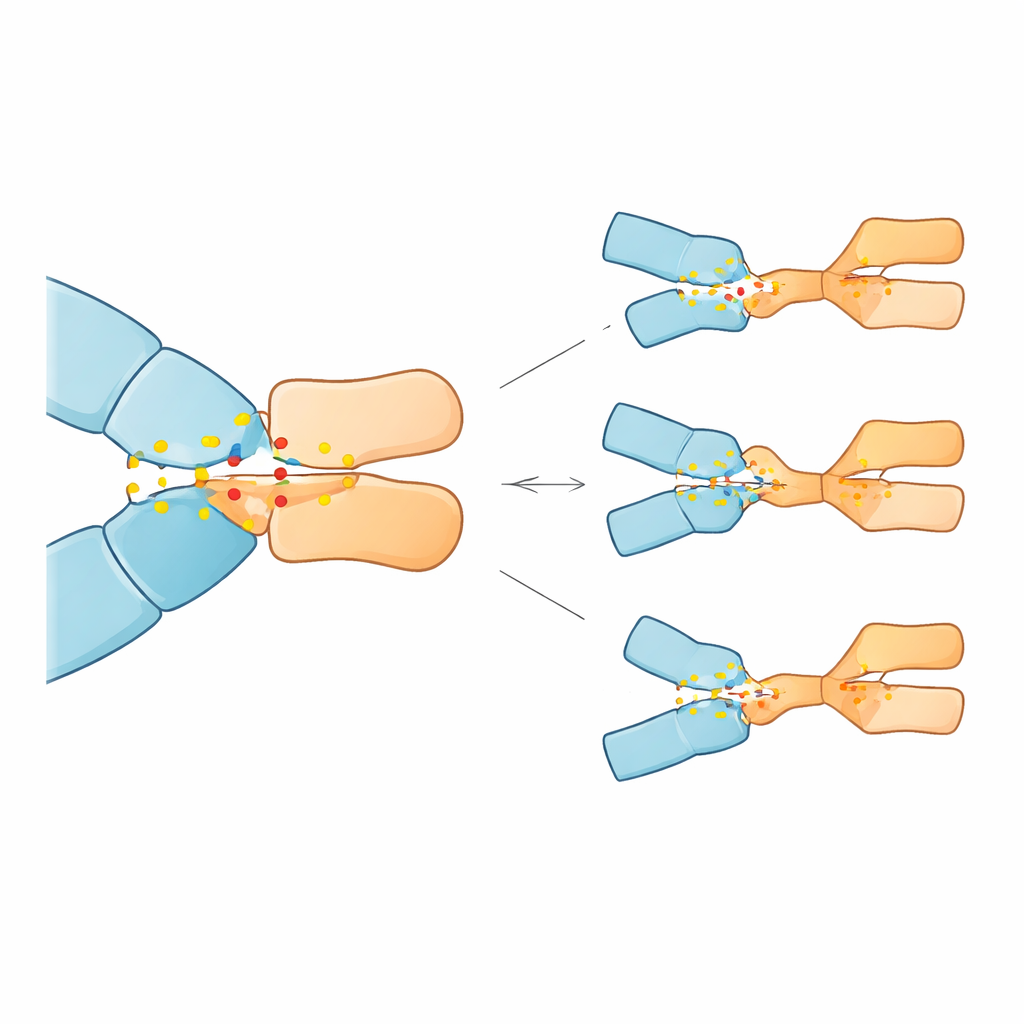
Las simulaciones revelaron que 23 de las 28 mutaciones debilitaron la unión de pembrolizumab, algunas de forma notable, mientras que cinco la reforzaron. Tres mutaciones destacaron por causar la mayor pérdida de afinidad predicha: sustituciones en las posiciones 85 y 89 de PD-1 (Asp85Gly, Asp85Asn y Pro89Arg). En la proteína normal, Asp85 actúa como un ancla electrostática, formando un puente salino robusto y enlaces de hidrógeno con una arginina del anticuerpo; Pro89 contribuye a formar un racimo de contactos hidrofóbicos ajustados con varios residuos del anticuerpo. Las mutaciones en Asp85 eliminaron la carga negativa o la capacidad de formar enlaces de hidrógeno en ese sitio, rompiendo efectivamente el ancla y desestabilizando la red de contactos circundante. El cambio Pro89Arg sustituyó un residuo neutro y de forma encajante por otro con carga positiva, alterando el racimo hidrofóbico y reduciendo su contribución estabilizadora. En contraste, algunas otras mutaciones en posiciones distintas remodelaron sutilmente la interfaz de maneras que, al menos en el modelo, podrían mejorar la unión.
Qué podría significar esto para los pacientes
Estos hallazgos sugieren que incluso cambios muy raros en el gen PD-1, si ocurren en puntos de contacto cruciales, podrían reducir la capacidad de pembrolizumab para adherirse a su objetivo y, por tanto, mermar su habilidad para liberar a las células T contra el cáncer. Aunque el trabajo es enteramente computacional y requiere confirmación experimental y clínica, ofrece una hoja de ruta: variantes específicas de PD-1, como las de las posiciones 85 y 89, podrían en el futuro servir como biomarcadores para identificar a pacientes con mayor riesgo de resistencia o para guiar la elección entre distintos fármacos dirigidos a PD-1. Más en general, el estudio ilustra cómo simulaciones informáticas detalladas pueden esclarecer las razones moleculares finas por las que inmunoterapias potentes funcionan en algunas personas pero fracasan en otras.
Cita: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Palabras clave: mutaciones de PD-1, resistencia a pembrolizumab, inmunoterapia contra el cáncer, inhibidores de puntos de control inmunitarios, simulación de dinámica molecular