Clear Sky Science · tr
PD-1 mutasyonlarının pembrolizumab bağlanması üzerindeki etkisi: moleküler dinamikler ve MM-GBSA analizinden çıkarımlar
Kanser tedavisi için bunun önemi
Pembrolizumab gibi immünoterapi ilaçları birçok kanser için tedaviyi dönüştürdü, ancak hastaların yalnızca bir kısmı bundan fayda görüyor — ve başlangıçta yanıt veren bazı hastalar daha sonra nüksediyor. Bu çalışma, klinik gizemin ardındaki odaklanmış bir soruyu sorguluyor: pembrolizumab’un bloke etmeye tasarlandığı immün “kapama anahtarı” PD-1’de ince değişiklikler olursa ne olur? Araştırmacılar hasta örnekleri yerine gelişmiş bilgisayar simülasyonları kullanarak, PD-1’de nadir görülen genetik değişikliklerin ilacın tutulmasını nasıl zayıflatabileceğini veya güçlendirebileceğini haritalıyor; bu da tedavinin bazen neden başarısız olduğunu ve gelecekte hangi testlerin veya ilaçların daha iyi olabileceğine dair ipuçları veriyor.
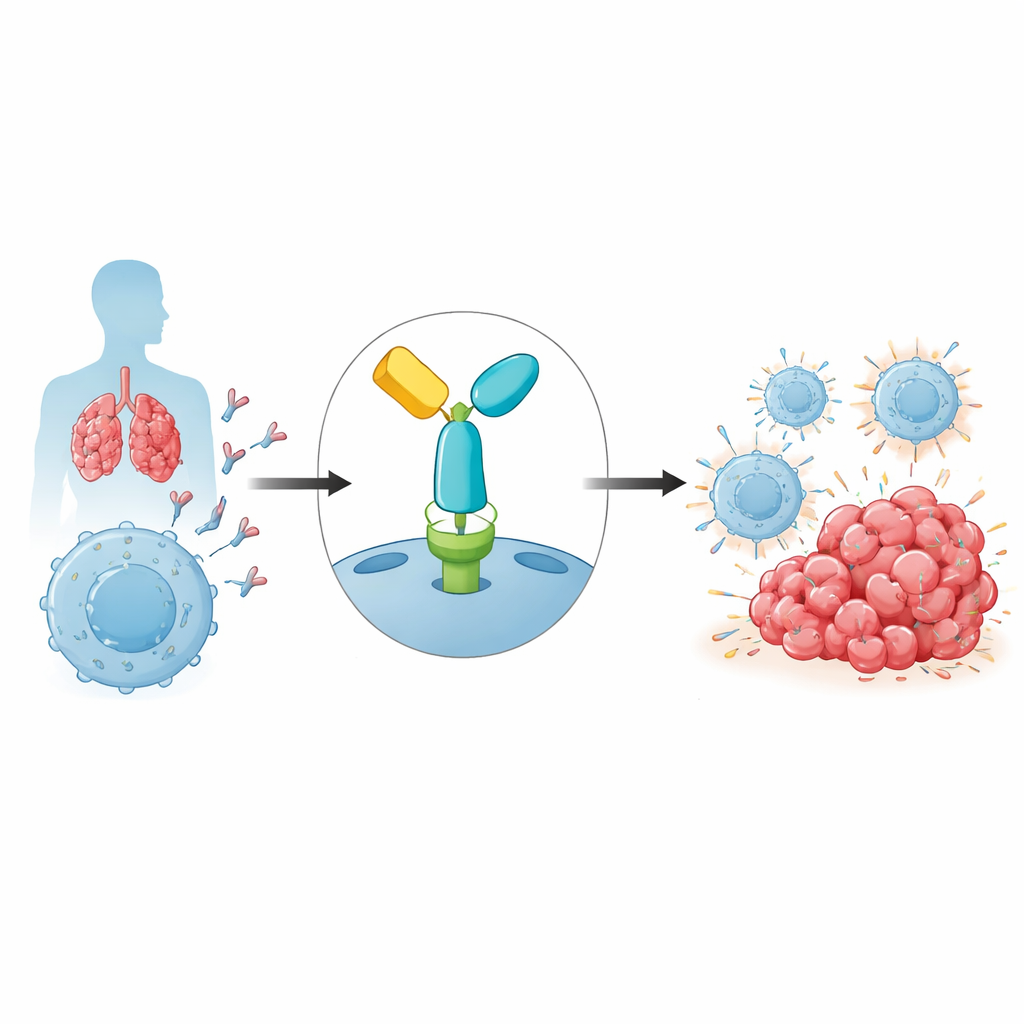
Tümörlerin kullandığı immün fren
Bağışıklık sistemimiz, kanser de dahil olmak üzere anormal hücreleri tanıyıp saldırması için T hücrelerine dayanır. Yan hasarı önlemek için T hücreleri immün kontrol noktaları denilen güvenlik anahtarlarına sahiptir. En önemlilerinden biri, T hücreleri üzerindeki bir reseptör olan PD-1’dir; bu reseptör, diğer hücrelerdeki PD-L1 tarafından bağlandığında bağışıklık aktivitesini azaltır. Tümörler sıklıkla PD-L1 göstererek bu yolağı suistimal eder ve yakınlardaki T hücrelerine geri çekilmelerini söyler. Pembrolizumab, PD-1’e bağlanan ve bu baskılayıcı etkileşimi engelleyen bir antikor ilacıdır; böylece T hücreleri yeniden etkinleştirilir ve tümör hücrelerine daha etkili saldırabilir. Bu strateji melanom ve akciğer kanseri gibi bazı kanserlerde uzun süreli remisyonlar sağlamış olsa da direnç yaygındır ve nedenleri hâlâ çözülmektedir.
Moleküler mikroskop olarak bilgisayar kullanmak
Araştırmacılar hücrelerde laboratuvar deneyleri yürütmek yerine, pembrolizumab ile bir arada kilitlenmiş PD-1 proteininin ayrıntılı bilgisayar modellerine başvurdular. Bu kompleksin yüksek çözünürlüklü kristal yapısıyla başladılar ve ilacın bağlandığı PD-1 üzerindeki ana temas noktalarını — hidrojen bağları, yağlayıcı benzeri hidrofobik temaslar veya iyonik “tuz köprüleri” oluşturan bireysel amino asitleri — belirlediler. Ardından moleküler dinamikler simülasyonları kullanarak bu temasların 50 milyar saniyenin küçük bir parçası boyunca (nanosaniye ölçeğinde) nasıl davrandığını izlediler ve her kalıntının kompleksin bütünlüğünü korumaya ne kadar katkıda bulunduğunu hesapladılar. Bu, güçlü bağlanma için özellikle önemli 16 PD-1 “sıcak nokta” pozisyonunu tespit etmelerini sağladı.
Büyütülmüş etkili nadir genetik değişiklikler
Sonrasında ekip, bu sıcak nokta pozisyonlarındaki doğal olarak oluşan değişiklikleri (mutasyonları) bulmak için büyük bir protein veritabanında arama yaptı ve 40 varyant ile laboratuvar testlerinde pembrolizumab bağlanmasını bozduğu daha önce rapor edilmiş ek bir mutasyon buldu. PD-1’in genel yapısını zedelemesi öngörülen varyantları filtreledikten sonra geriye, yapıyı koruyacak ancak ilacın etkileşimini ince şekilde değiştirebilecek 28 “muhtemelen iyi huylu” mutasyon kaldı. Bunların her biri için üç boyutlu bir mutant model oluşturup aynı tür moleküler dinamikler simülasyonunu çalıştırdılar ve ardından pembrolizumab’un normal versiyonla karşılaştırıldığında ne kadar güçlü bağlanacağını tahmin etmek için bir enerji hesaplama yöntemi (MM-GBSA) uyguladılar.
Ana çapa kaybedildiğinde
Simülasyonlar, 28 mutasyondan 23’ünün pembrolizumab bağlanmasını zayıflattığını, bazı durumlarda oldukça dramatik biçimde, beşinin ise aslında güçlendirdiğini gösterdi. En büyük öngörülen afinité kaybına neden olan üç mutasyon öne çıktı: PD-1’in 85 ve 89 numaralı pozisyonlarındaki substitüsyonlar (Asp85Gly, Asp85Asn ve Pro89Arg). Normal proteinde Asp85 elektrostatik bir çapa görevi görür; antikor üzerindeki bir argininle sağlam bir tuz köprüsü ve hidrojen bağları oluşturur; Pro89 ise birkaç antikor kalıntısıyla sıkı bir hidrofobik temas kümesi oluşturmaya yardımcı olur. Asp85 mutasyonları bu bölgedeki negatif yükü veya hidrojen bağı kurma yeteneğini ortadan kaldırarak çapanın kopmasına ve çevresindeki temas ağının kararsızlaşmasına yol açtı. Pro89Arg değişimi şekil itibarıyla nötr ve yerini iyi dolduran bir kalıntıyı pozitif yüklü bir tanesiyle değiştirdi; bu, hidrofobik kümeyi bozdu ve stabilize edici katkısını azalttı. Buna karşın, farklı pozisyonlardaki birkaç başka mutasyon ara yüzü ince şekilde yeniden şekillendirerek modele göre bağlanmayı artırmış olabilir.
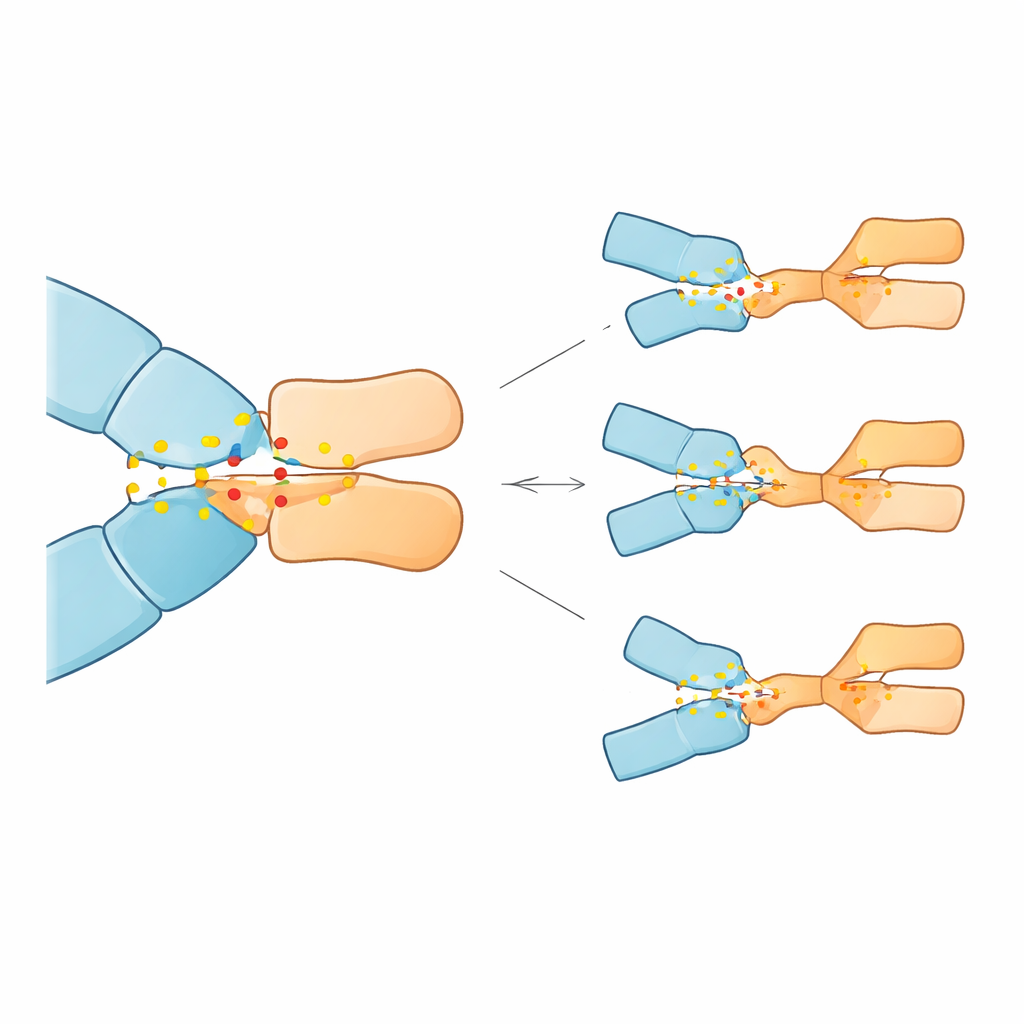
Bu hastalar için ne anlama gelebilir
Bu bulgular, PD-1 genindeki çok nadir değişikliklerin, eğer kritik temas noktalarında ortaya çıkarlarsa, pembrolizumab’un hedefine tutunma gücünü azaltabileceğini ve dolayısıyla T hücrelerini kanserle mücadele için serbest bırakma yeteneğini köreltilebileceğini öne sürüyor. Çalışma tamamen hesaplamalı olup deneysel ve klinik onay gerektirse de bir yol haritası sunuyor: 85 ve 89 pozisyonlarındaki spesifik PD-1 varyantları bir gün direnç riski yüksek hastaları işaretlemek veya farklı PD-1 hedefleyen ilaçlar arasında seçim yapmaya rehberlik etmek için biyobelirteçler olarak kullanılabilir. Daha geniş açıdan, çalışma, ayrıntılı bilgisayar simülasyonlarının güçlü immünoterapilerin bazı hastalarda neden başarılı olup bazılarında başarısız olduğuna dair moleküler düzeyde açıklamalar sağlayabileceğini gösteriyor.
Atıf: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Anahtar kelimeler: PD-1 mutasyonları, pembrolizumab direnci, kanser immünoterapisi, immün kontrol noktası inhibitörleri, moleküler dinamikler simülasyonu