Clear Sky Science · sv
Effekten av PD-1‑mutationer på pembrolizumab‑bindning: insikter från molekylär dynamik och MM‑GBSA‑analys
Varför detta spelar roll för cancerbehandling
Immunterapiläkemedel som pembrolizumab har förändrat vården för många cancerformer, men bara en del av patienterna får verklig nytta — och vissa som initialt svarar får senare återfall. Denna studie ställer en fokuserad fråga bakom det kliniska mysteriet: vad händer om subtila förändringar uppstår i PD‑1, den immuna ”avstängningsknapp” som pembrolizumab är utformad för att blockera? Genom att använda avancerade datorimuleringar i stället för patientprover kartlägger författarna hur sällsynta genetiska förändringar i PD‑1 kan försvaga eller förstärka läkemedlets grepp, vilket ger ledtrådar till varför behandlingen ibland misslyckas och hur framtida tester eller läkemedel kan förbättras.
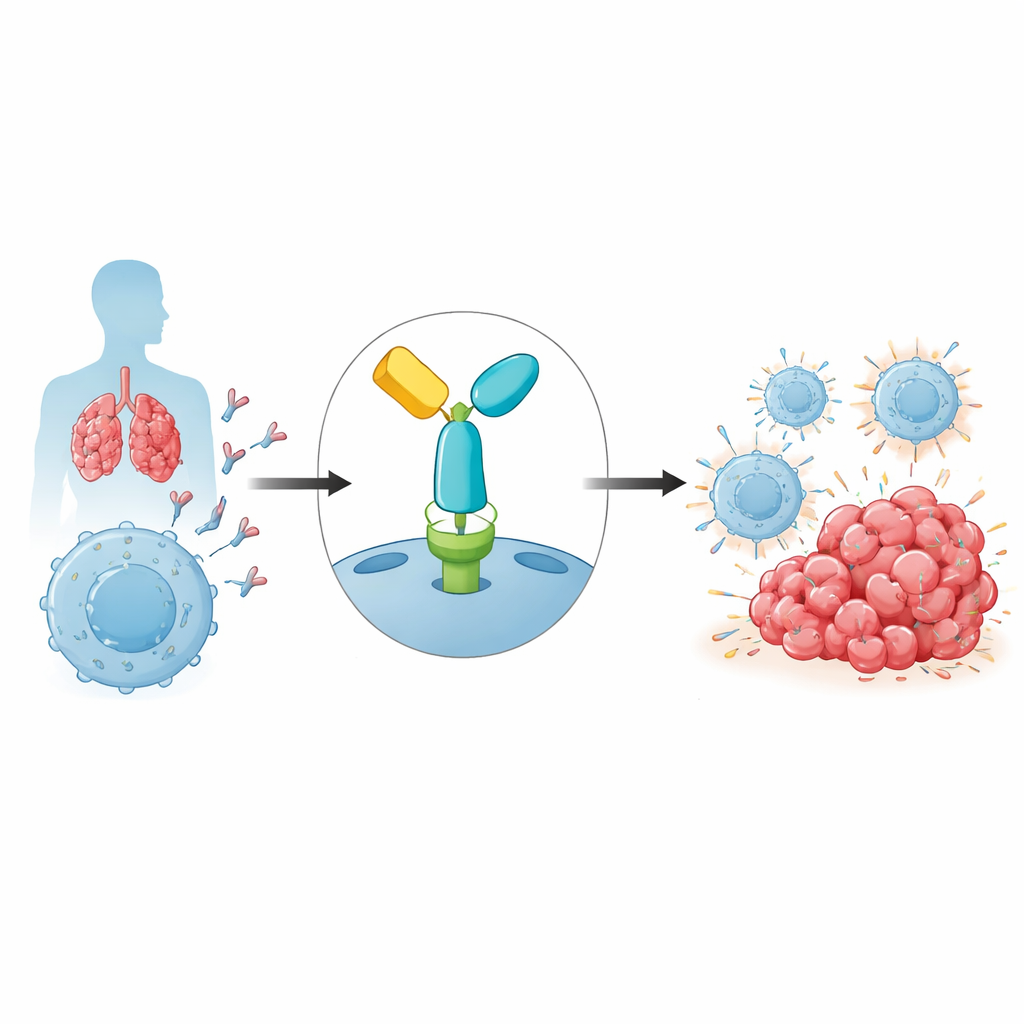
Den immuna broms som tumörer utnyttjar
Vårt immunsystem är beroende av T‑celler för att känna igen och angripa onormala celler, inklusive cancer. För att undvika oavsiktliga skador bär T‑celler säkerhetsspärrar kallade immunkontrollpunkter. En av de viktigaste är PD‑1, en receptor på T‑celler som, när den bindas av sin partner PD‑L1 på andra celler, dämpar den immunologiska aktiviteten. Tumörer utnyttjar ofta denna väg genom att visa upp PD‑L1, vilket i praktiken säger åt närliggande T‑celler att stå tillbaka. Pembrolizumab är ett antikroppsbaserat läkemedel som binder till PD‑1 och blockerar denna hämmande interaktion, vilket återaktiverar T‑celler så att de kan angripa tumörceller mer effektivt. Även om denna strategi har lett till långvariga remissioner vid cancerformer som melanom och lungcancer är resistens vanlig, och orsakerna undersöks fortfarande.
Använda datorer som ett molekylärt mikroskop
I stället för att utföra labbexperiment på celler vände sig forskarna till detaljerade datormodeller av PD‑1‑proteinet bundet till pembrolizumab. De började med en högupplöst kristallstruktur av detta komplex och identifierade nyckelkontaktpunkter — individuella aminosyror på PD‑1 som bildar vätebindningar, hydrofoba kontaktytor eller joniska ”saltbryggor” med läkemedlet. Därefter, med hjälp av molekylär dynamiksimulering, följde de hur dessa kontakter uppförde sig över 50 miljondels sekund och beräknade hur mycket varje rest bidrog till att hålla komplexet intakt. Detta gjorde det möjligt att peka ut 16 ”hot spot”-positioner på PD‑1 som är särskilt viktiga för stark bindning.
Sällsynta genetiska förändringar med oproportionerliga effekter
Nästa steg var att söka i en stor proteindatabas efter naturligt förekommande förändringar (mutationer) i dessa hot spot‑positioner och man fann 40 varianter, plus ytterligare en mutation som tidigare rapporterats störa pembrolizumab‑bindning i laboratorietester. Efter att ha filtrerat bort varianter som förutsågs skada PD‑1:s övergripande struktur återstod 28 ”troligen godartade” mutationer — förändringar som bör lämna PD‑1 funktionell men som subtilt kan ändra hur det interagerar med läkemedel. För var och en av dessa byggde de en tredimensionell mutantmodell och körde samma typ av molekylär dynamiksimulering, följt av en energiberäkning (MM‑GBSA) för att uppskatta hur starkt pembrolizumab skulle binda jämfört med den normala versionen.
När viktiga ankare försvinner
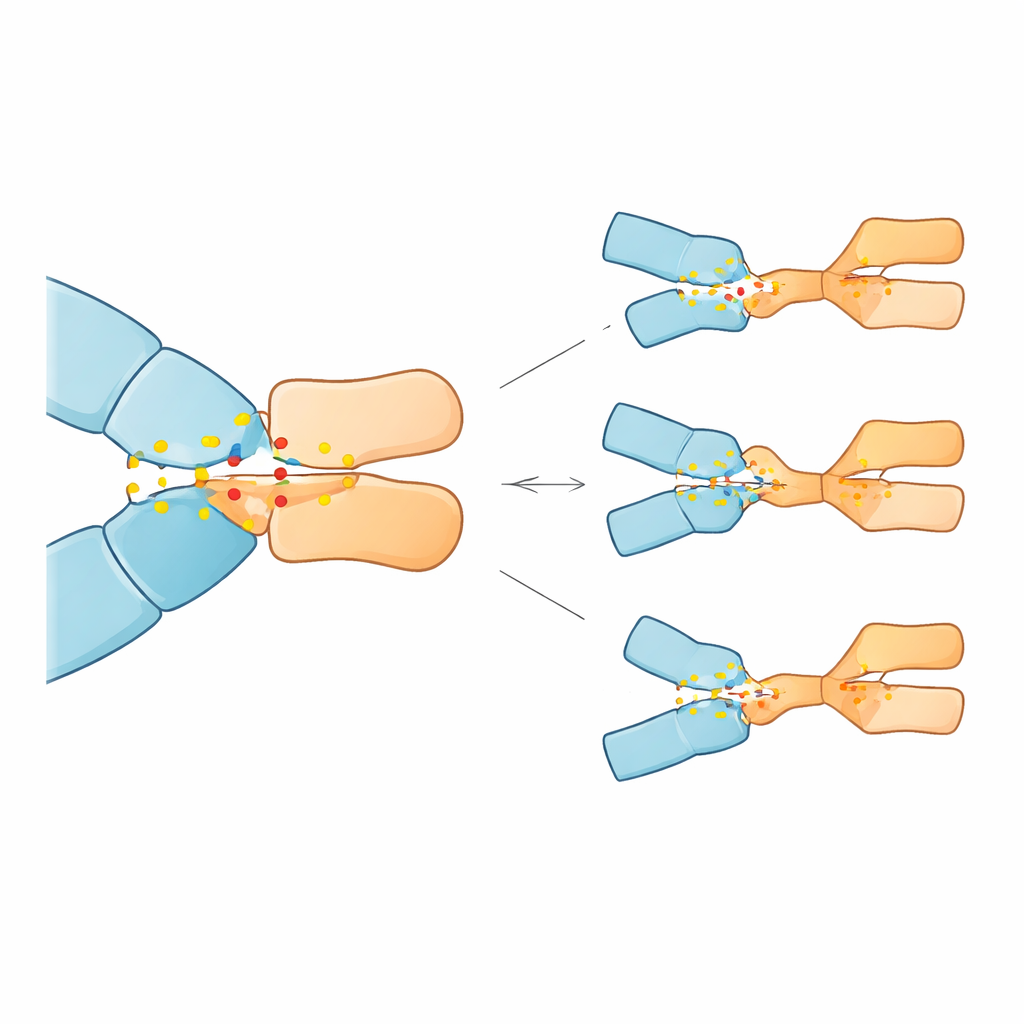
Simuleringarna visade att 23 av de 28 mutationerna försvagade pembrolizumab‑bindningen, några avsevärt, medan fem faktiskt förstärkte den. Tre mutationer stack ut för att orsaka den största förutsagda förlusten i affinitet: substitutioner vid positionerna 85 och 89 i PD‑1 (Asp85Gly, Asp85Asn och Pro89Arg). I det normala proteinet fungerar Asp85 som ett elektrostatiskt ankare och bildar en robust saltbrygga och vätebindningar med en arginin på antikroppen; Pro89 hjälper till att skapa en kluster av täta hydrofoba kontakter med flera antikroppsrester. Asp85‑mutationerna tog bort den negativa laddningen eller förmågan att bilda vätebindningar på denna plats, vilket i praktiken bröt ankaret och destabiliserade det omgivande kontaktnätverket. Pro89Arg‑ändringen ersatte en neutral, formpassande rest med en positivt laddad, störde det hydrofoba klustret och minskade dess stabiliserande bidrag. I kontrast omformade några andra mutationer gränsytan subtilt på sätt som i modellen kunde förbättra bindningen.
Vad detta kan innebära för patienter
Dessa fynd tyder på att även mycket sällsynta förändringar i PD‑1‑genen, om de inträffar i avgörande kontaktpunkter, kan minska hur väl pembrolizumab fäster vid sitt mål och därigenom dämpa dess förmåga att frigöra T‑celler mot cancer. Eftersom arbetet är helt beräkningsbaserat och behöver experimentell och klinisk bekräftelse erbjuder det ändå en färdplan: specifika PD‑1‑varianter, som de vid positionerna 85 och 89, kan någon gång fungera som biomarkörer för att flagga patienter med högre risk för resistens eller för att vägleda valet mellan olika PD‑1‑inriktade läkemedel. Mer generellt illustrerar studien hur djupgående datorsimuleringar kan belysa de finmaskiga molekylära skälen till varför kraftfulla immunterapier lyckas hos vissa personer men sviktar hos andra.
Citering: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Nyckelord: PD-1‑mutationer, pembrolizumab‑resistens, cancerimmunoterapi, hämmare av immunkontrollpunkter, molekylär dynamiksimulering