Clear Sky Science · de
Die Auswirkungen von PD‑1‑Mutationen auf die Pembrolizumab‑Bindung: Erkenntnisse aus Molekulardynamik und MM‑GBSA‑Analysen
Warum das für die Krebstherapie wichtig ist
Immuntherapien wie Pembrolizumab haben die Behandlung vieler Krebsarten verändert, dennoch profitieren nur ein Teil der Patienten – und manche, die zunächst ansprechen, erleiden später ein Rezidiv. Diese Studie stellt eine gezielte Frage hinter diesem klinischen Rätsel: Was passiert, wenn es subtile Veränderungen in PD‑1 gibt, dem immunologischen «Aus‑Schalter», den Pembrolizumab blockieren soll? Mithilfe fortgeschrittener Computersimulationen statt Patientenproben vermessen die Autorinnen und Autoren, wie seltene genetische Veränderungen in PD‑1 den Halt des Medikaments schwächen oder verstärken könnten, und liefern damit Hinweise darauf, warum die Behandlung manchmal versagt und wie künftige Tests oder Wirkstoffe besser gestaltet werden könnten.
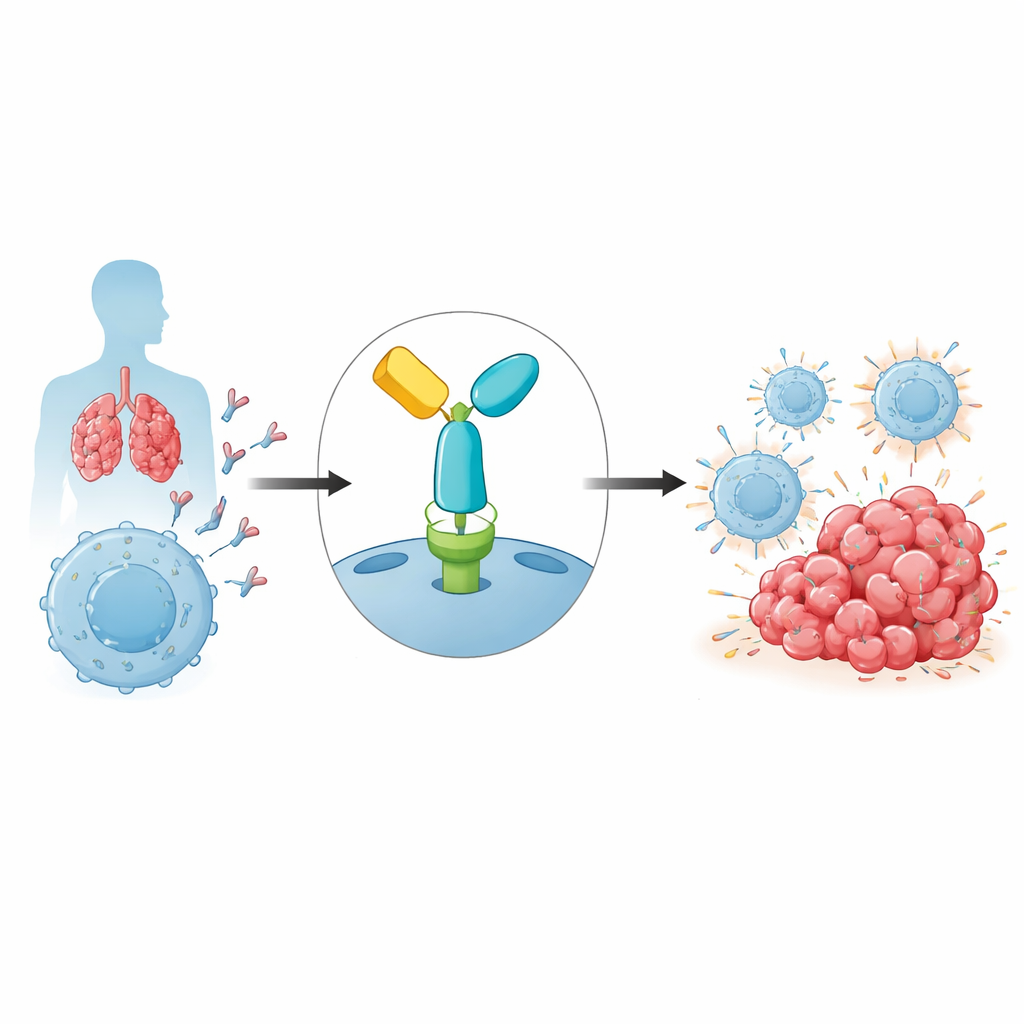
Die immunologische Bremse, die Tumoren ausnutzen
Unser Immunsystem verlässt sich auf T‑Zellen, um abnorme Zellen, einschließlich Krebszellen, zu erkennen und anzugreifen. Um Kollateralschäden zu vermeiden, tragen T‑Zellen Sicherheitsabschaltungen, sogenannte Immuncheckpoints. Einer der wichtigsten ist PD‑1, ein Rezeptor auf T‑Zellen, der bei Bindung seines Partners PD‑L1 auf anderen Zellen die Immunaktivität dämpft. Tumoren nutzen diesen Weg häufig, indem sie PD‑L1 präsentieren und den benachbarten T‑Zellen effektiv signalisieren, sich zurückzuhalten. Pembrolizumab ist ein Antikörperwirkstoff, der an PD‑1 bindet und diese hemmende Interaktion blockiert, wodurch T‑Zellen reaktiviert werden und Tumorzellen effektiver attackieren können. Obwohl diese Strategie zu langanhaltenden Remissionen bei Krebsarten wie Melanom und Lungenkrebs geführt hat, ist Resistenzen häufig, und die Ursachen werden weiterhin erforscht.
Computer als molekulares Mikroskop
Anstatt Laborversuche an Zellen durchzuführen, nutzten die Forschenden detaillierte Computermodelle des PD‑1‑Proteins im Komplex mit Pembrolizumab. Sie starteten mit einer hochauflösenden Kristallstruktur dieses Komplexes und identifizierten die entscheidenden Kontaktstellen – einzelne Aminosäuren auf PD‑1, die Wasserstoffbrücken, hydrophobe Kontakte oder ionische «Salzbrücken» mit dem Medikament ausbilden. Anschließend beobachteten sie mittels Molekulardynamik‑Simulationen, wie sich diese Kontakte über 50 Milliardstel Sekunden verhielten, und berechneten, welchen Beitrag jede Restseite zur Stabilität des Komplexes leistete. So konnten sie 16 „Hot‑Spot“-Positionen auf PD‑1 lokalisieren, die besonders wichtig für eine starke Bindung sind.
Seltene genetische Veränderungen mit überproportionalen Effekten
Danach durchsuchte das Team eine große Protein‑Datenbank nach natürlich vorkommenden Veränderungen (Mutationen) an diesen Hot‑Spot‑Positionen und fand 40 Varianten sowie eine zusätzliche Mutation, die zuvor in Labortests gemeldet worden war, weil sie die Pembrolizumab‑Bindung störte. Nach dem Herausfiltern von Varianten, die voraussichtlich die Gesamtstruktur von PD‑1 schädigen würden, blieben 28 „wahrscheinlich gutartige“ Mutationen übrig – Veränderungen, die PD‑1 funktionell erhalten sollten, aber die Wechselwirkung mit Medikamenten subtil verändern könnten. Für jede dieser Varianten bauten die Forschenden ein dreidimensionales Mutantenmodell, führten die gleichen Molekulardynamik‑Simulationen durch und nutzten anschließend eine Energieberechnungsmethode (MM‑GBSA), um abzuschätzen, wie stark Pembrolizumab im Vergleich zur normalen Version binden würde.
Wenn wichtige Verankerungen verloren gehen
Die Simulationen zeigten, dass 23 der 28 Mutationen die Pembrolizumab‑Bindung abschwächten, teils sehr deutlich, während fünf die Bindung tatsächlich verstärkten. Drei Mutationen fielen besonders auf, weil sie den größten vorhergesagten Affinitätsverlust verursachten: Substitutionen an den Positionen 85 und 89 von PD‑1 (Asp85Gly, Asp85Asn und Pro89Arg). Im normalen Protein wirkt Asp85 als elektrostatische Verankerung, bildet eine robuste Salzbrücke und Wasserstoffbindungen zu einem Arginin des Antikörpers; Pro89 trägt zur Ausbildung eines kompakten hydrophoben Clusters mit mehreren Antikörper‑Resten bei. Die Asp85‑Mutationen beseitigten die negative Ladung oder die Fähigkeit zur Wasserstoffbindung an dieser Stelle, wodurch die Verankerung entfernt und das umgebende Kontaktnetz destabilisiert wurde. Der Pro89Arg‑Austausch ersetzte eine neutrale, formpassende Seite durch eine positiv geladene, störte das hydrophobe Cluster und reduzierte dessen stabilisierenden Beitrag. Im Gegensatz dazu formten einige andere Mutationen an unterschiedlichen Positionen die Schnittstelle so um, dass die Bindung im Modell leicht verstärkt werden konnte.
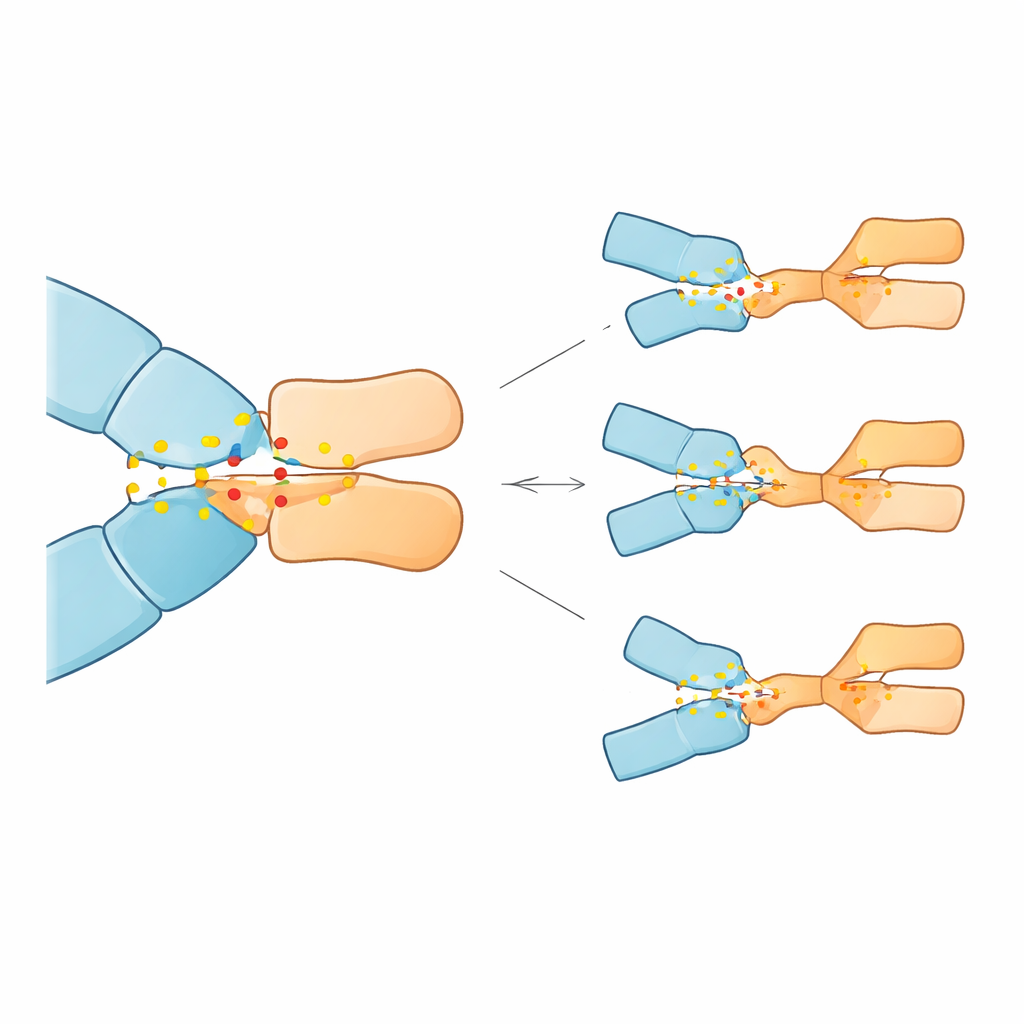
Was das für Patienten bedeuten könnte
Diese Ergebnisse legen nahe, dass selbst sehr seltene Veränderungen im PD‑1‑Gen, sofern sie an entscheidenden Kontaktpunkten liegen, die Fähigkeit von Pembrolizumab verringern könnten, an sein Ziel anzudocken, und damit die Wirksamkeit bei der Aktivierung von T‑Zellen gegen Krebs abschwächen. Da die Arbeit rein rechnerisch ist und experimentelle sowie klinische Bestätigung benötigt, bietet sie dennoch eine Landkarte: Bestimmte PD‑1‑Varianten, etwa solche an den Positionen 85 und 89, könnten eines Tages als Biomarker dienen, um Patienten mit erhöhtem Resistenzrisiko zu identifizieren oder die Auswahl zwischen verschiedenen PD‑1‑gerichteten Wirkstoffen zu lenken. Allgemeiner zeigt die Studie, wie tiefgehende Computersimulationen die feingliedrigen molekularen Gründe beleuchten können, weshalb potente Immuntherapien bei manchen Menschen erfolgreich sind, bei anderen aber versagen.
Zitation: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Schlüsselwörter: PD‑1‑Mutationen, Pembrolizumab‑Resistenz, Krebsimmuntherapie, Immuncheckpoint‑Inhibitoren, Molekulardynamik‑Simulation