Clear Sky Science · pt
O impacto de mutações em PD-1 na ligação de pembrolizumabe: percepções a partir de dinâmica molecular e análise MM-GBSA
Por que isso importa para o tratamento do câncer
Drogas de imunoterapia como o pembrolizumabe transformaram o cuidado de muitos tipos de câncer, mas apenas uma fração dos pacientes se beneficia — e alguns que respondem inicialmente acabam tendo recaída. Este estudo faz uma pergunta focada por trás desse mistério clínico: o que acontece se ocorrerem mudanças sutis no PD-1, o “interruptor de desligar” do sistema imune que o pembrolizumabe foi projetado para bloquear? Ao usar simulações computacionais avançadas em vez de amostras de pacientes, os autores mapeiam como alterações genéticas raras no PD-1 podem enfraquecer ou fortalecer a afinidade do medicamento, oferecendo pistas sobre por que o tratamento às vezes falha e como testes ou fármacos futuros poderiam ser aprimorados.
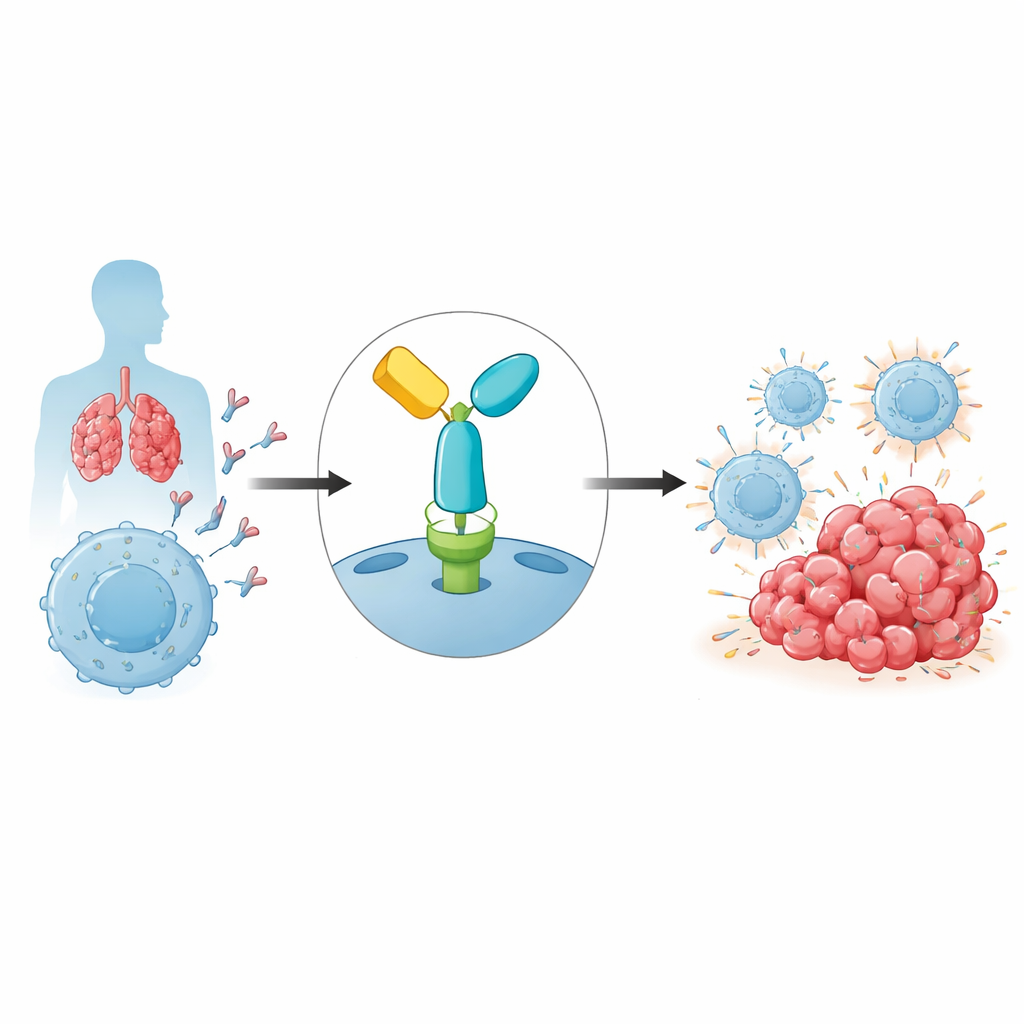
O freio imune que os tumores exploram
Nosso sistema imunológico depende de células T para reconhecer e atacar células anormais, incluindo as cancerosas. Para evitar danos colaterais, as células T carregam mecanismos de segurança chamados pontos de verificação imune. Um dos mais importantes é o PD-1, um receptor nas células T que, quando ativado por seu parceiro PD-L1 em outras células, reduz a atividade imune. Tumores frequentemente exploram essa via exibindo PD-L1, efetivamente dizendo às células T próximas para recuar. O pembrolizumabe é um anticorpo terapêutico que se liga ao PD-1 e bloqueia essa interação inibitória, reativando as células T para que possam atacar as células tumorais com mais eficácia. Embora essa estratégia tenha levado a remissões duradouras em cânceres como melanoma e câncer de pulmão, a resistência é comum e suas causas ainda estão sendo desvendadas.
Usando computadores como um microscópio molecular
Em vez de realizar experimentos de laboratório com células, os pesquisadores recorreram a modelos computacionais detalhados da proteína PD-1 complexada com o pembrolizumabe. Partiram de uma estrutura cristalográfica de alta resolução desse complexo e identificaram os pontos de contato chave — aminoácidos individuais no PD-1 que formam ligações de hidrogênio, contatos hidrofóbicos semelhantes a “graxa” ou pontes iônicas (salt bridges) com o anticorpo. Em seguida, usando simulações de dinâmica molecular, observaram como esses contatos se comportaram ao longo de 50 bilionésimos de segundo e calcularam quanto cada resíduo contribuía para manter o complexo intacto. Isso lhes permitiu identificar 16 posições “hot spot” no PD-1 que são especialmente importantes para uma ligação forte.
Mudanças genéticas raras com efeitos desproporcionais
Depois, a equipe pesquisou em um grande banco de dados de proteínas por alterações naturais (mutações) nessas posições hot spot e encontrou 40 variantes, mais uma mutação adicional relatada anteriormente por interromper a ligação do pembrolizumabe em testes de laboratório. Após filtrar variantes previstas para danificar a estrutura global do PD-1, restaram 28 mutações “provavelmente benignas” — alterações que deveriam deixar o PD-1 funcional, mas que podem alterar sutilmente como ele interage com fármacos. Para cada uma delas, construíram um modelo tridimensional do mutante e executaram o mesmo tipo de simulação de dinâmica molecular, seguida por um método de cálculo de energia (MM-GBSA) para estimar quão fortemente o pembrolizumabe se ligaria em comparação com a versão normal.
Quando âncoras chave são perdidas
As simulações revelaram que 23 das 28 mutações enfraqueceram a ligação do pembrolizumabe, algumas de forma bastante dramática, enquanto cinco a fortaleceram. Três mutações se destacaram por causar a maior perda prevista de afinidade: substituições nas posições 85 e 89 do PD-1 (Asp85Gly, Asp85Asn e Pro89Arg). Na proteína normal, Asp85 age como uma âncora eletrostática, formando uma ponte salina robusta e ligações de hidrogênio com uma arginina do anticorpo; Pro89 ajuda a formar um aglomerado de contatos hidrofóbicos encaixados com vários resíduos do anticorpo. As mutações em Asp85 removeram a carga negativa ou a capacidade de formar ligações de hidrogênio nesse sítio, efetivamente quebrando a âncora e desestabilizando a rede de contatos ao redor. A mudança Pro89Arg substituiu um resíduo neutro e adaptado em forma por um residu com carga positiva, perturbando o aglomerado hidrofóbico e reduzindo sua contribuição estabilizadora. Em contraste, algumas outras mutações em posições diferentes remodelaram sutilmente a interface de maneiras que poderiam aumentar a ligação, ao menos no modelo.
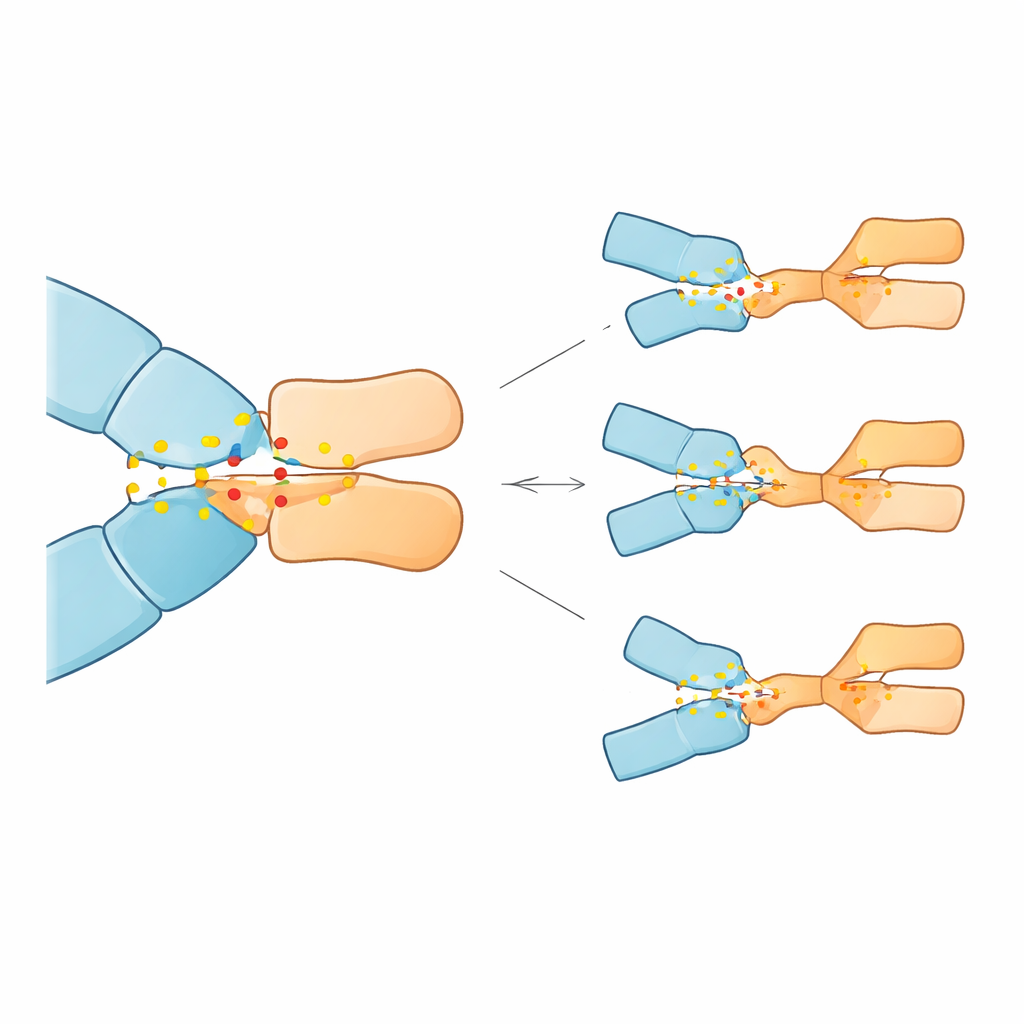
O que isso pode significar para os pacientes
Esses achados sugerem que mesmo mudanças muito raras no gene PD-1, se ocorrerem em pontos de contato cruciais, podem reduzir o quão bem o pembrolizumabe se liga ao seu alvo e, assim, diminuir sua capacidade de liberar as células T contra o câncer. Embora o trabalho seja inteiramente computacional e necessite de confirmação experimental e clínica, ele oferece um roteiro: variantes específicas de PD-1, como as nas posições 85 e 89, podem um dia servir como biomarcadores para identificar pacientes com maior risco de resistência ou para orientar a escolha entre diferentes fármacos que visam PD-1. Mais amplamente, o estudo ilustra como simulações computacionais aprofundadas podem iluminar as razões moleculares em detalhe por que imunoterapias potentes têm sucesso em algumas pessoas, mas falham em outras.
Citação: Bouricha, E.M., Hakmi, M., Batlamous, B. et al. The impact of PD-1 mutations on pembrolizumab binding: insights from molecular dynamics and MM-GBSA analysis. Sci Rep 16, 10773 (2026). https://doi.org/10.1038/s41598-026-45077-0
Palavras-chave: Mutações em PD-1, resistência ao pembrolizumabe, imunoterapia contra o câncer, inibidores de pontos de verificação imune, simulação de dinâmica molecular