Clear Sky Science · zh
宏观偏振成像识别与量化AGRO适配体和GK1肽在皮肤黑色素瘤预临床模型中抗血管生成作用
以新视角观察癌组织
癌症医生和病理学家仍然在很大程度上依赖显微镜下观察薄片组织来判断肿瘤的行为以及治疗是否有效。但这种目视检查速度慢、仅覆盖极小区域,且在一定程度上带有主观性。本研究引入了一种基于光学的成像方法,能够一次性扫描大块黑色素瘤组织切片,并自动区分富含血管的区域与密集肿瘤细胞区,为追踪新型抗癌疗法如何重塑肿瘤内部结构提供了一种更客观的手段。
为什么血管在黑色素瘤中很重要
黑色素瘤是最危险的皮肤癌类型,当其侵袭性生长并转移到全身时往往危及生命。为了实现这一点,肿瘤会建立自身的血管网络,这一过程称为血管生成。这些血管为肿瘤提供氧气和营养,并为癌细胞通往远处器官提供通道。因此,切断或重塑肿瘤血管的药物——即抗血管生成疗法——是癌症研究的重点。在这项工作中,作者在小鼠黑色素瘤模型中研究了两种实验性药物的联合治疗:一种名为AGRO的适配体和一种名为GK1的肽,两者均旨在破坏血供并削弱肿瘤。
把偏振光变成组织图谱
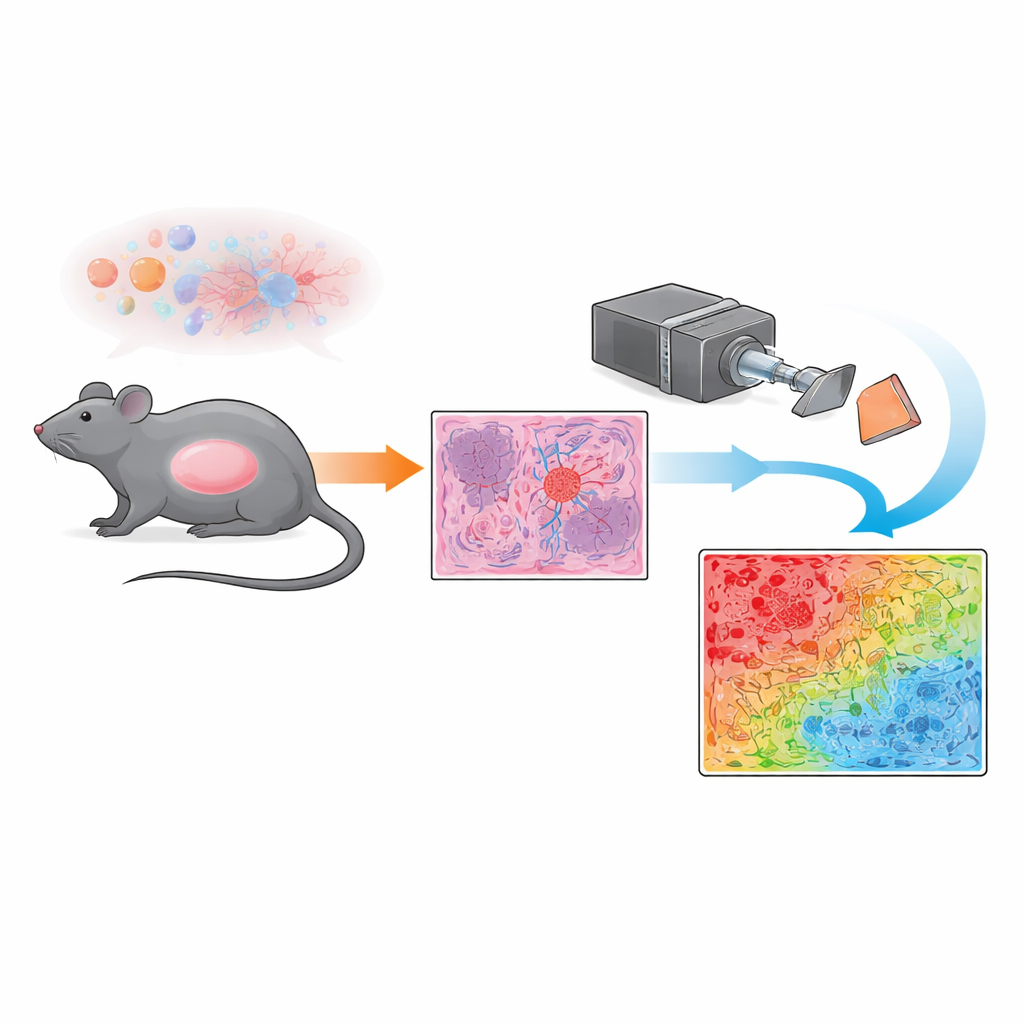
研究团队没有仅依赖常规显微镜,而是使用了一种称为穆勒偏振成像的技术。简单来说,他们将偏振光——在某一优选方向振动的光波——照射到染色的肿瘤切片上,并记录组织如何扰乱或保持这种偏振状态。肿瘤内部的不同结构,例如密集且无序的血管或较为均匀的肿瘤细胞簇,会以不同方式改变光的偏振。通过在大视场内对每个微小点的这些变化进行测量,系统生成了一张“去偏振指数”图,这是一种光学指纹,反映了每个像素处显微结构的有序或无序程度。
用颜色标识血管与肿瘤细胞
为了将这些光学指纹转化为病理学家能一目了然的图像,研究者开发了一个简单的逐像素分类方案。他们首先将偏振图与由资深病理学家审阅的高倍显微图像进行对比,侧重于明确以肿瘤细胞或不规则血管为主的区域。富含血管的区域表现出强烈的去偏振(对光的强烈搅动),而以肿瘤细胞为主的区域表现出较弱的去偏振(光通过较有序)。利用从这些参考区域得出的阈值,团队将每个像素分配到若干类别之一——强去偏振、弱去偏振、过渡或背景——并以彩色掩模覆盖在整个切片上。该方法使他们能够以平方毫米为单位量化每块肿瘤切片中由血管主导的组织、由肿瘤细胞主导的组织以及混合区域的面积。
在整个肿瘤范围内追踪治疗影响
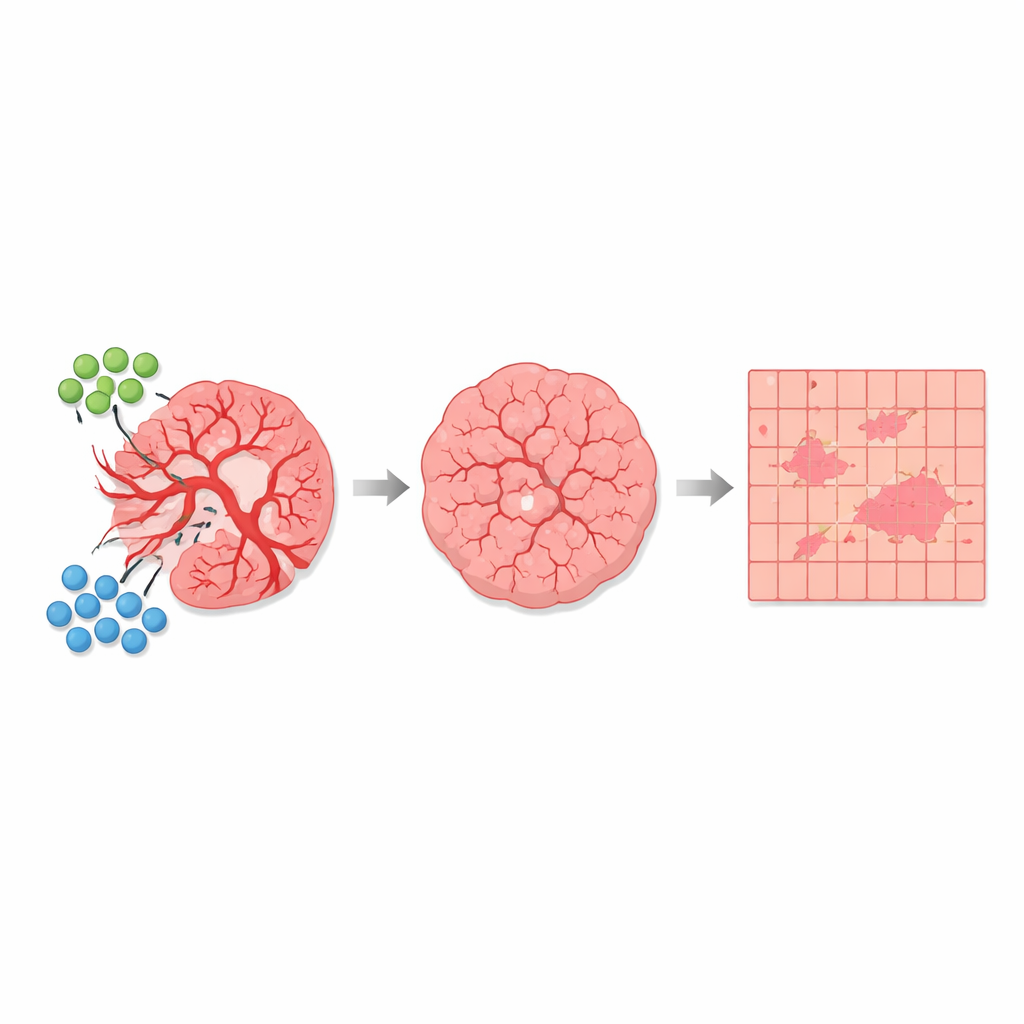
在建立该自动分割方法后,作者比较了未治疗小鼠与接受AGRO加GK1联合治疗小鼠的多块组织切片。在超过1700平方毫米的分析组织中,他们发现与血管相关的强去偏振区域总体上仅占约1%的面积——但不同组别之间这一比例明显不同。在未治疗的肿瘤中,血管主导的组织及其邻近的混合区域在切片中占比更大。经治疗的肿瘤中,这些高去偏振和过渡区域缩小,而主要由肿瘤细胞构成的弱去偏振区域相对增多。重要的是,各组织类型的基本光学“特征”保持不变;随疗法变化的是肿瘤属于各类别的面积比例,这与抗血管生成作用通过修剪血管并改变肿瘤微环境的结论相一致。
这对未来癌症护理的意义
对非专业读者来说,核心信息是这种偏振成像方法提供了一种广角、量化的肿瘤结构视图,是标准显微镜不易提供的。通过客观地计算肿瘤切片中血管与肿瘤细胞分别占据的面积,并在比典型显微视野大几十倍的区域上进行此类测量,该技术能敏感地检测抗血管生成疗法是否在减少肿瘤的血供。尽管这项工作是在黑色素瘤的小鼠预临床模型中完成的,但它指向了未来可能帮助研究人员并最终协助临床医生更快速、更一致地评估新型抗癌疗法的工具,作为对病理学家经验的补充——而非替代。
引用: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
关键词: 黑色素瘤, 肿瘤微环境, 偏振成像, 血管生成, 癌症治疗