Clear Sky Science · nl
Macroscopische polarimetrische discriminatie en kwantificering van het anti-angiogene effect van AGRO-aptame en GK1-peptide in een preklinisch melanoommodel
De kankertissue in een nieuw licht zien
Oncologen en pathologen vertrouwen nog steeds sterk op het bekijken van dunne weefselplakjes onder de microscoop om te bepalen hoe een tumor zich gedraagt en of een behandeling werkt. Maar deze visuele inspectie is traag, bestrijkt slechts kleine gebieden en kan deels subjectief zijn. Deze studie introduceert een lichtgebaseerde beeldvormingstechniek die grote stukken melanoomweefsel in één keer kan scannen en automatisch bloedvatrijke gebieden kan onderscheiden van zones vol tumorcellen, en zo een objectievere manier biedt om te volgen hoe nieuwe antikankerbehandelingen het interne landschap van de tumor herschikken.
Waarom bloedvaten belangrijk zijn bij melanoom
Melanoom, de gevaarlijkste vorm van huidkanker, wordt vaak levensbedreigend wanneer het agressief groeit en uitzaait door het lichaam. Om dat te doen bouwen tumoren hun eigen netwerk van bloedvaten, een proces dat bekendstaat als angiogenese. Deze vaten voorzien de tumor van zuurstof en voedingsstoffen en bieden ontsnappingsroutes voor kankercellen naar verre organen. Daarom zijn geneesmiddelen die de tumorbloedvaten afsluiten of herschikken—anti-angiogene therapieën—een belangrijk aandachtspunt in kankeronderzoek. In dit werk bestudeerden de auteurs een muismodel van melanoom dat behandeld werd met een combinatie van twee experimentele middelen, een aptame genaamd AGRO en een peptide genaamd GK1, beide ontworpen om de bloedtoevoer te verstoren en de tumor te verzwakken.
Gepolariseerd licht omzetten in een weefselkaart
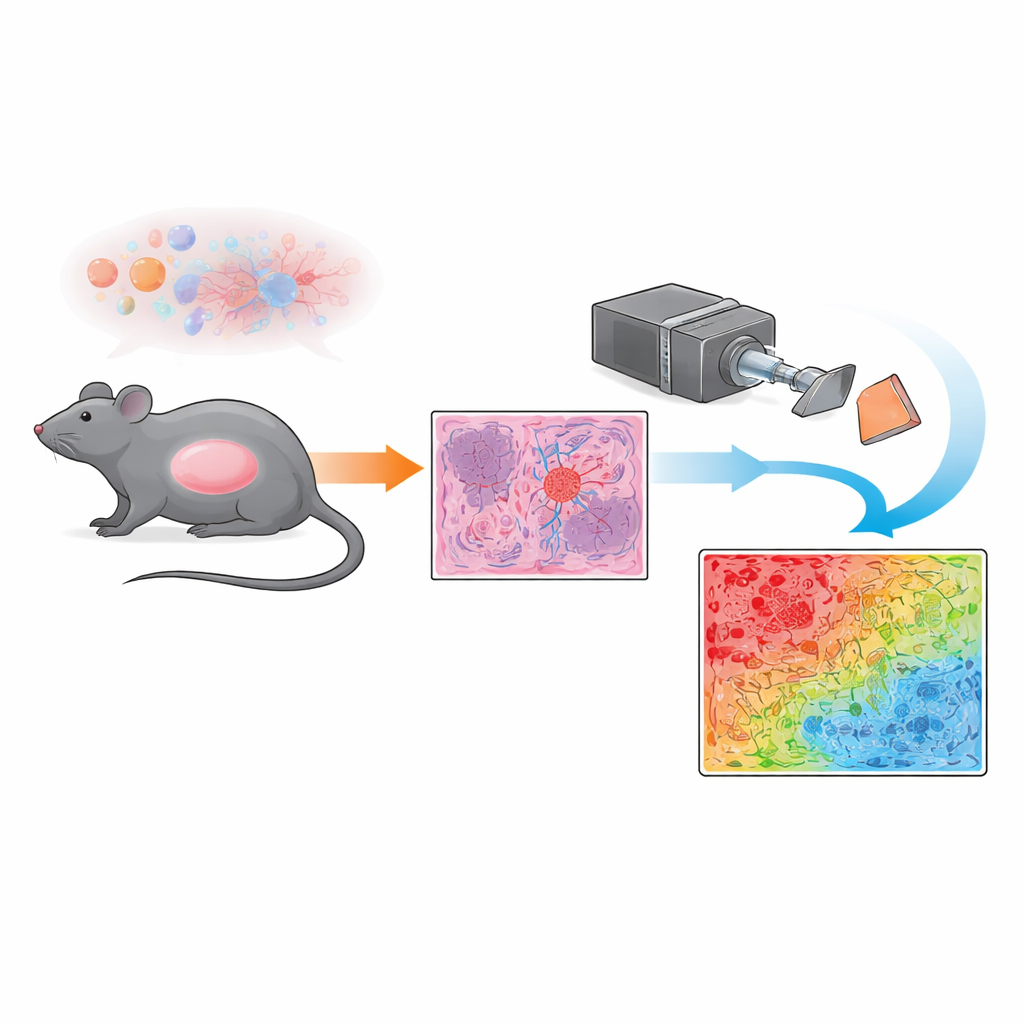
In plaats van alleen op conventionele microscopie te vertrouwen, gebruikte het team een techniek genaamd Mueller-polarimetrische beeldvorming. In eenvoudige bewoordingen laten ze gepolariseerd licht—lichtgolven die in een voorkeursrichting trillen—op gekleurde tumorplakjes schijnen en registreren hoe het weefsel die polarisatie verstrooit of behoudt. Verschillende structuren binnen de tumor, zoals dicht opeengepakte, wanordelijke bloedvaten of meer uniforme clusters van tumorcellen, verstoren het licht op verschillende manieren. Door deze veranderingen op elk klein punt over een groot gezichtsveld te meten, maakt het systeem een “depolarisatie-index” kaart, een soort optische vingerafdruk die weerspiegelt hoe geordend of ongeordend de microscopische structuur op elke pixel is.
Bloedvaten en tumorcellen met kleur coderen
Om deze optische vingerafdrukken in iets om te zetten dat een patholoog in één oogopslag kan interpreteren, ontwikkelden de onderzoekers een eenvoudige pixel-voor-pixel classificatiestrategie. Ze vergeleken eerst de polarimetrische kaarten met microscopische afbeeldingen bij hoge vergroting die door een expert-patholoog waren beoordeeld, met focus op goed gedefinieerde gebieden die gedomineerd werden door ofwel tumorcellen ofwel onregelmatige bloedvaten. Bloedvatrijke zones vertoonden sterke depolarisatie (sterke verstrooiing van het licht), terwijl door tumorcellen gedomineerde gebieden zwakkere depolarisatie lieten zien (ordelijker doorgang van het licht). Met drempelwaarden afgeleid van deze referentieregio’s kennde het team elke pixel toe aan een van meerdere categorieën—sterk depolariserend, zwak depolariserend, overgangsgebied of achtergrond—en toonden ze die als een kleurgecodeerd masker over hele secties. Met deze aanpak konden ze in vierkante millimeters kwantificeren hoeveel van elk tumorplakje bestond uit door vaten gedomineerd weefsel versus door tumorcellen gedomineerd weefsel en gemengde gebieden.
Het volgen van behandelimpact over de hele tumor
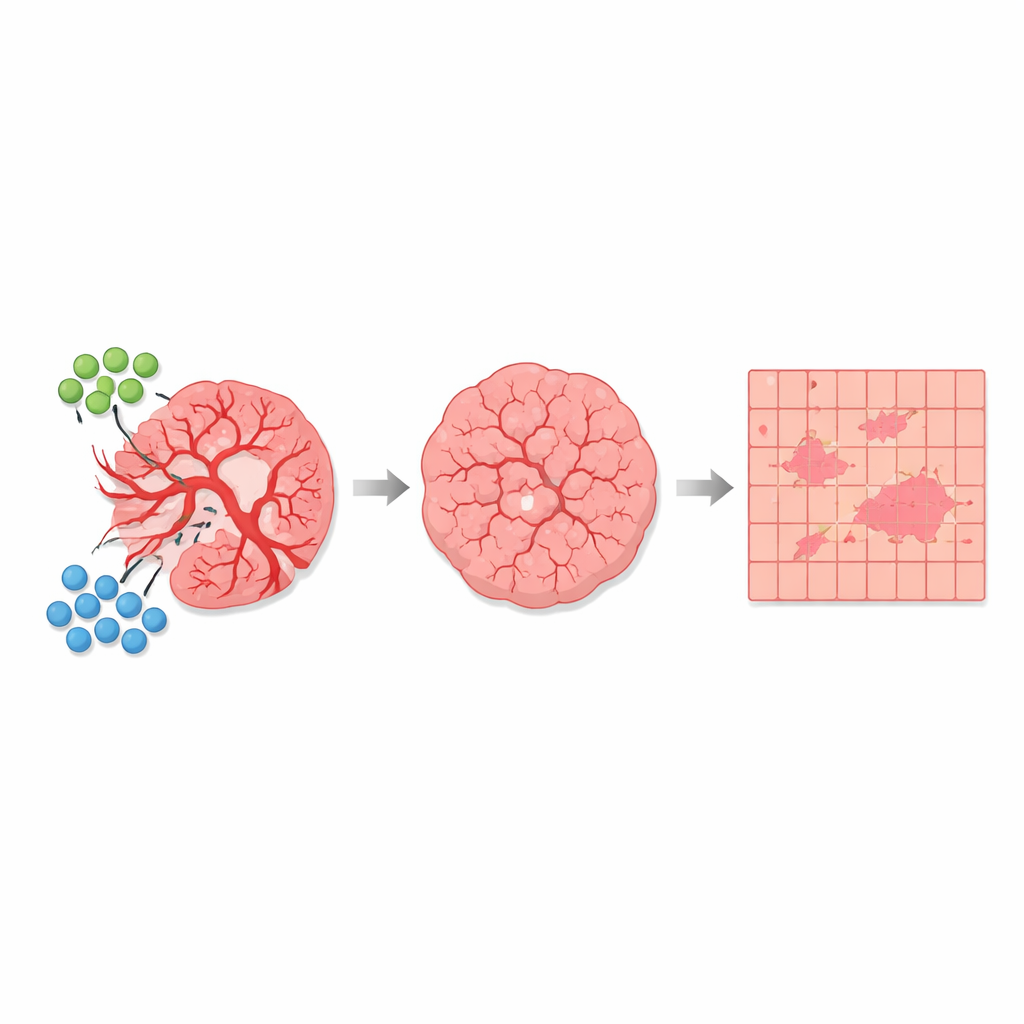
Met deze automatische segmentatie konden de auteurs veel weefselsecties vergelijken van onbehandelde muizen en van muizen behandeld met de combinatie AGRO plus GK1. Over meer dan 1.700 vierkante millimeter geanalyseerd weefsel ontdekten ze dat sterk depolariserende gebieden die geassocieerd zijn met bloedvaten slechts ongeveer 1 procent van het totale oppervlak in beslag namen—maar hun aandeel verschilde duidelijk tussen de groepen. In onbehandelde tumoren namen door bloedvaten gedomineerde weefsels en nabijgelegen gemengde zones een groter deel van het plakje in beslag. In behandelde tumoren krompen deze hoog-depolarisatie en overgangsgebieden, terwijl zwak depolariserende gebieden, hoofdzakelijk bestaande uit tumorcellen, relatief meer voorkwamen. Belangrijk is dat het basisoptische “handtekening” van elk weefseltype hetzelfde bleef; wat met therapie veranderde was hoeveel van de tumor tot elke categorie behoorde, in overeenstemming met een anti-angiogeen effect dat vaten snoeit en de tumormicro-omgeving verandert.
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat deze polarimetrische beeldvorming een breed, kwantitatief zicht op de tumorarchitectuur biedt dat standaardmicroscopen niet gemakkelijk geven. Door objectief te tellen hoeveel van een tumorplakje wordt ingenomen door bloedvaten versus tumorcellen, en dat te doen over gebieden tientallen keren groter dan een typisch microscoopveld, kan de techniek gevoelig detecteren of een anti-angiogene behandeling de bloedtoevoer naar de tumor vermindert. Hoewel het werk in een preklinisch muismodel van melanoom is uitgevoerd, wijst het op toekomstige hulpmiddelen die onderzoekers en uiteindelijk klinici kunnen helpen nieuwe kankertherapieën sneller en consistenter te evalueren, als aanvulling op—maar niet als vervanging van—het getrainde oog van de patholoog.
Bronvermelding: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Trefwoorden: melanoom, tumormicro-omgeving, polarimetrische beeldvorming, angiogenese, kankergeneeskunde