Clear Sky Science · pt
Discriminação e quantificação polarimétrica macroscópica do efeito antiangiogênico do aptâmero AGRO e do peptídeo GK1 em um modelo pré-clínico de melanoma
Vendo o tecido canceroso sob uma nova luz
Médicos oncologistas e patologistas ainda dependem fortemente da observação de lâminas finas de tecido ao microscópio para avaliar o comportamento de um tumor e se um tratamento está funcionando. Mas essa inspeção visual é lenta, abrange apenas áreas muito pequenas e pode ser relativamente subjetiva. Este estudo apresenta um método de imagem baseado em luz que pode escanear grandes porções de tecido de tumor de melanoma de uma só vez e distinguir automaticamente regiões ricas em vasos sanguíneos de áreas densas em células tumorais, oferecendo uma maneira mais objetiva de acompanhar como novos tratamentos anticâncer remodelam a paisagem interna do tumor.
Por que os vasos sanguíneos importam no melanoma
O melanoma, a forma mais perigosa de câncer de pele, frequentemente se torna fatal quando cresce de maneira agressiva e se dissemina pelo corpo. Para isso, os tumores constroem sua própria rede de vasos sanguíneos, um processo conhecido como angiogênese. Esses vasos alimentam o tumor com oxigênio e nutrientes e fornecem rotas de escape para células cancerosas atingirem órgãos distantes. Por essa razão, drogas que cortam ou remodelam os vasos tumorais — chamadas terapias antiangiogênicas — são foco importante da pesquisa oncológica. Neste trabalho, os autores estudaram um modelo murino de melanoma tratado com a combinação de dois agentes experimentais, um aptâmero chamado AGRO e um peptídeo denominado GK1, ambos projetados para interromper o suprimento sanguíneo e enfraquecer o tumor.
Transformando luz polarizada em um mapa do tecido
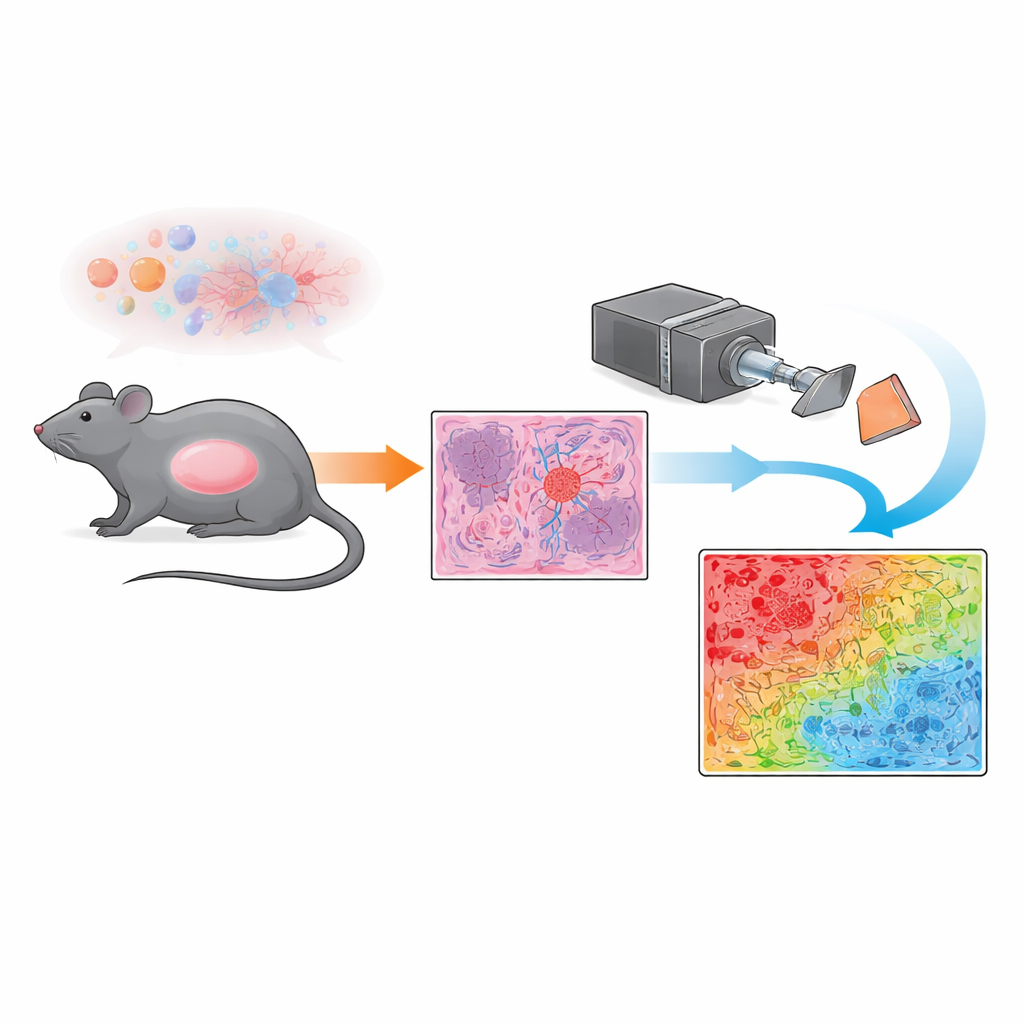
Em vez de depender apenas da microscopia convencional, a equipe utilizou uma técnica chamada imagem polarimétrica de Mueller. Em termos simples, eles iluminam fatias coradas do tumor com luz polarizada — ondas de luz que vibram em uma direção preferencial — e registram como o tecido embaralha ou preserva essa polarização. Estruturas distintas dentro do tumor, como vasos sanguíneos densos e desordenados ou aglomerados mais uniformes de células tumorais, perturbam a luz de maneiras diferentes. Ao medir essas mudanças em cada ponto minúsculo ao longo de um amplo campo de visão, o sistema produz um mapa do “índice de despolarização”, uma espécie de impressão óptica que reflete o grau de ordem ou desordem da estrutura microscópica em cada pixel.
Cores para diferenciar vasos e células tumorais
Para transformar essas impressões ópticas em algo que um patologista pudesse interpretar rapidamente, os pesquisadores desenvolveram um esquema simples de classificação pixel a pixel. Primeiro, eles compararam os mapas polarimétricos com imagens microscópicas de alta ampliação revisadas por um patologista experiente, concentrando-se em regiões bem definidas dominadas por células tumorais ou por vasos sanguíneos irregulares. Zonas ricas em vasos mostraram forte despolarização (grande embaralhamento da luz), enquanto áreas dominadas por células tumorais exibiram despolarização mais fraca (passagem da luz mais ordenada). Usando valores de limiar derivados dessas regiões de referência, a equipe classificou cada pixel em uma das categorias — fortemente despolarizante, fracamente despolarizante, transitória ou fundo — e as exibiu como uma máscara codificada por cores sobre seções inteiras. Essa abordagem permitiu quantificar, em milímetros quadrados, quanto de cada lâmina tumoral era composto por tecido dominado por vasos versus tecido dominado por células tumorais e áreas mistas.
Acompanhando o impacto do tratamento em todo o tumor
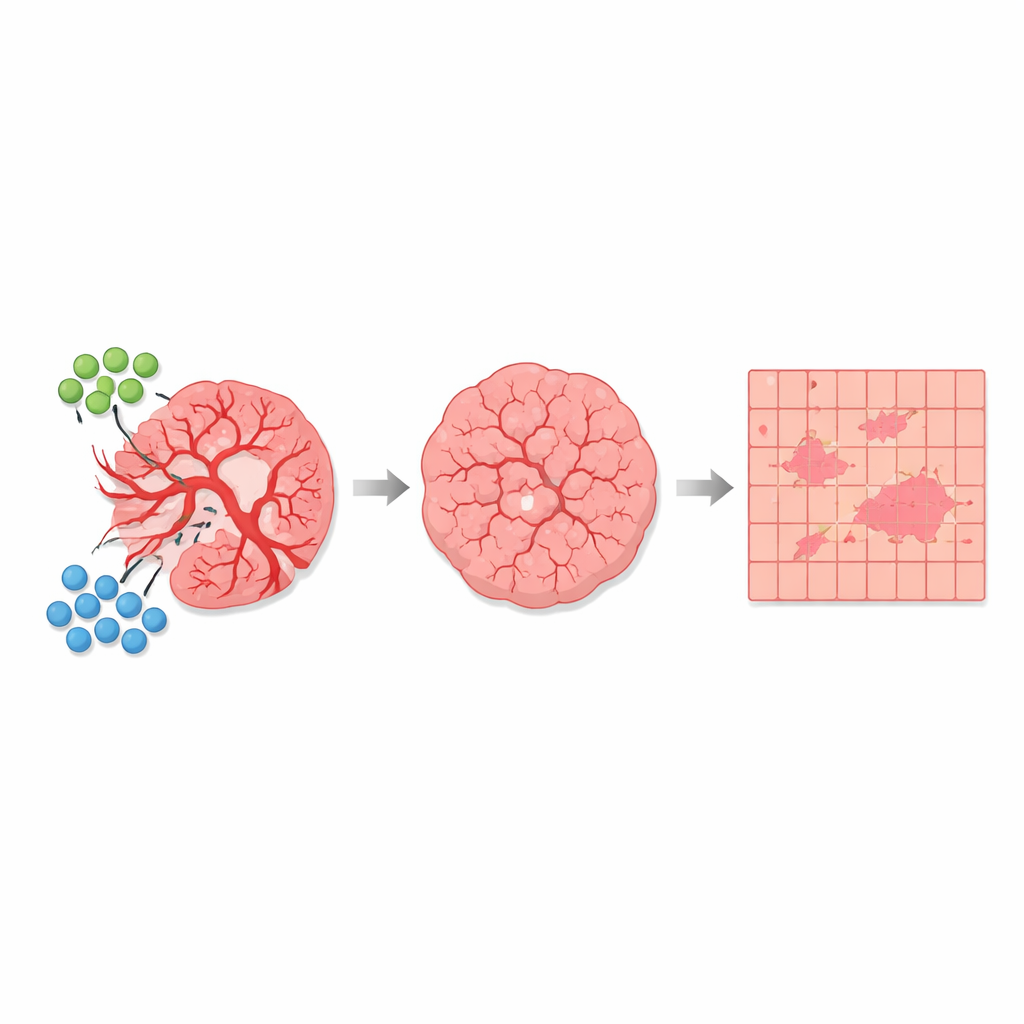
Com essa segmentação automática implementada, os autores compararam muitas seções de tecido de camundongos não tratados e de camundongos tratados com a combinação AGRO mais GK1. Em mais de 1.700 milímetros quadrados de tecido analisado, eles descobriram que as regiões fortemente despolarizantes, associadas a vasos sanguíneos, ocupavam apenas cerca de 1% da área total — mas sua proporção variou claramente entre os grupos. Em tumores não tratados, o tecido dominado por vasos e as zonas mistas próximas ocupavam uma fração maior da lâmina tumoral. Em tumores tratados, essas regiões de alta despolarização e as transitórias encolheram, enquanto as regiões fracamente despolarizantes, compostas principalmente por células tumorais, tornaram-se relativamente mais abundantes. Importante, a “assinatura” óptica básica de cada tipo de tecido permaneceu a mesma; o que mudou com a terapia foi a extensão do tumor pertencente a cada categoria, consistente com um efeito antiangiogênico que poda vasos e altera o microambiente tumoral.
O que isso significa para o futuro do cuidado contra o câncer
Para não especialistas, a mensagem principal é que esse método de imagem polarimétrica oferece uma visão ampla e quantitativa da arquitetura tumoral que os microscópios tradicionais não fornecem com facilidade. Ao contabilizar de forma objetiva quanto de uma lâmina tumoral é ocupado por vasos sanguíneos versus células tumorais, e fazendo isso em áreas dezenas de vezes maiores que um campo típico de microscópio, a técnica pode detectar com sensibilidade se um tratamento antiangiogênico está reduzindo o suprimento sanguíneo do tumor. Embora o trabalho tenha sido realizado em um modelo pré-clínico de melanoma em camundongo, ele aponta para ferramentas futuras que podem ajudar pesquisadores e, eventualmente, clínicos a avaliar novas terapias contra o câncer de forma mais rápida e consistente, complementando — mas não substituindo — o olhar treinado do patologista.
Citação: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Palavras-chave: melanoma, microambiente tumoral, imagem polarimétrica, angiogênese, terapia contra o câncer