Clear Sky Science · fr
Discrimination et quantification polarimétriques macroscopiques de l’effet anti‑angiogénique de l’aptamère AGRO et du peptide GK1 dans un modèle préclinique de mélanome
Voir les tissus cancéreux sous une nouvelle lumière
Les oncologues et les pathologistes s’appuient encore largement sur l’examen de coupes tissulaires minces au microscope pour évaluer le comportement d’une tumeur et l’efficacité d’un traitement. Mais cette inspection visuelle est lente, ne couvre que de très petites zones et peut être en partie subjective. Cette étude présente une méthode d’imagerie par la lumière capable de balayer en une fois de larges portions de tissu tumoral de mélanome et de distinguer automatiquement les régions riches en vaisseaux sanguins des zones compactes en cellules tumorales, offrant une manière plus objective de suivre comment de nouveaux traitements anticancéreux remodèlent le paysage interne de la tumeur.
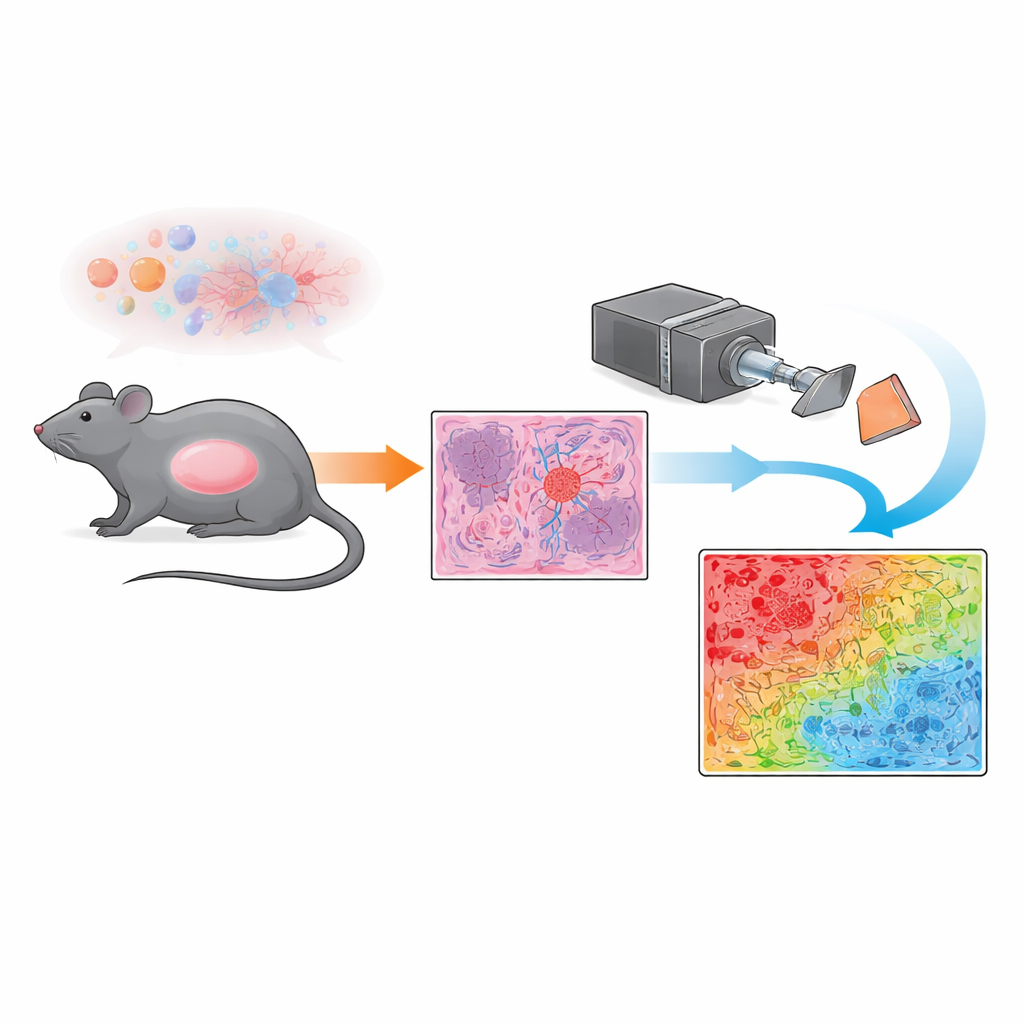
Pourquoi les vaisseaux sanguins comptent dans le mélanome
Le mélanome, la forme la plus agressive du cancer de la peau, devient souvent mortel lorsqu’il croît de façon agressive et se propage dans l’organisme. Pour ce faire, les tumeurs construisent leur propre réseau vasculaire, un processus appelé angiogenèse. Ces vaisseaux alimentent la tumeur en oxygène et en nutriments et offrent des voies de fuite pour les cellules cancéreuses vers des organes distants. C’est pourquoi les médicaments qui coupent ou remodèlent les vaisseaux tumoraux — les thérapies anti‑angiogéniques — sont au cœur de la recherche en oncologie. Dans ce travail, les auteurs ont étudié un modèle murin de mélanome traité par une combinaison de deux agents expérimentaux, un aptamère nommé AGRO et un peptide appelé GK1, tous deux conçus pour perturber l’apport sanguin et affaiblir la tumeur.
Transformer la lumière polarisée en carte tissulaire
Plutôt que de se fier uniquement à la microscopie conventionnelle, l’équipe a utilisé une technique appelée imagerie polarimétrique de Mueller. En termes simples, ils projettent une lumière polarisée — des ondes lumineuses vibrantes selon une direction privilégiée — sur des coupes tumorales colorées et enregistrent la manière dont le tissu désorganise ou préserve cette polarisation. Les différentes structures à l’intérieur de la tumeur, telles que des vaisseaux sanguins denses et désordonnés ou des amas plus uniformes de cellules tumorales, perturbent la lumière de façons distinctes. En mesurant ces changements à chaque point d’un grand champ de vue, le système produit une carte d’« indice de dépolarisation », une sorte d’empreinte optique qui reflète le degré d’ordre ou de désordre de la structure microscopique à chaque pixel.
Coder en couleurs les vaisseaux et les cellules tumorales
Pour rendre ces empreintes optiques interprétables d’un coup d’œil par un pathologiste, les chercheurs ont développé un schéma de classification simple pixel par pixel. Ils ont d’abord comparé les cartes polarimétriques avec des images microscopiques à fort grossissement examinées par un pathologiste expert, en se concentrant sur des régions bien délimitées dominées soit par des cellules tumorales, soit par des vaisseaux sanguins irréguliers. Les zones riches en vaisseaux montraient une forte dépolarisation (forte dispersion de la lumière), tandis que les régions dominées par les cellules tumorales présentaient une dépolarisation plus faible (passage de la lumière plus ordonné). À partir de valeurs seuils dérivées de ces régions de référence, l’équipe a attribué à chaque pixel une catégorie — fortement dépolarisant, faiblement dépolarisant, transitionnel ou fond — et les a affichées sous forme d’un masque coloré sur l’ensemble des sections. Cette approche leur a permis de quantifier, en millimètres carrés, la surface de chaque coupe tumorale occupée par du tissu dominé par les vaisseaux par rapport au tissu dominé par les cellules tumorales et aux zones mixtes.
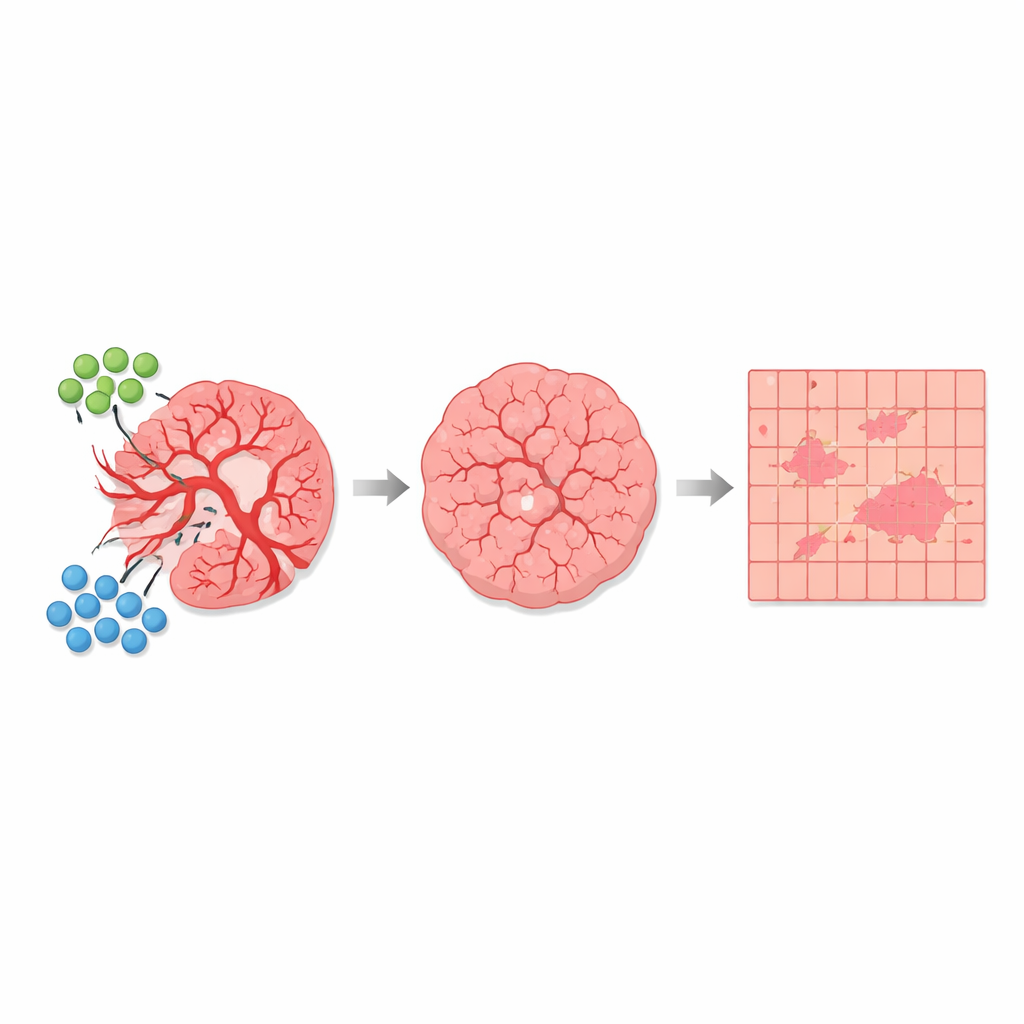
Suivre l’impact du traitement sur l’ensemble de la tumeur
Avec cette segmentation automatique en place, les auteurs ont comparé de nombreuses sections tissulaires provenant de souris non traitées et de souris traitées par la combinaison AGRO plus GK1. Sur plus de 1 700 millimètres carrés de tissu analysé, ils ont constaté que les régions fortement dépolarisantes associées aux vaisseaux occupaient en moyenne seulement environ 1 % de la surface totale — mais leur proportion variait nettement selon les groupes. Dans les tumeurs non traitées, le tissu dominé par les vaisseaux et les zones mixtes adjacentes occupaient une plus grande part de la coupe tumorale. Dans les tumeurs traitées, ces régions à forte dépolarisation et transitionnelles diminuaient, tandis que les régions faiblement dépolarisantes, principalement composées de cellules tumorales, devenaient relativement plus abondantes. Il est important de noter que la « signature » optique de base de chaque type de tissu restait la même ; ce qui changeait avec la thérapie était la part relative de la tumeur appartenant à chaque catégorie, cohérente avec un effet anti‑angiogénique qui élaguerait les vaisseaux et modifierait le microenvironnement tumoral.
Ce que cela signifie pour la prise en charge future du cancer
Pour les non‑spécialistes, le message clé est que cette méthode d’imagerie polarimétrique offre une vue large et quantitative de l’architecture tumorale que la microscopie standard ne fournit pas facilement. En quantifiant objectivement l’espace occupé par les vaisseaux par rapport aux cellules tumorales sur des zones des dizaines de fois plus grandes qu’un champ microscopique typique, la technique peut détecter avec sensibilité si un traitement anti‑angiogénique réduit l’apport sanguin de la tumeur. Bien que le travail ait été réalisé dans un modèle préclinique murin de mélanome, il ouvre la voie à des outils futurs qui pourraient aider les chercheurs et, éventuellement, les cliniciens à évaluer plus rapidement et plus systématiquement de nouveaux traitements anticancéreux, en complément — mais pas en remplacement — du regard expert du pathologiste.
Citation: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Mots-clés: mélanome, microenvironnement tumoral, imagerie polarimétrique, angiogenèse, thérapie anticancéreuse