Clear Sky Science · es
Discriminación y cuantificación polarimétrica macroscópica del efecto antiangiogénico del aptámero AGRO y el péptido GK1 en un modelo preclínico de melanoma
Ver el tejido canceroso con una nueva luz
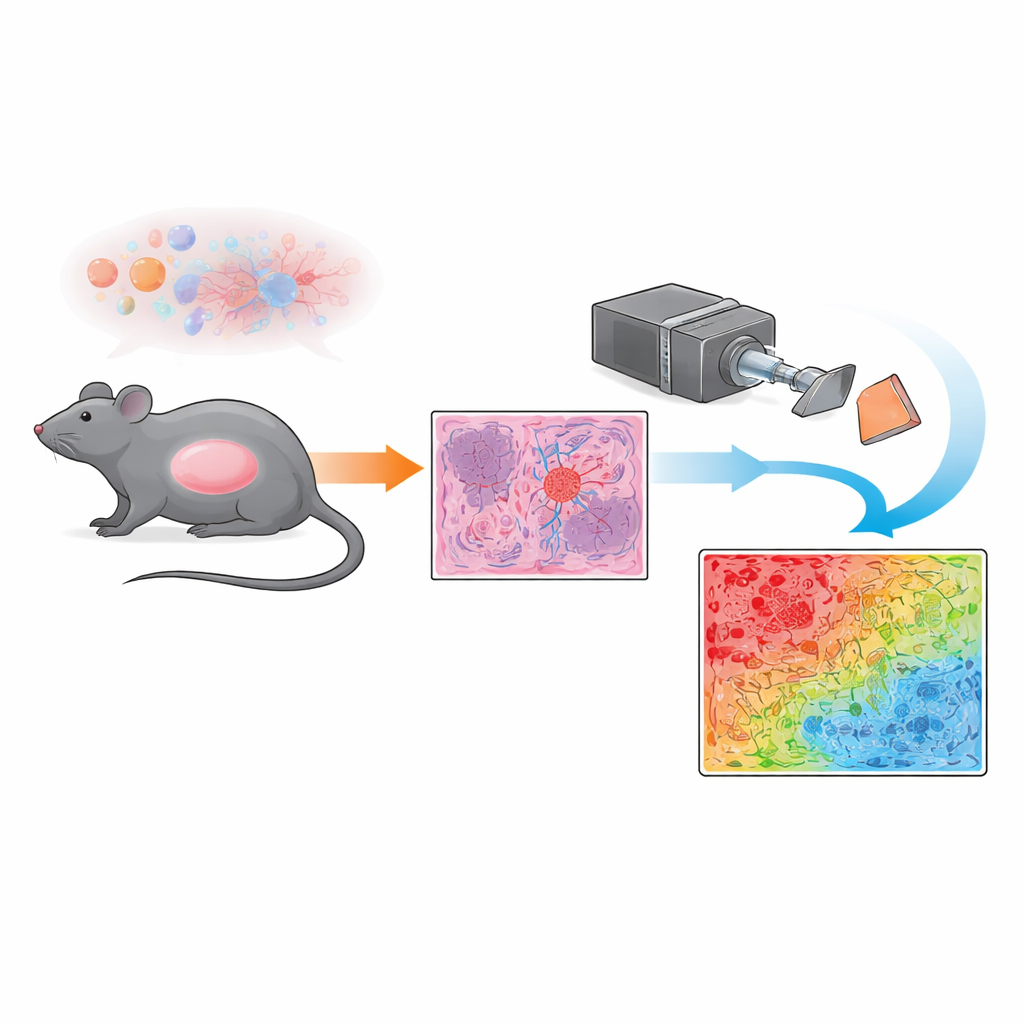
Los oncólogos y patólogos todavía dependen en gran medida de observar finas láminas de tejido al microscopio para juzgar el comportamiento de un tumor y si un tratamiento está funcionando. Pero esta inspección visual es lenta, cubre solo áreas muy pequeñas y puede ser algo subjetiva. Este estudio presenta un método de imágenes basado en la luz que puede escanear a la vez grandes fragmentos de tejido tumoral de melanoma y distinguir automáticamente las regiones ricas en vasos sanguíneos de las áreas densamente pobladas por células tumorales, ofreciendo una forma más objetiva de seguir cómo los nuevos tratamientos anticancerígenos remodelan el paisaje interno del tumor.
Por qué los vasos sanguíneos importan en el melanoma
El melanoma, la forma más peligrosa de cáncer de piel, suele volverse mortal cuando crece de forma agresiva y se disemina por el organismo. Para hacerlo, los tumores construyen su propia red de vasos sanguíneos, un proceso conocido como angiogénesis. Estos vasos alimentan el tumor con oxígeno y nutrientes y proporcionan rutas de escape para que las células cancerosas lleguen a órganos distantes. Por eso, los fármacos que cortan o remodelan los vasos tumorales —llamadas terapias antiangiogénicas— son un foco importante de la investigación oncológica. En este trabajo, los autores estudiaron un modelo murino de melanoma tratado con una combinación de dos agentes experimentales, un aptámero llamado AGRO y un péptido denominado GK1, ambos diseñados para interrumpir el suministro sanguíneo y debilitar el tumor.
Convertir luz polarizada en un mapa tisular
En lugar de depender únicamente de la microscopía convencional, el equipo utilizó una técnica llamada imagen polarimétrica de Mueller. En términos sencillos, proyectan luz polarizada —ondas de luz que vibran en una dirección preferente— sobre cortes teñidos del tumor y registran cómo el tejido revuelve o preserva esa polarización. Diferentes estructuras dentro del tumor, como vasos sanguíneos densos y desordenados o agregados más uniformes de células tumorales, alteran la luz de maneras distintas. Midiendo esos cambios en cada punto minúsculo a lo largo de un amplio campo de visión, el sistema genera un mapa de “índice de despolarización”, una especie de huella óptica que refleja cuánto ordenado o desordenado está la estructura microscópica en cada píxel.
Codificar en color vasos sanguíneos y células tumorales
Para transformar estas huellas ópticas en algo que un patólogo pudiera interpretar de un vistazo, los investigadores desarrollaron un esquema de clasificación simple píxel por píxel. Primero compararon los mapas polarimétricos con imágenes de microscopio a alta magnificación revisadas por un patólogo experto, centrándose en regiones bien definidas dominadas o bien por células tumorales o bien por vasos sanguíneos irregulares. Las zonas ricas en vasos mostraron una fuerte despolarización (gran revuelto de la luz), mientras que las áreas dominadas por células tumorales presentaron una despolarización más débil (paso de la luz más ordenado). Usando valores umbral derivados de estas regiones de referencia, el equipo asignó cada píxel a una de varias categorías —fuertemente despolarizante, débilmente despolarizante, de transición o fondo— y las mostraron como una máscara codificada por colores sobre secciones enteras. Este enfoque les permitió cuantificar, en milímetros cuadrados, cuánto de cada corte tumoral estaba compuesto por tejido dominado por vasos frente a tejido dominado por células tumorales y áreas mixtas.
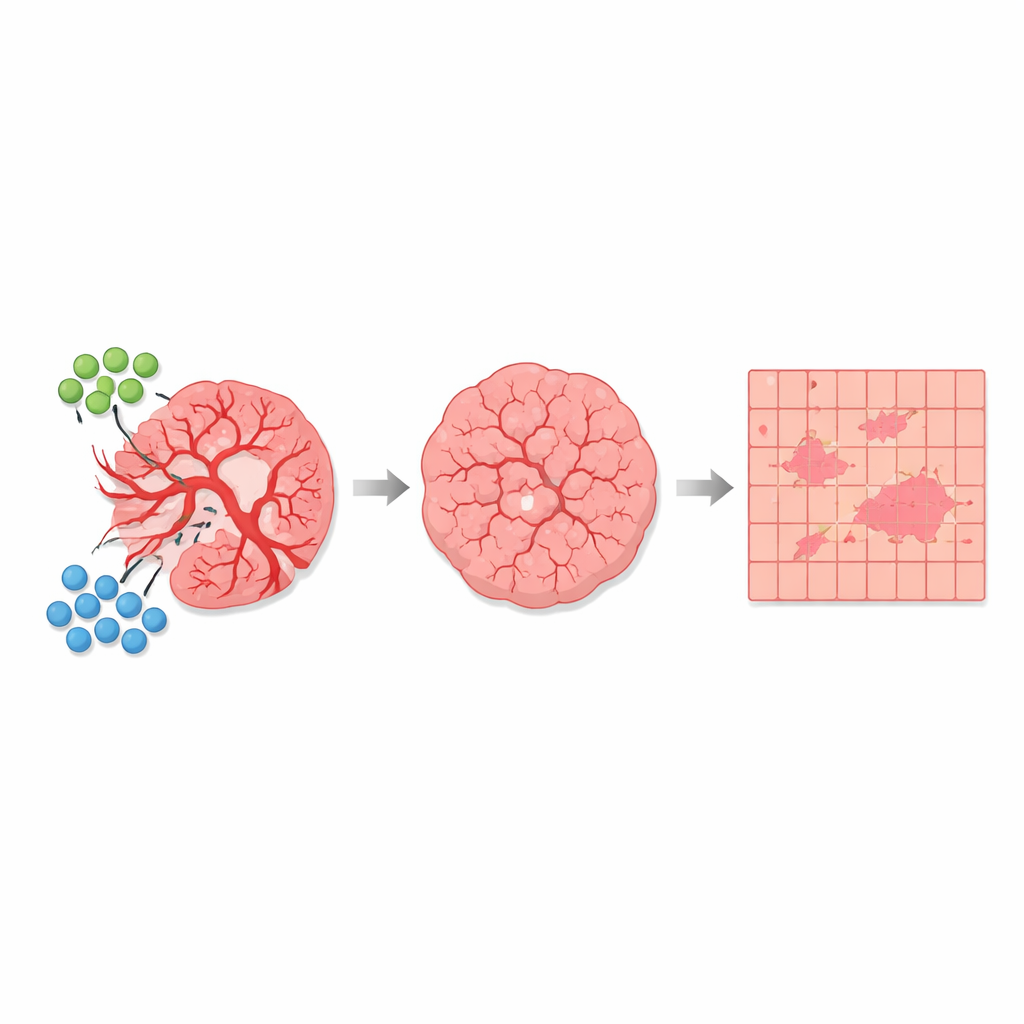
Rastrear el impacto del tratamiento en todo el tumor
Con esta segmentación automática, los autores compararon muchas secciones de tejido de ratones no tratados y de ratones tratados con la combinación AGRO más GK1. En más de 1.700 milímetros cuadrados de tejido analizado, encontraron que las regiones fuertemente despolarizantes asociadas con vasos sanguíneos ocupaban solo alrededor del 1 por ciento del área total en conjunto, pero su proporción difería claramente entre los grupos. En los tumores no tratados, el tejido dominado por vasos y las zonas mixtas cercanas ocupaban una fracción mayor del corte tumoral. En los tumores tratados, estas regiones de alta despolarización y de transición se redujeron, mientras que las regiones débilmente despolarizantes, compuestas principalmente por células tumorales, se hicieron relativamente más abundantes. Importante: la “firma” óptica básica de cada tipo de tejido se mantuvo; lo que cambió con la terapia fue la extensión de tumor perteneciente a cada categoría, coherente con un efecto antiangiogénico que poda vasos y altera el microambiente tumoral.
Qué significa esto para la futura atención del cáncer
Para quienes no son especialistas, el mensaje clave es que este método de imagen polarimétrica ofrece una vista amplia y cuantitativa de la arquitectura tumoral que los microscopios estándar no proporcionan fácilmente. Al contar objetivamente cuánto de un corte tumoral está ocupado por vasos frente a células tumorales, y haciéndolo sobre áreas decenas de veces mayores que un campo microscópico típico, la técnica puede detectar con sensibilidad si un tratamiento antiangiogénico está reduciendo el suministro de sangre al tumor. Aunque el trabajo se realizó en un modelo preclínico murino de melanoma, apunta hacia herramientas futuras que podrían ayudar a investigadores y, eventualmente, a clínicos a evaluar nuevas terapias contra el cáncer de forma más rápida y consistente, complementando —pero no reemplazando— la mirada experta del patólogo.
Cita: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Palabras clave: melanoma, microambiente tumoral, imagen polarimétrica, angiogénesis, terapia contra el cáncer