Clear Sky Science · sv
Makroskopisk polarimetrisk diskriminering och kvantifiering av den antiangiogena effekten av AGRO-aptamer och GK1-peptid i en preklinisk melanommodell
Att se cancertissue i nytt ljus
Cancerläkare och patologer förlitar sig fortfarande i stor utsträckning på att granska tunna vävnadsskivor i mikroskop för att avgöra hur en tumör beter sig och om en behandling fungerar. Men denna visuella inspektion är långsam, täcker bara mycket små områden och kan vara något subjektiv. I den här studien presenteras en ljusburen avbildningsmetod som kan skanna stora stycken melanomtumörvävnad samtidigt och automatiskt skilja blodkärlsrika områden från områden fyllda med tumörceller, vilket erbjuder ett mer objektivt sätt att följa hur nya antitumörbehandlingar omformar tumörens inre landskap.
Varför blodkärl spelar roll i melanom
Melanom, den farligaste formen av hudcancer, blir ofta livshotande när det växer aggressivt och sprider sig i kroppen. För att göra det bygger tumörer ett eget nätverk av blodkärl, en process som kallas angiogenes. Dessa kärl matar tumören med syre och näring och ger flyktvägar för cancerceller att nå avlägsna organ. På grund av detta är läkemedel som skär av eller omformar tumörens blodkärl — så kallade antiangiogena terapier — ett huvudfokus inom cancerforskningen. I detta arbete studerade författarna en musmodell av melanom som behandlades med en kombination av två experimentella agenter, en aptamer kallad AGRO och en peptid vid namn GK1, båda utformade för att störa blodförsörjningen och försvaga tumören.
Att omvandla polariserat ljus till en vävnadskarta
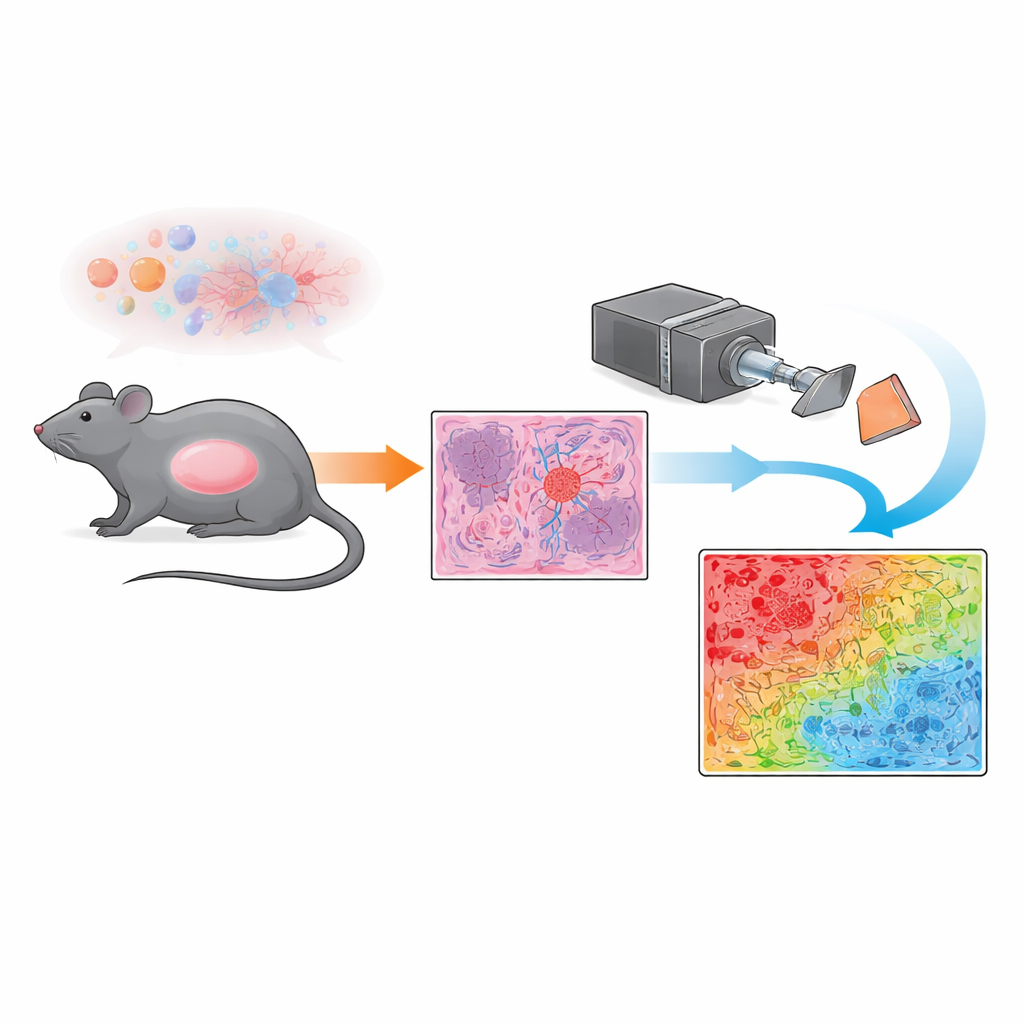
I stället för att enbart förlita sig på konventionell mikroskopi använde teamet en teknik kallad Mueller-polarimetrisk avbildning. Enkelt uttryckt belyser de de färgade tumörskivorna med polariserat ljus — ljusvågor som svänger i en föredragen riktning — och registrerar hur vävnaden rör om eller bevarar den polarisationen. Olika strukturer i tumören, såsom täta, oordnade blodkärl eller mer homogena kluster av tumörceller, påverkar ljuset på olika sätt. Genom att mäta dessa förändringar vid varje litet punkt över ett stort synfält producerar systemet en "depolarisationsindex"-karta, ett slags optiskt fingeravtryck som speglar hur ordnad eller oordnad den mikroskopiska strukturen är vid varje pixel.
Färgkodning av blodkärl och tumörceller
För att göra dessa optiska fingeravtryck tolkbara för en patolog utvecklade forskarna ett enkelt klassificeringsschema pixel för pixel. De jämförde först de polarimetriska kartorna med högförstorade mikroskopbilder granskade av en expertpatolog, med fokus på välavgränsade områden dominerade antingen av tumörceller eller av oregelbundna blodkärl. Blodkärlsrika zoner visade stark depolarisation (stor omrörning av ljuset), medan områden dominerade av tumörceller uppvisade svagare depolarisation (mer ordnad passage av ljuset). Med hjälp av tröskelvärden hämtade från dessa referensområden tilldelade teamet varje pixel till en av flera kategorier — starkt depolariserande, svagt depolariserande, övergångs- eller bakgrund — och visade dem som en färgkodad mask över hela sektioner. Detta tillvägagångssätt gjorde det möjligt för dem att kvantifiera, i kvadratmillimeter, hur stor del av varje tumörskiva som bestod av kärldominerad vävnad respektive tumörcellsdominerad vävnad och blandade områden.
Att spåra behandlingseffekt över hela tumören
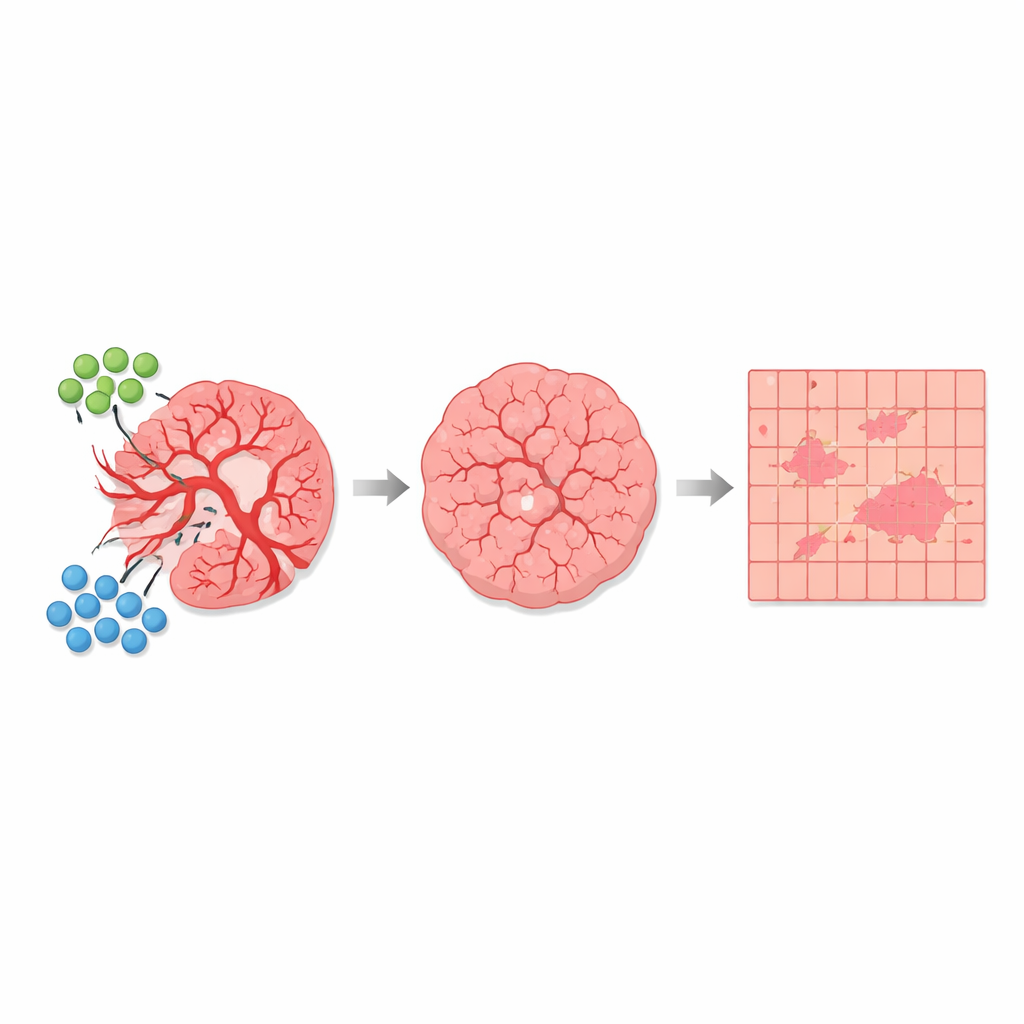
Med denna automatiska segmentering på plats jämförde författarna många vävnadssektioner från obehandlade möss och från möss behandlade med AGRO plus GK1-kombinationen. Över mer än 1 700 kvadratmillimeter analyserad vävnad fann de att starkt depolariserande områden associerade med blodkärl utgjorde bara omkring 1 procent av den totala ytan — men deras andel skiljde sig tydligt mellan grupperna. I obehandlade tumörer upptog kärldominerad vävnad och intilliggande blandzoner en större del av tumörskivan. I behandlade tumörer krympte dessa hög-depolarisations- och övergångsområden, medan svagt depolariserande områden, främst bestående av tumörceller, blev relativt mer omfattande. Viktigt är att varje vävnadstyps grundläggande optiska "signatur" förblev densamma; det som förändrades med terapin var hur stor del av tumören som tillhörde varje kategori, i linje med en antiangiogen effekt som beskär kärl och förändrar tumörmikromiljön.
Vad detta betyder för framtida cancervård
För icke-specialister är huvudbudskapet att denna polarimetriska avbildningsmetod erbjuder en vidvinkel, kvantitativ bild av tumörarkitekturen som standardmikroskop inte lätt kan ge. Genom att objektivt räkna hur stor del av en tumörskiva som upptas av blodkärl kontra tumörceller, och göra det över områden som är tiotals gånger större än ett typiskt mikroskopfält, kan tekniken känsligt upptäcka om en antiangiogen behandling minskar tumörens blodförsörjning. Även om arbetet utfördes i en preklinisk musmodell av melanom pekar det mot framtida verktyg som kan hjälpa forskare och så småningom kliniker att utvärdera nya cancerterapier snabbare och mer konsekvent, som ett komplement till — men inte en ersättning för — patologens tränade öga.
Citering: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Nyckelord: melanom, tumörmikromiljö, polarimetrisk avbildning, angiogenes, cancerbehandling