Clear Sky Science · de
Makroskopische polarimetrische Unterscheidung und Quantifizierung der antiangiogenen Wirkung des AGRO-Aptamers und des GK1-Peptids in einem präklinischen Melanom-Modell
Krebsgwebe in neuem Licht sehen
Onkologen und Pathologen verlassen sich nach wie vor stark darauf, dünne Gewebeschnitte unter dem Mikroskop zu betrachten, um einzuschätzen, wie sich ein Tumor verhält und ob eine Behandlung wirkt. Diese visuelle Inspektion ist jedoch zeitaufwendig, erfasst nur winzige Bereiche und kann subjektiv sein. Diese Studie stellt eine lichtbasierte Bildgebungsmethode vor, die große Stücke von Melanomgewebe gleichzeitig abtasten und automatisch gefäßreiche Regionen von Bereichen unterscheiden kann, die dicht von Tumorzellen besetzt sind. So entsteht eine objektivere Möglichkeit, nachzuvollziehen, wie neue Krebstherapien die innere Struktur des Tumors verändern.
Warum Blutgefäße beim Melanom wichtig sind
Das Melanom, die gefährlichste Form von Hautkrebs, wird oft lebensbedrohlich, wenn es aggressiv wächst und metastasiert. Dafür bauen Tumoren ein eigenes Netzwerk aus Blutgefäßen auf — ein Prozess, der als Angiogenese bezeichnet wird. Diese Gefäße versorgen den Tumor mit Sauerstoff und Nährstoffen und bieten Fluchtwege für Krebszellen, um entfernte Organe zu erreichen. Daher sind Wirkstoffe, die die Tumorblutgefäße abschneiden oder umbauen — sogenannte antiangiogene Therapien — ein zentrales Forschungsthema in der Onkologie. In dieser Arbeit untersuchten die Autoren ein Mausmodell des Melanoms, das mit einer Kombination aus zwei experimentellen Wirkstoffen behandelt wurde: einem Aptamer namens AGRO und einem Peptid namens GK1, die beide darauf abzielen, die Blutversorgung zu stören und den Tumor zu schwächen.
Polarisiertes Licht in eine Gewebekarte verwandeln
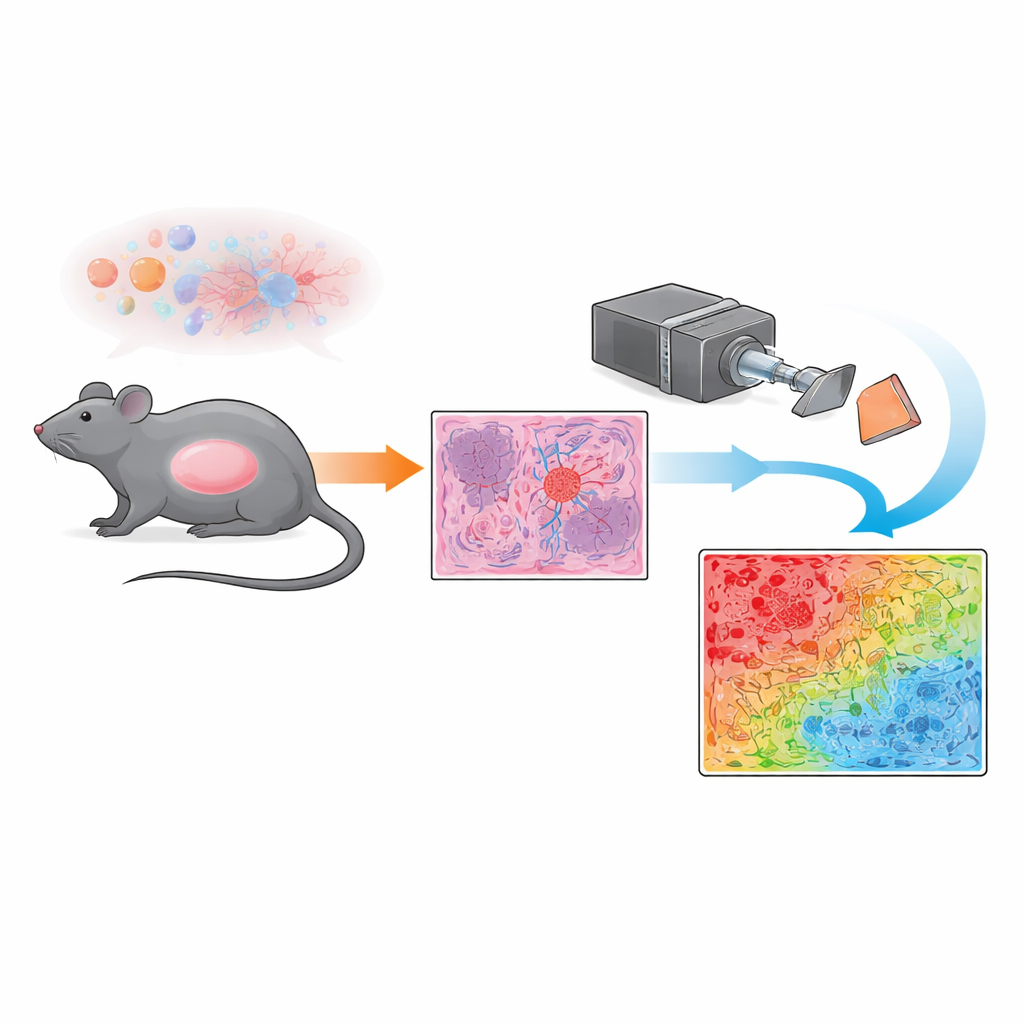
Statt sich nur auf konventionelle Mikroskopie zu stützen, verwendete das Team eine Technik namens Mueller-Polarimetrie. Einfach ausgedrückt, bestrahlen sie gefärbte Tumorschnitte mit polarisiertem Licht — Lichtwellen, die in einer bevorzugten Richtung schwingen — und zeichnen auf, wie das Gewebe diese Polarisation verwirbelt oder erhält. Verschiedene Strukturen im Tumor, etwa dichte, ungeordnete Blutgefäße oder gleichmäßigere Zellverbände, stören das Licht auf unterschiedliche Weise. Indem diese Veränderungen an jedem winzigen Punkt über ein großes Sichtfeld gemessen werden, erzeugt das System eine Karte des „Depolarisationsindex“, eine optische Signatur, die widerspiegelt, wie geordnet oder ungeordnet die mikroskopische Struktur an jedem Pixel ist.
Blutgefäße und Tumorzellen farbcodiert darstellen
Um diese optischen Fingerabdrücke für Pathologen schnell interpretierbar zu machen, entwickelten die Forschenden ein einfaches Pixel-für-Pixel-Klassifikationsschema. Zunächst verglichen sie die polarimetrischen Karten mit hochauflösenden Mikroskopaufnahmen, die von einem erfahrenen Pathologen bewertet wurden, und konzentrierten sich auf klar definierte Regionen, die entweder von Tumorzellen oder von unregelmäßigen Blutgefäßen dominiert waren. Gefäßreiche Zonen zeigten starke Depolarisation (starkes Verwürfeln des Lichts), während Gebiete, die hauptsächlich aus Tumorzellen bestanden, schwächere Depolarisation aufwiesen (ordnungsgemäßere Lichtdurchlässigkeit). Anhand von Schwellenwerten, die aus diesen Referenzregionen abgeleitet wurden, ordnete das Team jedes Pixel einer von mehreren Kategorien zu — stark depolarisierend, schwach depolarisierend, Übergangsbereich oder Hintergrund — und stellte sie als farbcodierte Maske über die gesamten Schnitte dar. Auf diese Weise konnten sie in Quadratmillimetern quantifizieren, wie viel jeder Tumorschnitt aus gefäßdominiertem Gewebe, tumorzelldominiertem Gewebe oder gemischten Bereichen bestand.
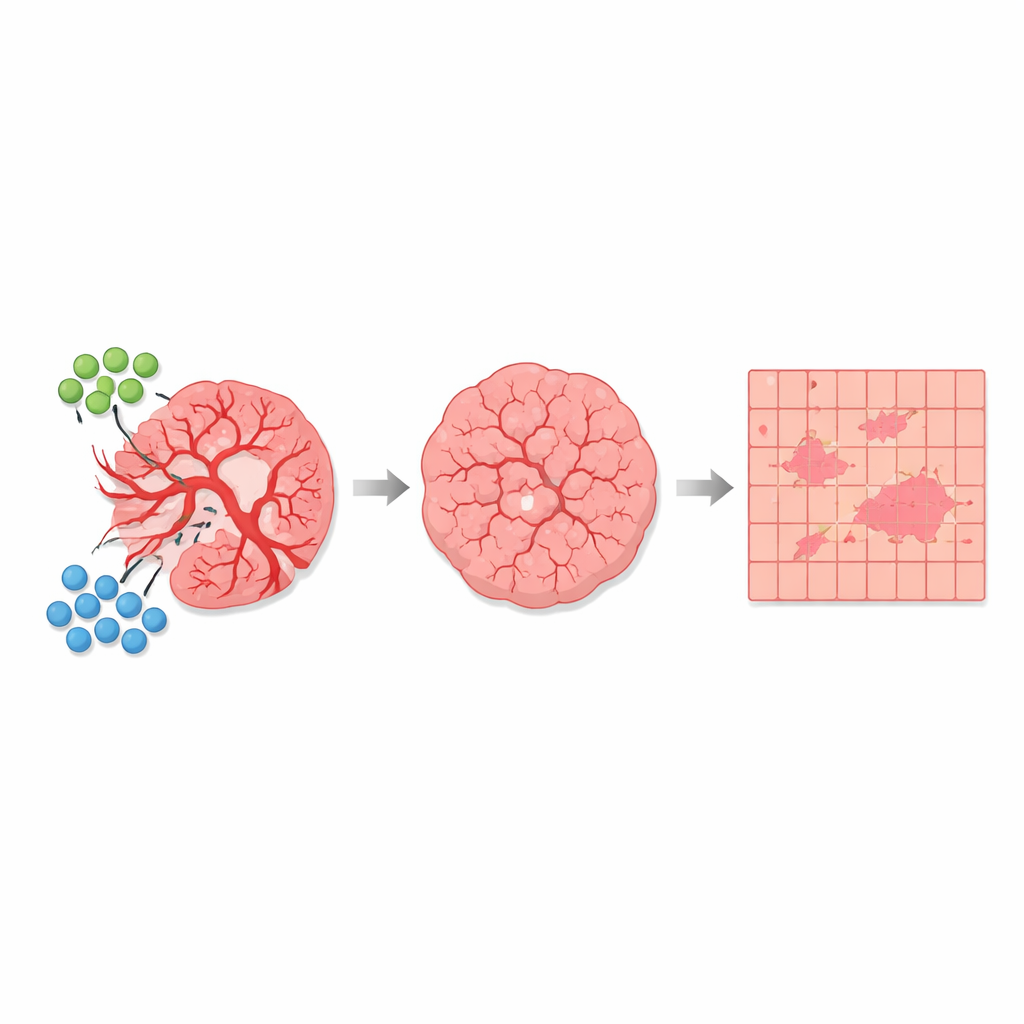
Die Wirkung der Behandlung im ganzen Tumor verfolgen
Mithilfe dieser automatischen Segmentierung verglichen die Autoren zahlreiche Gewebeschnitte aus unbehandelten Mäusen mit solchen aus Mäusen, die die Kombination AGRO plus GK1 erhielten. Über mehr als 1.700 Quadratmillimeter analysiertes Gewebe stellten sie fest, dass stark depolarisierende Regionen, die mit Blutgefäßen assoziiert sind, insgesamt nur etwa 1 Prozent der Fläche einnahmen — ihre Anteile unterschieden sich jedoch deutlich zwischen den Gruppen. In unbehandelten Tumoren nahmen gefäßdominierte Gewebeareale und angrenzende Mischzonen einen größeren Anteil der Schnitte ein. In behandelten Tumoren schrumpften diese stark depolarisierenden und Übergangsbereiche, während schwach depolarisierende Bereiche, überwiegend bestehend aus Tumorzellen, relativ häufiger wurden. Wichtig ist, dass die grundlegende optische „Signatur“ jeder Gewebeart gleich blieb; die Therapie veränderte vor allem den Anteil des Tumors, der zu jeder Kategorie gehörte, was mit einem antiangiogenen Effekt übereinstimmt, der Gefäße zurückbildet und die Tumormikroumgebung verändert.
Was das für die zukünftige Krebsversorgung bedeutet
Für Nicht-Fachleute ist die Kernbotschaft, dass diese polarimetrische Bildgebung einen großflächigen, quantitativen Blick auf die Tumorarchitektur bietet, den Standardmikroskope nicht leicht leisten. Indem sie objektiv zählen, wie viel eines Tumorschnitts von Blutgefäßen gegenüber Tumorzellen eingenommen wird — und das über Flächen, die um ein Vielfaches größer sind als ein typisches Mikroskopfeld — kann die Technik sensibel nachweisen, ob eine antiangiogene Behandlung die Blutversorgung des Tumors reduziert. Obwohl die Arbeit in einem präklinischen Mausmodell des Melanoms durchgeführt wurde, deutet sie auf künftige Werkzeuge hin, die Forschern und schließlich auch Klinikerinnen und Klinikern helfen könnten, neue Krebstherapien schneller und konsistenter zu bewerten und damit die Arbeit des Pathologen zu ergänzen, aber nicht zu ersetzen.
Zitation: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Schlüsselwörter: Melanom, Tumormikroumgebung, polarimetrische Bildgebung, Angiogenese, Krebstherapie