Clear Sky Science · tr
AGRO aptameri ve GK1 peptidinin preklinik melanom modelinde antianjiyogenik etkisinin makroskobik polarimetrik ayırımı ve nicelenmesi
Kanser Dokusunu Yeni Bir Işıkta Görmek
Onkologlar ve patologlar hâlâ bir tümörün nasıl davrandığını ve bir tedavinin işe yarayıp yaramadığını değerlendirmek için ince doku kesitlerine mikroskop altında bakmaya büyük ölçüde güveniyor. Ancak bu görsel inceleme yavaş, yalnızca çok küçük alanları kapsıyor ve bir dereceye kadar sübjektif olabilir. Bu çalışma, büyük melanom doku parçalarını aynı anda tarayabilen ve kan damarları açısından zengin bölgeleri tümör hücreleriyle dolu alanlardan otomatik olarak ayıran, yeni antikanser tedavilerin tümörün iç yapısını nasıl yeniden şekillendirdiğini daha nesnel biçimde izlemeyi sağlayan bir ışık tabanlı görüntüleme yöntemi sunuyor.
Melanomda Kan Damarlarının Önemi
En tehlikeli cilt kanseri türü olan melanom, agresif şekilde büyüyüp vücuda yayıldığında hayatı tehdit edici hale gelir. Bunu başarmak için tümörler anjiyogenez olarak adlandırılan, kendi kan damarları ağlarını kurarlar. Bu damarlar tümörü oksijen ve besinle besler ve kanser hücrelerinin uzak organlara ulaşması için kaçış yolları sağlar. Bu yüzden tümör damarlarını kesen veya yeniden düzenleyen ilaçlar — antianjiyogenik tedaviler — kanser araştırmalarının önemli bir odağıdır. Bu çalışmada yazarlar, kan tedarikini bozmayı ve tümörü zayıflatmayı amaçlayan AGRO adlı bir aptamer ile GK1 adlı bir peptidin kombinasyonuyla tedavi edilen bir fare melanom modelini incelediler.
Polarize Işığı Doku Haritasına Çevirmek
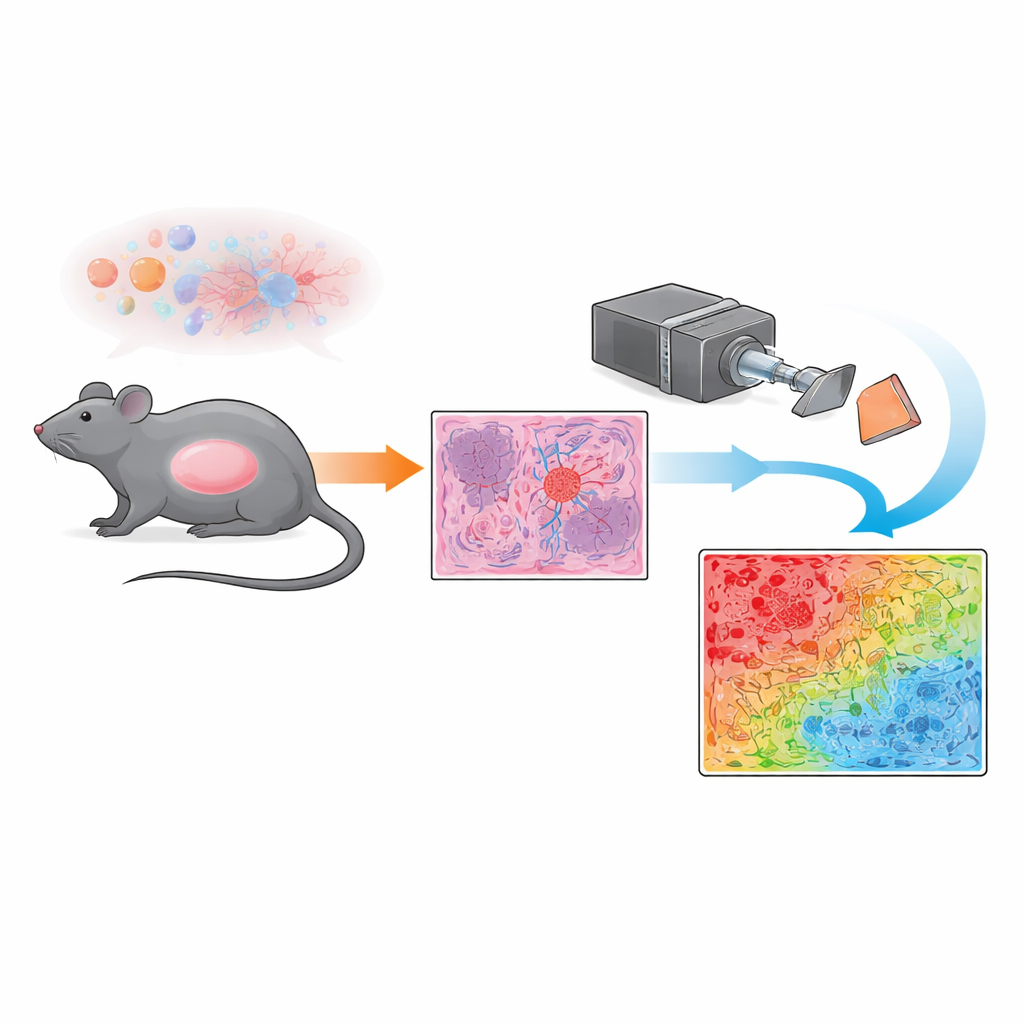
Geleneksel mikroskopiye yalnızca güvenmek yerine ekip, Mueller polarimetrik görüntüleme adlı bir teknik kullandı. Basitçe söylemek gerekirse, boyanmış tümör kesitlerine tercih edilen yönde titreşen polarize ışık tutuyorlar ve dokunun bu polarizasyonu nasıl karıştırdığını veya koruduğunu kaydediyorlar. Tümör içindeki farklı yapılar—yoğun, düzensiz kan damarları veya daha homojen tümör hücresi kümeleri gibi—ışığı farklı biçimlerde bozar. Geniş görüş alanı boyunca her küçük noktada bu değişiklikleri ölçerek sistem, her pikselde mikroskobik yapının ne kadar düzenli veya düzensiz olduğuna karşılık gelen bir tür optik parmak izi olan “depolarizasyon indeksi” haritası üretiyor.
Kan Damarlarını ve Tümör Hücrelerini Renk Kodlamak
Bu optik parmak izlerini bir patologun bakışta yorumlayabileceği bir şeye dönüştürmek için araştırmacılar basit bir piksel bazlı sınıflandırma şeması geliştirdiler. Önce polarimetrik haritaları, iyi tanımlanmış olarak ya tümör hücrelerinin ya da düzensiz kan damarlarının hakim olduğu bölgeleri odaklayan bir uzman patolog tarafından incelenmiş yüksek büyütmeli mikroskop görüntüleriyle karşılaştırdılar. Kan damarı açısından zengin bölgeler güçlü depolarizasyon (ışığın şiddetli karışması) gösterirken, tümör hücrelerinin hakim olduğu alanlar daha zayıf depolarizasyon (ışığın daha düzenli geçişi) gösterdi. Bu referans bölgelerden türetilen eşik değerlerini kullanarak ekip, her pikseli güçlü depolarize eden, zayıf depolarize eden, geçişsel veya arka plan gibi birkaç kategoriden birine atadı ve tüm kesitler üzerinde renk kodlu bir maske olarak görüntüledi. Bu yaklaşım, her bir tümör kesitinin milimetre kare cinsinden ne kadarının damar-dominant doku, ne kadarının tümör-hücresi–dominant doku ve karışık alanlardan oluştuğunu nicelendirilebilmesini sağladı.
Tüm Tümör Boyunca Tedavi Etkisini İzlemek
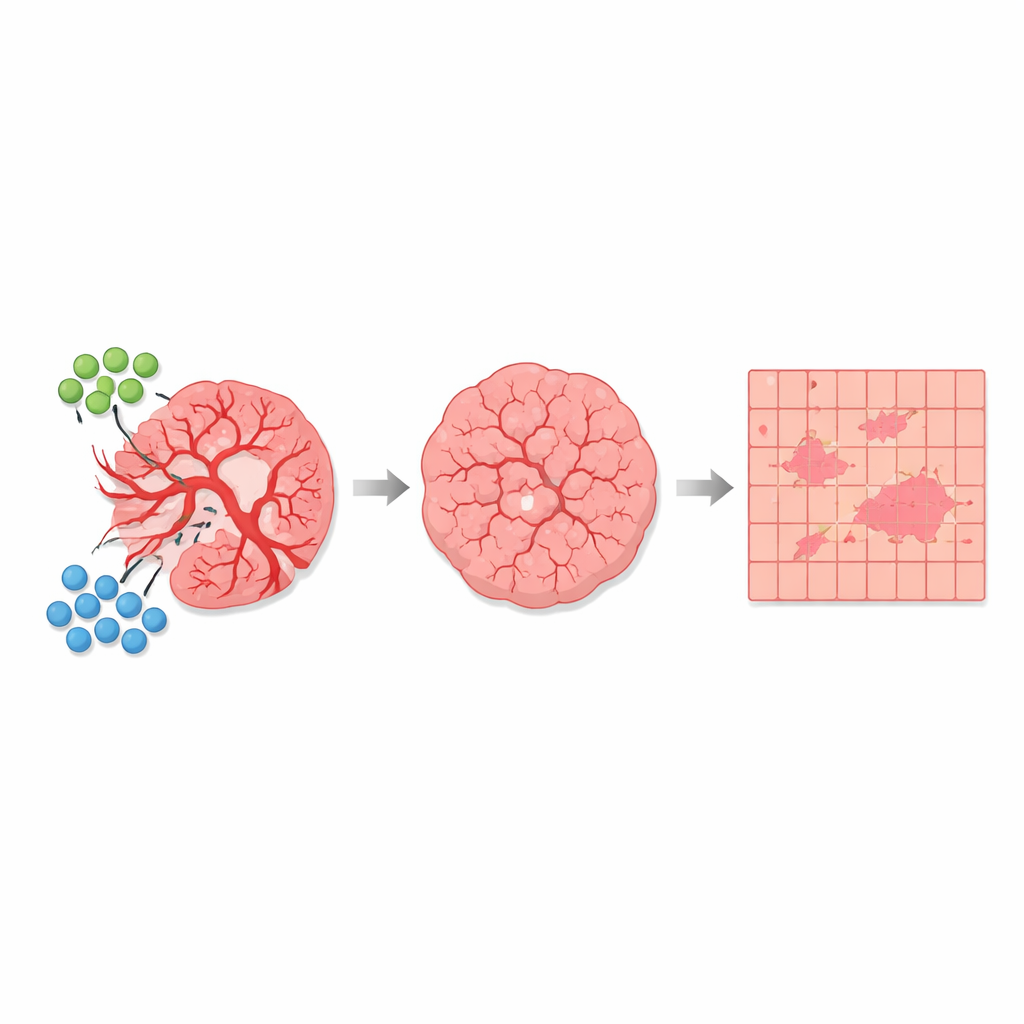
Bu otomatik segmentasyon kullanıma alındıktan sonra yazarlar, tedavi edilmemiş farelerden ve AGRO ile GK1 kombinasyonuyla tedavi edilen farelerden çok sayıda doku kesitini karşılaştırdılar. Analiz edilen toplamda 1.700 milimetre kareyi aşkın dokuda, kan damarlarıyla ilişkili güçlü depolarize eden bölgelerin genel alandan yalnızca yaklaşık yüzde 1’ini kapladığını buldular — ancak bu oranın gruplar arasında açıkça farklılaştığını gözlemlediler. Tedavi edilmemiş tümörlerde damar-dominant doku ve yakınındaki karışık bölgeler tümör kesitinin daha büyük bir kısmını kaplıyordu. Tedavi edilen tümörlerde bu yüksek depolarizasyonlu ve geçişsel bölgeler küçüldü, zayıf depolarize eden bölgeler ise — esas olarak tümör hücrelerinden oluşan — göreli olarak daha yaygın hale geldi. Önemli olarak, her doku tipinin temel optik “imzası” aynı kaldı; terapiyle değişen şey, tümörün hangi kategoriye ne kadar ait olduğuydu ve bu da damarları budayan ve tümör mikroçevresini değiştiren antianjiyogenik bir etkiyle uyumluydu.
Geleceğin Kanser Bakımı İçin Anlamı
Uzman olmayanlar için ana mesaj, bu polarimetrik görüntüleme yönteminin standart mikroskopların kolayca sağlayamadığı geniş açılı, nicel bir tümör mimarisi görünümü sunduğudur. Bir tümör kesitinin ne kadarının kan damarlarıyla ne kadarının tümör hücreleriyle dolu olduğunu nesnel olarak sayarak ve bunu tipik bir mikroskop alanından onlarca kat daha büyük alanlarda yaparak, teknik antianjiyogenik bir tedavinin tümörün kan tedarikini azaltıp azaltmadığını hassas şekilde tespit edebilir. Çalışma bir preklinik fare melanom modelinde yapılmış olsa da, bu yaklaşım araştırmacıların ve nihayetinde klinisyenlerin yeni kanser tedavilerini daha hızlı ve tutarlı biçimde değerlendirmelerine yardımcı olabilecek araçlara işaret ediyor; eğitimli patologun gözüne tamamlayıcı olmayı — yerine geçmeyi değil — amaçlar.
Atıf: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Anahtar kelimeler: melanom, tümör mikroçevresi, polarimetrik görüntüleme, anjiyogenez, kanser tedavisi