Clear Sky Science · it
Discriminazione e quantificazione polarimetrica macroscopica dell’effetto antiangiogenico dell’aptamero AGRO e del peptide GK1 in un modello preclinico di melanoma
Vedere il tessuto tumorale sotto una nuova luce
I medici oncologi e i patologi si affidano ancora in larga misura all’osservazione di sottili sezioni di tessuto al microscopio per valutare il comportamento di un tumore e l’efficacia di una terapia. Ma questa ispezione visiva è lenta, copre solo aree molto piccole e può risultare in parte soggettiva. Questo studio introduce un metodo di imaging basato sulla luce che può scansionare ampie porzioni di tessuto tumorale di melanoma contemporaneamente e distinguere automaticamente le regioni ricche di vasi sanguigni dalle aree densamente popolate da cellule tumorali, offrendo un modo più oggettivo per monitorare come nuovi trattamenti anticancro rimodellano l’architettura interna del tumore.
Perché i vasi sanguigni sono importanti nel melanoma
Il melanoma, la forma più pericolosa di cancro della pelle, diventa spesso letale quando cresce in modo aggressivo e si diffonde nell’organismo. Per farlo, i tumori costruiscono una loro rete di vasi sanguigni, un processo noto come angiogenesi. Questi vasi nutrono il tumore con ossigeno e nutrienti e forniscono vie di fuga per le cellule tumorali verso organi lontani. Per questo motivo, i farmaci che interrompono o rimodellano i vasi tumorali — le cosiddette terapie antiangiogeniche — sono un importante campo di ricerca oncologica. In questo lavoro, gli autori hanno studiato un modello murino di melanoma trattato con la combinazione di due agenti sperimentali, un aptamero chiamato AGRO e un peptide denominato GK1, entrambi progettati per ostacolare l’apporto di sangue e indebolire il tumore.
Trasformare la luce polarizzata in una mappa del tessuto
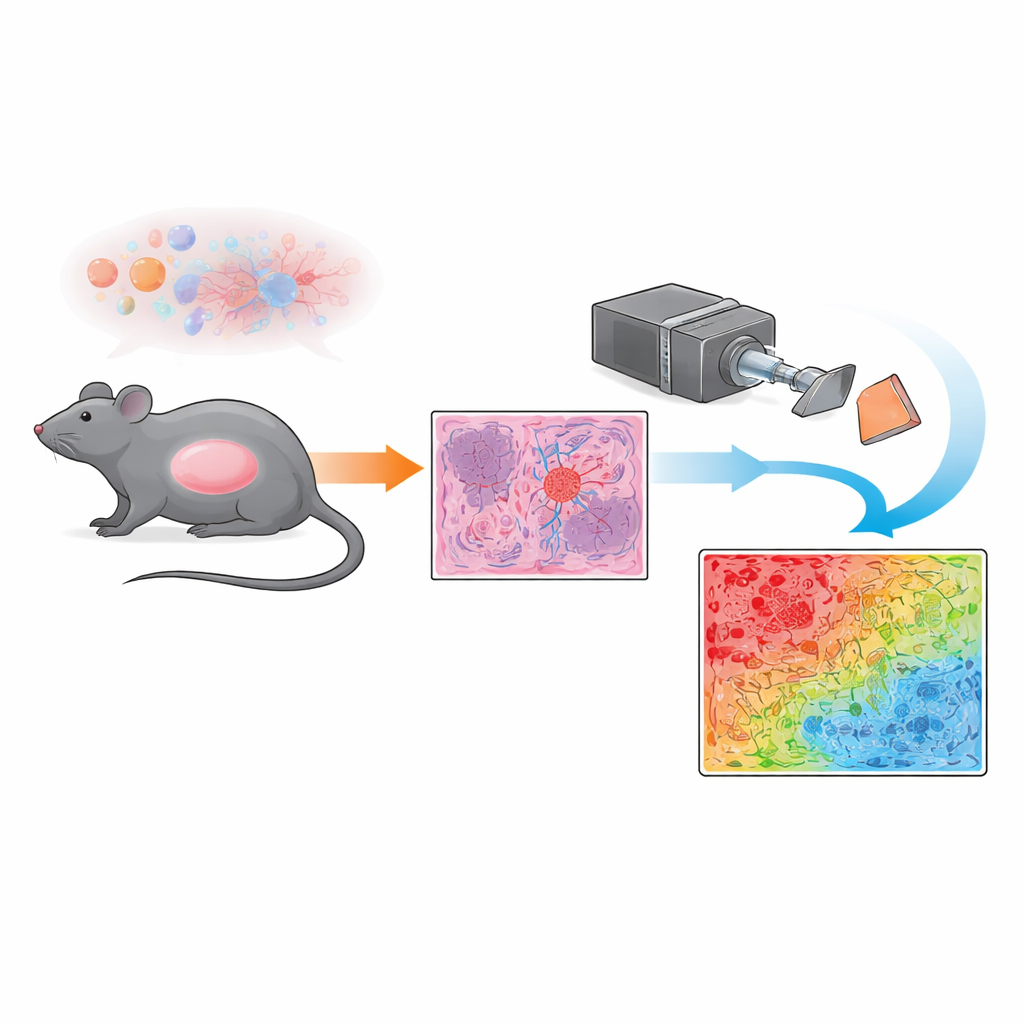
Invece di affidarsi esclusivamente alla microscopia convenzionale, il gruppo ha utilizzato una tecnica chiamata imaging polarimetrico di Mueller. In termini semplici, si illumina con luce polarizzata — onde luminose che vibrano in una direzione preferenziale — le sezioni tumorali colorate e si registra come il tessuto modifica o conserva quella polarizzazione. Diverse strutture all’interno del tumore, come vasi sanguigni densi e disordinati o gruppi più omogenei di cellule tumorali, perturbano la luce in modi distinti. Misurando questi cambiamenti in ogni punto microscopico su un ampio campo visivo, il sistema produce una mappa dell’«indice di depolarizzazione», una sorta di impronta ottica che riflette quanto la struttura microscopica è ordinata o disordinata a ciascun pixel.
Codificare a colori vasi sanguigni e cellule tumorali
Per trasformare queste impronte ottiche in qualcosa che un patologo potesse interpretare a colpo d’occhio, i ricercatori hanno sviluppato uno schema di classificazione pixel per pixel. Hanno prima confrontato le mappe polarimetriche con immagini microscopiche ad alta ingrandimento esaminate da un patologo esperto, concentrandosi su regioni ben definite dominate o dalle cellule tumorali o dai vasi irregolari. Le zone ricche di vasi mostrano forte depolarizzazione (forte disturbo della luce), mentre le aree dominate da cellule tumorali mostrano depolarizzazione più debole (passaggio della luce più ordinato). Utilizzando valori di soglia ricavati da queste regioni di riferimento, il gruppo ha assegnato a ogni pixel una delle categorie — fortemente depolarizzante, debolmente depolarizzante, transizionale o sfondo — e le ha visualizzate come una maschera codificata a colori sulle sezioni intere. Questo approccio ha permesso di quantificare, in millimetri quadrati, quanto di ciascuna sezione tumorale fosse costituito da tessuto dominato dai vasi rispetto a tessuto dominato dalle cellule tumorali e aree miste.
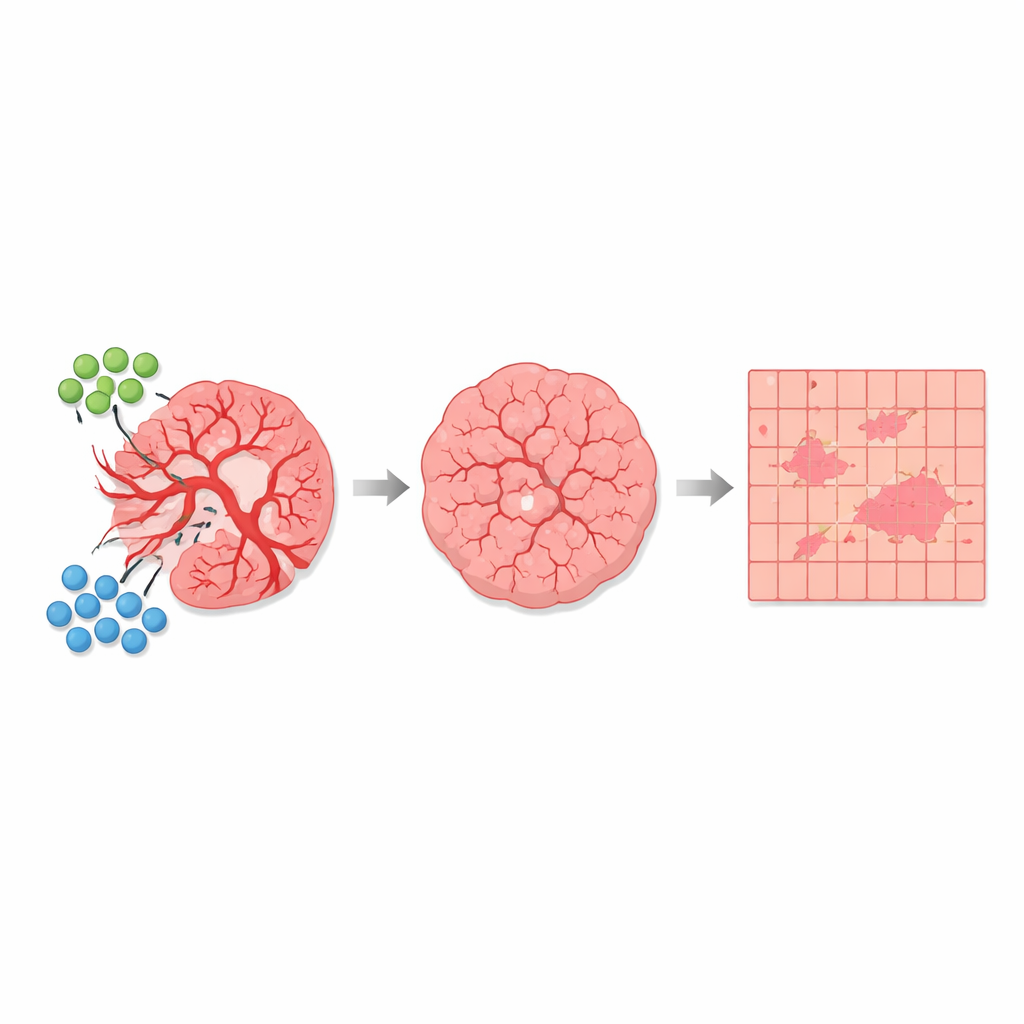
Monitorare l’impatto del trattamento sull’intero tumore
Con questa segmentazione automatica, gli autori hanno confrontato numerose sezioni tissutali di topi non trattati e di topi trattati con la combinazione AGRO più GK1. Su oltre 1.700 millimetri quadrati di tessuto analizzato, hanno rilevato che le regioni fortemente depolarizzanti associate ai vasi sanguigni occupavano complessivamente solo circa l’1% dell’area totale — ma la loro proporzione variava chiaramente tra i gruppi. Nei tumori non trattati, il tessuto dominato dai vasi e le zone miste circostanti occupavano una frazione maggiore della sezione tumorale. Nei tumori trattati, queste regioni ad alta depolarizzazione e transizionali si sono ridotte, mentre le regioni debolmente depolarizzanti, costituite principalmente da cellule tumorali, sono diventate relativamente più abbondanti. È importante notare che la «firma» ottica di base di ciascun tipo di tessuto è rimasta la stessa; ciò che è cambiato con la terapia è stata la quantità di tumore appartenente a ciascuna categoria, coerente con un effetto antiangiogenico che pota i vasi e altera il microambiente tumorale.
Cosa significa per la cura del cancro in futuro
Per i non specialisti, il messaggio chiave è che questo metodo di imaging polarimetrico offre una visione ampia e quantitativa dell’architettura tumorale che i microscopi standard non forniscono facilmente. Contando in modo oggettivo quanto di una sezione tumorale è occupato da vasi rispetto alle cellule tumorali, e facendo ciò su aree decine di volte più ampie rispetto a un campo microscopico tipico, la tecnica può rilevare con sensibilità se un trattamento antiangiogenico sta riducendo l’apporto di sangue al tumore. Pur essendo stato condotto in un modello preclinico murino di melanoma, lo studio indica strumenti futuri che potrebbero aiutare i ricercatori e, in prospettiva, i clinici a valutare nuove terapie oncologiche più rapidamente e in modo più coerente, integrando — ma non sostituendo — l’occhio esperto del patologo.
Citazione: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Parole chiave: melanoma, microambiente tumorale, immagine polarimetrica, angiogenesi, terapia oncologica