Clear Sky Science · pl
Makroskopowa polarimetryczna dyskryminacja i ilościowa ocena efektu przeciwangiogenicznego aptameru AGRO i peptydu GK1 w przedklinicznym modelu czerniaka
Widzenie tkanki nowotworowej w nowym świetle
Onkolodzy i patolodzy nadal w dużej mierze polegają na oglądaniu cienkich skrawków tkanki pod mikroskopem, aby ocenić, jak zachowuje się guz i czy leczenie działa. Jednak taka wizualna inspekcja jest powolna, obejmuje jedynie niewielkie obszary i może być częściowo subiektywna. W tym badaniu przedstawiono metodę obrazowania opartą na świetle, która może jednocześnie skanować duże fragmenty tkanki guza czerniaka i automatycznie rozróżniać rejony bogate w naczynia krwionośne od obszarów wypełnionych komórkami nowotworowymi, oferując bardziej obiektywny sposób śledzenia, jak nowe terapie przeciwnowotworowe przekształcają wewnętrzny krajobraz guza.
Dlaczego naczynia krwionośne mają znaczenie w czerniaku
Czerniak, najgroźniejsza postać raka skóry, często staje się śmiertelny, gdy rośnie agresywnie i daje przerzuty. Aby to umożliwić, guzy tworzą własną sieć naczyń krwionośnych w procesie zwanym angiogenezą. Naczynia te dostarczają guzowi tlen i składniki odżywcze oraz zapewniają drogi ucieczki dla komórek nowotworowych, które mogą dotrzeć do odległych narządów. Z tego powodu leki, które przerywają lub przebudowują naczynia guza — tzw. terapie przeciwangiogeniczne — są ważnym obszarem badań nad rakiem. W tej pracy autorzy badali myszy z modelem czerniaka leczone kombinacją dwóch eksperymentalnych środków: aptameru o nazwie AGRO i peptydu nazwanego GK1, oba zaprojektowane, by zaburzać ukrwienie i osłabiać guz.
Przekształcanie spolaryzowanego światła w mapę tkanki
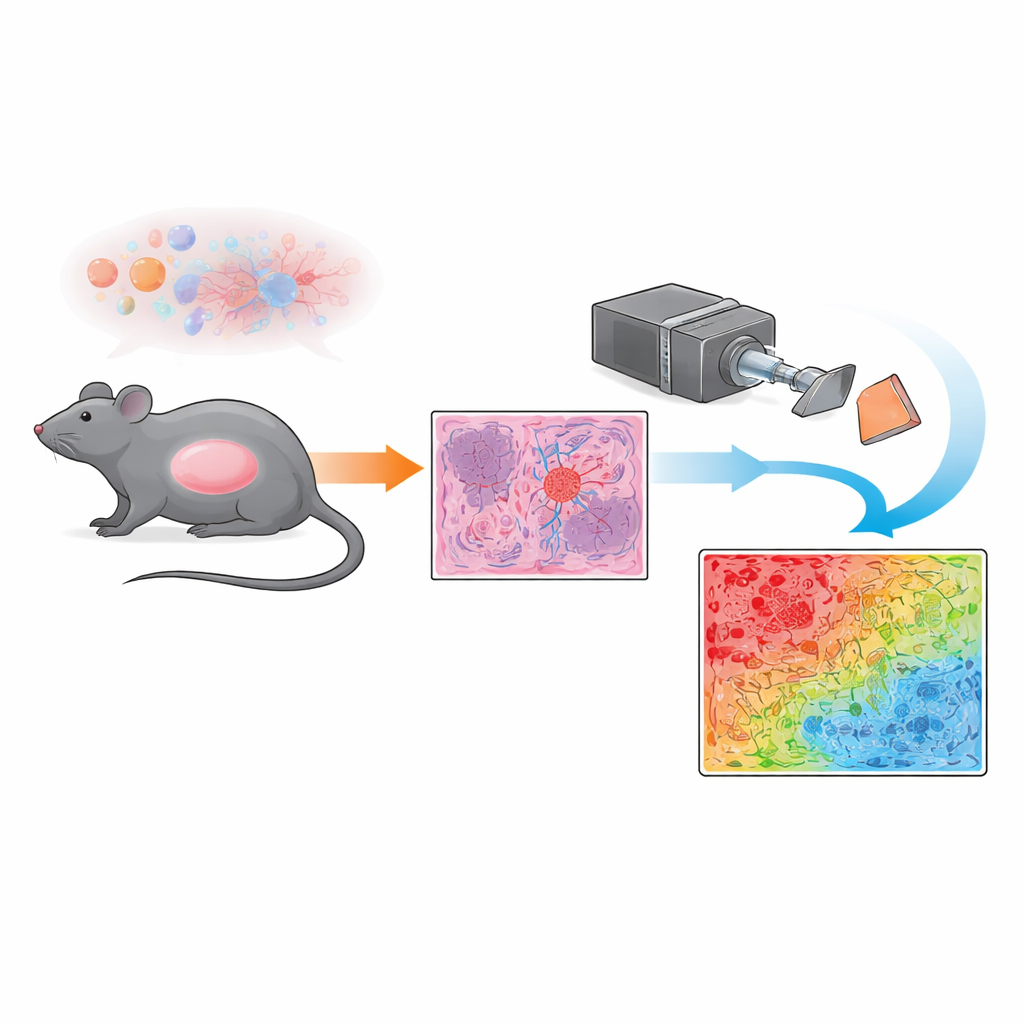
Zamiast polegać wyłącznie na konwencjonalnej mikroskopii, zespół zastosował technikę zwaną obrazowaniem polarimetrycznym Muellera. Mówiąc prościej, na barwione skrawki guza pada spolaryzowane światło — fale świetlne drgające w preferowanym kierunku — i rejestruje się, jak tkanka miesza lub zachowuje tę polaryzację. Różne struktury w guzie, takie jak gęste, chaotyczne naczynia krwionośne lub bardziej jednorodne skupiska komórek nowotworowych, zaburzają światło na różne sposoby. Mierząc te zmiany w każdym małym punkcie na dużym polu widzenia, system tworzy mapę „wskaźnika depolaryzacji”, rodzaj optycznego odcisku palca pokazującego, jak uporządkowana lub nieuporządkowana jest mikroskopowa struktura w każdym pikselu.
Kodowanie kolorami naczyń i komórek nowotworowych
Aby przekształcić te optyczne odciski w coś, co patolog mógłby szybko zinterpretować, badacze opracowali prosty schemat klasyfikacji piksel-po-pikselu. Najpierw porównali mapy polarimetryczne z obrazami mikroskopowymi o dużym powiększeniu ocenianymi przez doświadczonego patologa, koncentrując się na dobrze zdefiniowanych obszarach zdominowanych albo przez komórki nowotworowe, albo przez nieregularne naczynia krwionośne. Strefy bogate w naczynia wykazywały silną depolaryzację (duże mieszanie światła), podczas gdy obszary z dominującymi komórkami nowotworowymi wykazywały słabszą depolaryzację (bardziej uporządkowane przejście światła). Używając wartości progowych wyprowadzonych z tych regionów referencyjnych, zespół przypisał każdy piksel do jednej z kilku kategorii — silnie depolaryzujący, słabo depolaryzujący, przejściowy lub tło — i wyświetlał je jako maskę kodowaną kolorami na całych przekrojach. Podejście to pozwoliło im ilościowo określić w milimetrach kwadratowych, jaka część każdego skrawka guza składała się z tkanki zdominowanej przez naczynia wobec tkanki zdominowanej przez komórki nowotworowe oraz obszarów mieszanych.
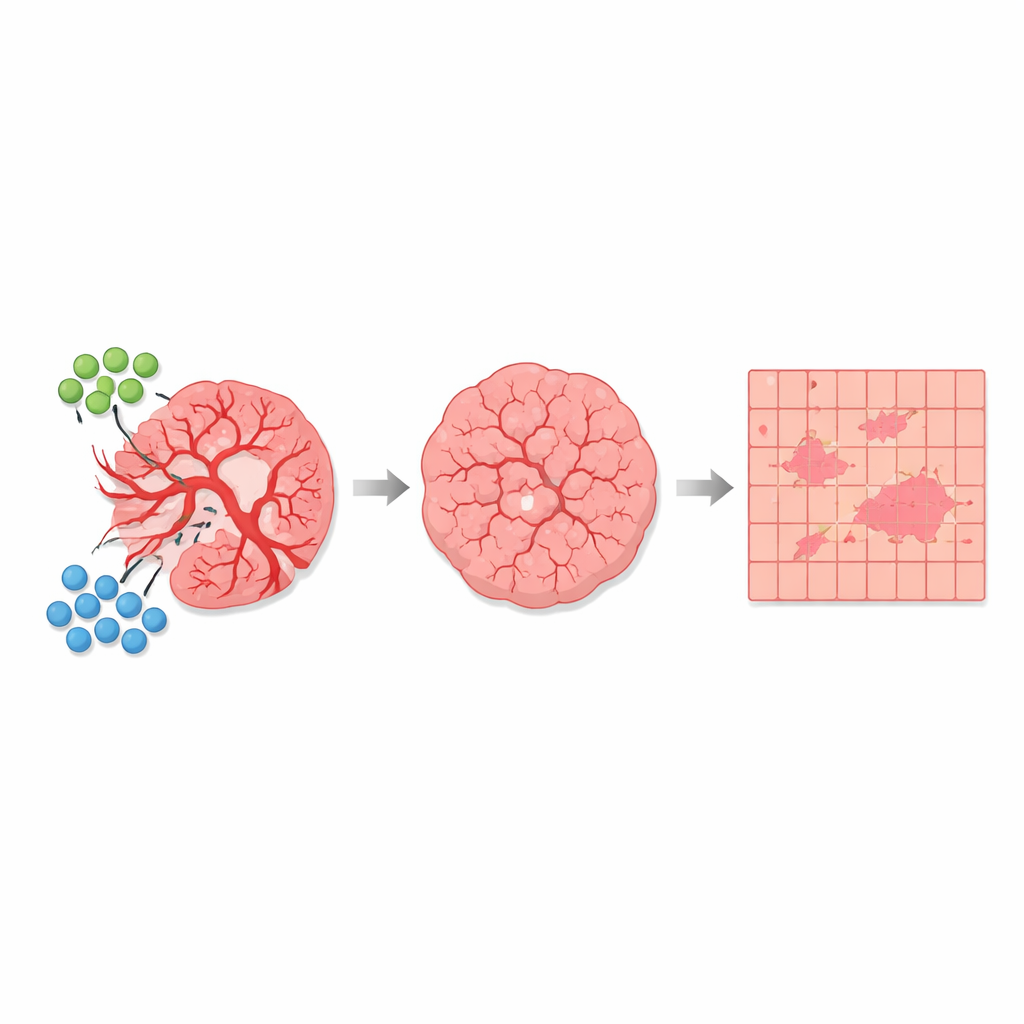
Śledzenie wpływu leczenia w całym guzie
Dzięki automatycznej segmentacji autorzy porównali wiele przekrojów tkanki od myszy nieleczonych oraz myszy leczonych kombinacją AGRO plus GK1. Na ponad 1 700 milimetrach kwadratowych analizowanej tkanki stwierdzili, że silnie depolaryzujące obszary związane z naczyniami krwionośnymi zajmowały łącznie jedynie około 1 procent całkowitej powierzchni — jednak ich odsetek wyraźnie różnił się między grupami. W guzach nieleczonych tkanka zdominowana przez naczynia i sąsiednie strefy mieszane zajmowały większą część skrawka guza. W guzach leczonych te obszary o wysokiej depolaryzacji i strefy przejściowe zmniejszyły się, podczas gdy obszary słabo depolaryzujące, głównie złożone z komórek nowotworowych, stały się stosunkowo bardziej rozpowszechnione. Co ważne, podstawowy optyczny „sygnatur” każdego typu tkanki pozostał niezmieniony; to, co zmieniło się pod wpływem terapii, to udział guza przypadający na poszczególne kategorie, zgodnie z efektem przeciwangiogenicznym prowadzącym do przerzedzenia naczyń i zmiany mikrośrodowiska guza.
Co to oznacza dla przyszłej opieki nad chorymi na raka
Dla osób niemających specjalistycznej wiedzy kluczowym przesłaniem jest to, że ta metoda obrazowania polarimetrycznego oferuje szerokokątny, ilościowy wgląd w architekturę guza, którego standardowe mikroskopy nie dostarczają łatwo. Poprzez obiektywne zliczanie, jaka część skrawka guza jest zajęta przez naczynia krwionośne w porównaniu z komórkami nowotworowymi — i robienie tego na obszarach dziesiątki razy większych niż typowe pole mikroskopu — technika może czułe wykrywać, czy terapia przeciwangiogeniczna zmniejsza unaczynienie guza. Chociaż badanie przeprowadzono w przedklinicznym modelu myszy z czerniakiem, wyniki wskazują na przyszłe narzędzia, które mogą pomóc badaczom i w końcu klinicystom szybciej i bardziej konsekwentnie oceniać nowe terapie przeciwnowotworowe, uzupełniając — ale nie zastępując — wytrenowane oko patologa.
Cytowanie: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Słowa kluczowe: czerniak, mikrośrodowisko guza, obrazowanie polarimetryczne, angiogeneza, terapia nowotworowa