Clear Sky Science · ru
Макроскопическая поляриметрическая дифференциация и количественная оценка антиангиогенного эффекта аптамера AGRO и пептида GK1 в доклинической модели меланомы
Видеть раковую ткань в новом свете
Онкологи и патологы по-прежнему во многом опираются на изучение тонких срезов ткани под микроскопом, чтобы оценить поведение опухоли и эффективность лечения. Однако такой визуальный осмотр медленный, охватывает лишь крошечные участки и частично субъективен. В этом исследовании предложен оптический метод визуализации, который может сканировать большие участки ткани меланомы одновременно и автоматически отличать зоны, богатые кровеносными сосудами, от областей, заполненных опухолевыми клетками, предлагая более объективный способ отслеживать, как новые противораковые препараты перестраивают внутреннюю структуру опухоли.
Почему кровеносные сосуды важны при меланоме
Меланома, самая опасная форма рака кожи, часто становится угрожающей жизни, когда агрессивно растёт и метастазирует. Для этого опухоли формируют собственную сеть кровеносных сосудов — процесс, известный как ангиогенез. Эти сосуды питают опухоль кислородом и питательными веществами и служат путями для распространения раковых клеток в отдалённые органы. Поэтому препараты, которые перекрывают или перестраивают сосуды опухоли — антиангиогенные терапии — являются важным направлением онкологических исследований. В этой работе авторы исследовали мышиную модель меланомы, леченную комбинацией двух экспериментальных агентов: аптамера AGRO и пептида GK1, оба нацелены на нарушение кровоснабжения и ослабление опухоли.
Преобразование поляризованного света в карту ткани
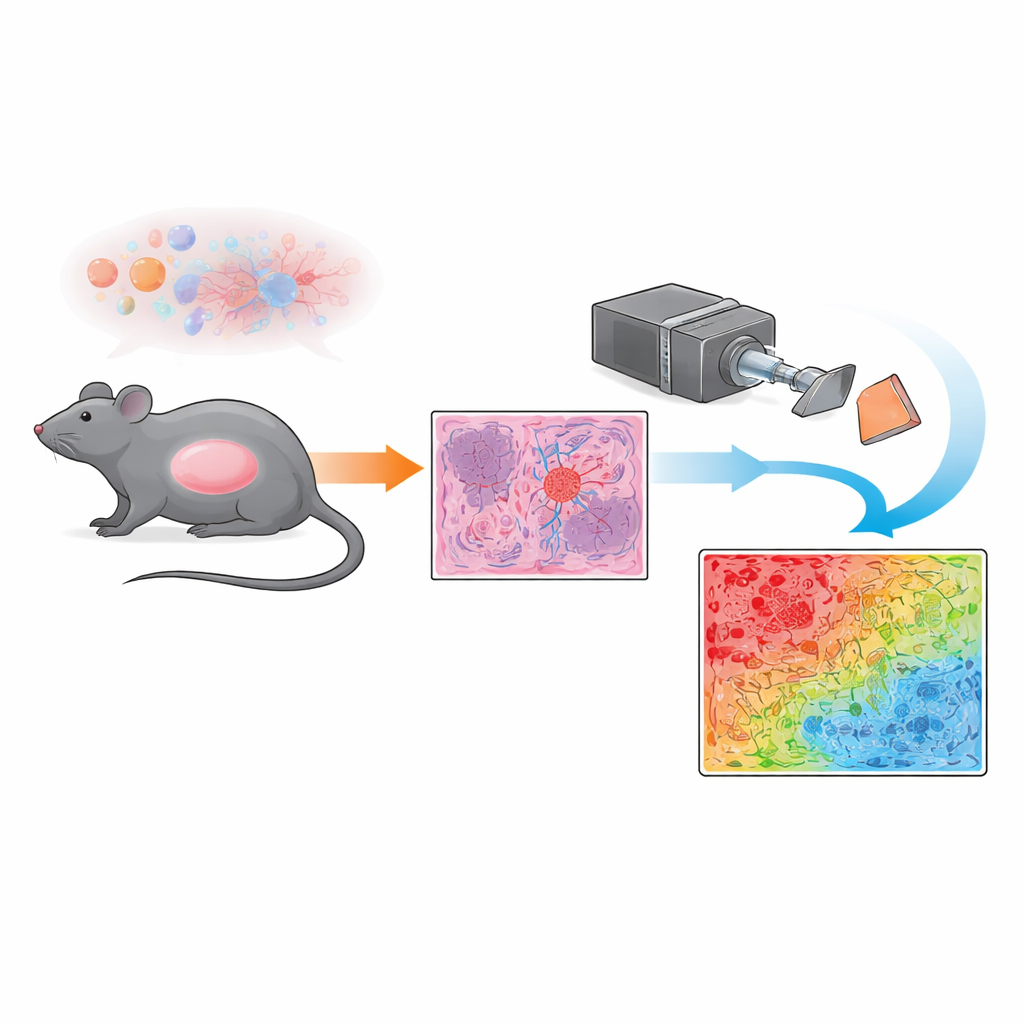
Вместо того чтобы полагаться только на традиционную микроскопию, команда применила метод мюллеровской поляриметрической визуализации. Проще говоря, на окрашенные срезы опухоли направляют поляризованный свет — волны света, колеблющиеся в предпочтительном направлении — и фиксируют, как ткань искажает или сохраняет эту поляризацию. Разные структуры внутри опухоли, такие как плотные неупорядоченные сосуды или более однородные скопления опухолевых клеток, по‑разному меняют поляризацию света. Измеряя эти изменения в каждой точке большого поля зрения, система строит карту «индекса деполяризации» — некий оптический отпечаток, отражающий степень упорядоченности или хаотичности микроструктуры в каждом пикселе.
Кодирование цветом сосудов и опухолевых клеток
Чтобы превратить эти оптические отпечатки в наглядное изображение для патолога, исследователи разработали простую построчную классификацию пикселей. Сначала они сравнили поляриметрические карты с микроскопическими изображениями высокого увеличения, проанализированными экспертом-патоморфологом, сосредоточив внимание на чётко определённых областях, доминирующих либо опухолевыми клетками, либо неправильными кровеносными сосудами. Зоны, богатые сосудами, демонстрировали сильную деполяризацию (сильное перемешивание света), тогда как области, доминируемые опухолевыми клетками, показывали более слабую деполяризацию (более упорядоченное прохождение света). Используя пороговые значения, выведенные из этих эталонных участков, команда отнесла каждый пиксель к одной из категорий — сильно деполяризующие, слабо деполяризующие, переходные или фоновая область — и отобразила их в виде цветовой маски на всем срезе. Такой подход позволил количественно оценить в квадратных миллиметрах, какая часть каждого среза состоит из ткани, доминируемой сосудами, по сравнению с тканью, доминируемой опухолевыми клетками, и смешанных зон.
Отслеживание влияния лечения по всему объёму опухоли
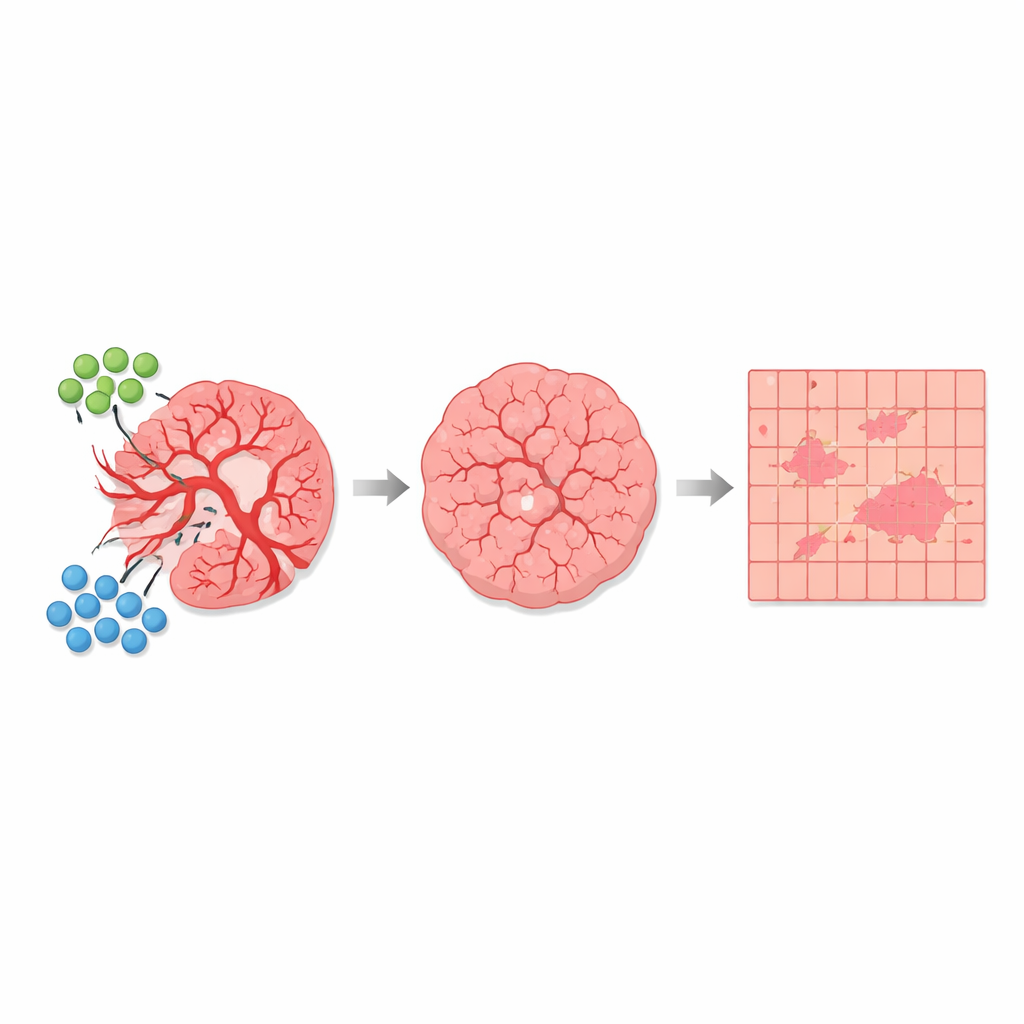
С автоматической сегментацией авторы сравнили множество срезов ткани от нелечённых мышей и от мышей, получавших комбинацию AGRO плюс GK1. На более чем 1700 квадратных миллиметров проанализированной ткани они обнаружили, что сильно деполяризующие области, связанные с сосудами, занимали всего около 1 процента от общей площади — но их доля явно различалась между группами. В нелечённых опухолях зоны, доминируемые сосудами, и соседние смешанные области занимали большую долю среза. В обработанных опухолях эти области с высокой деполяризацией и переходные зоны уменьшались, тогда как слабо деполяризующие области, в основном состоящие из опухолевых клеток, относительной мерой становились более обширными. Важно, что базовый оптический «подпись» каждого типа ткани оставался прежним; изменялось только соотношение площадей в каждой категории, что согласуется с антиангиогенным эффектом, который уменьшает число сосудов и изменяет микроокружение опухоли.
Что это значит для будущей онкологической помощи
Для неспециалистов основной вывод заключается в том, что этот метод поляриметрической визуализации предоставляет широкий количественный обзор архитектуры опухоли, которого обычные микроскопы легко не дают. Объективно подсчитывая, какая часть среза опухоли занята сосудами и какая — опухолевыми клетками, и делая это на участках в десятки раз больших, чем типичное поле зрения микроскопа, техника чувствительно выявляет, снижает ли антиангиогенное лечение кровоснабжение опухоли. Хотя работа проведена в доклинической модели меланомы у мышей, она указывает на возможные будущие инструменты, которые помогут исследователям и, в перспективе, клиницистам быстрее и последовательнее оценивать новые противораковые терапии, дополняя — но не заменяя — опытное мнение патолога.
Цитирование: Montes-Gonzalez, I., Bisbal-Amat, J., Perez-Torres, A. et al. Macroscopic polarimetric discrimination and quantification of antiangiogenic effect of AGRO aptamer and GK1 peptide in a preclinical melanoma model. Sci Rep 16, 14299 (2026). https://doi.org/10.1038/s41598-026-44959-7
Ключевые слова: меланома, опухолевое микроокружение, поляриметрическая визуализация, ангиогенез, терапия рака