Clear Sky Science · zh
由 let-7g-5p/STAT2 轴调控的 IFITM3 介导的癫痫神经炎症
为何脑内炎症在癫痫中重要
癫痫影响着全球数千万人的生活,其中约三分之一患者现有药物无法完全控制发作。科学家越来越认为,脑内的慢性炎症会使发作更频繁且更难治疗。本研究探讨了脑内免疫细胞中一条新发现的分子链,这条链似乎能够加剧或缓解伴随癫痫的炎症反应。理解这条链条或能为未来疗法开辟道路,这类疗法通过平息大脑自身的免疫反应而非仅仅抑制电活动来发挥作用。
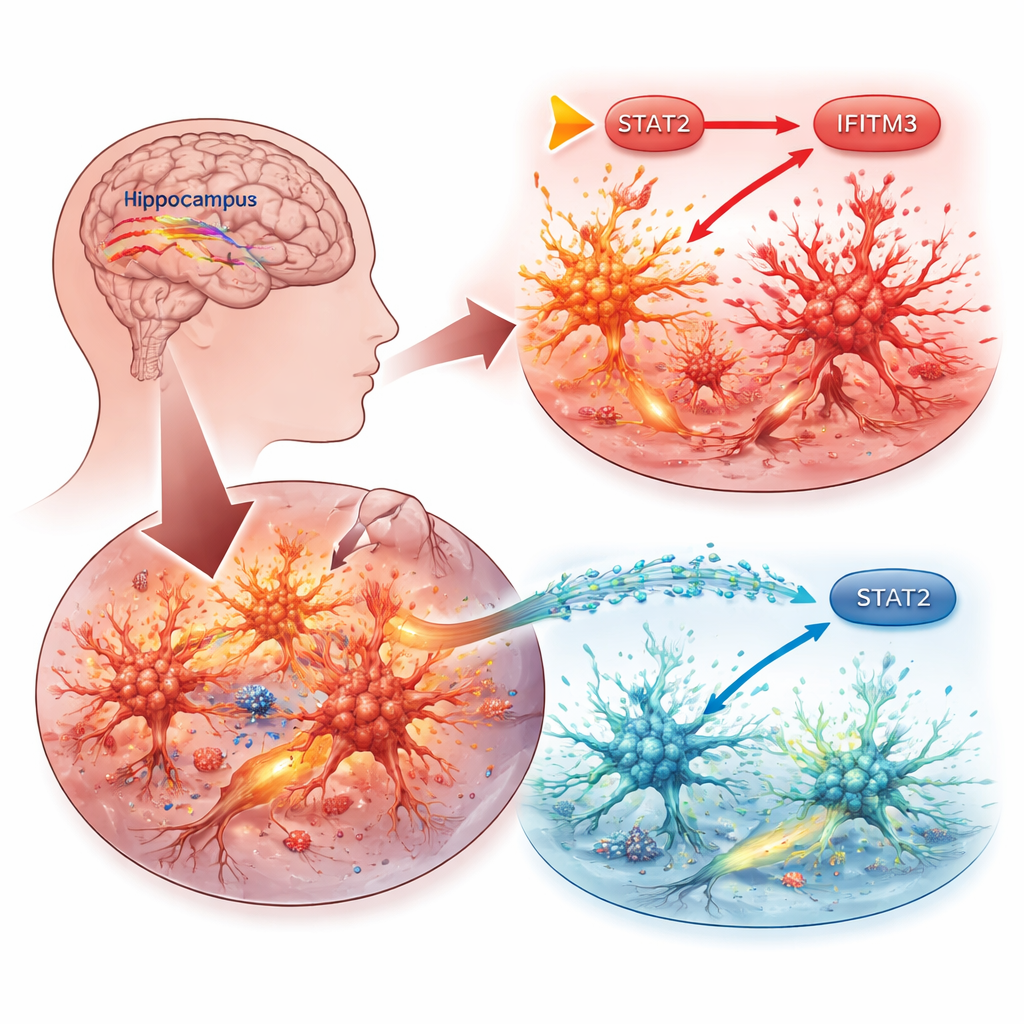
聚焦大脑的免疫细胞
该研究聚焦于小胶质细胞——大脑的常驻免疫细胞。当癫痫发作或其他损伤发生时,小胶质细胞会被激活,释放炎性分子,这些分子可损伤附近神经元并降低再次发生发作的阈值。研究者们探究了小胶质细胞内哪些特定分子驱动了这一有害循环。他们首先从小鼠癫痫模型和炎症小胶质细胞的公共基因数据库中挖掘,寻找那些持续上调的基因。一位候选者脱颖而出:IFITM3——一种最初以帮助细胞抵御病毒而闻名的蛋白,但越来越多研究将其与阿尔茨海默病、卒中等情况下的脑炎症联系起来。
加重癫痫的分子开关
为测试 IFITM3 的作用,团队使用了暴露于细菌模拟物的鼠源小胶质细胞,这种处理会强烈激活炎症。当 IFITM3 水平升高时,细胞释放出大量炎性介质,如白细胞介素-1β、白细胞介素-6 和肿瘤坏死因子,同时显示出更多的程序性细胞死亡迹象,包括一种伴随膜孔形成的炽热性细胞焦亡(pyroptosis)。沉默 IFITM3 则产生相反效果,显著降低炎性信号和细胞死亡标志物。研究人员随后转入在体实验,构建小鼠慢性发作模型并用病毒载体在脑内下调 IFITM3。IFITM3 降低的小鼠在行为评分量表上表现出较轻的癫痫,脑电记录更平静,脑组织中的炎性和细胞死亡标志物水平也较低。
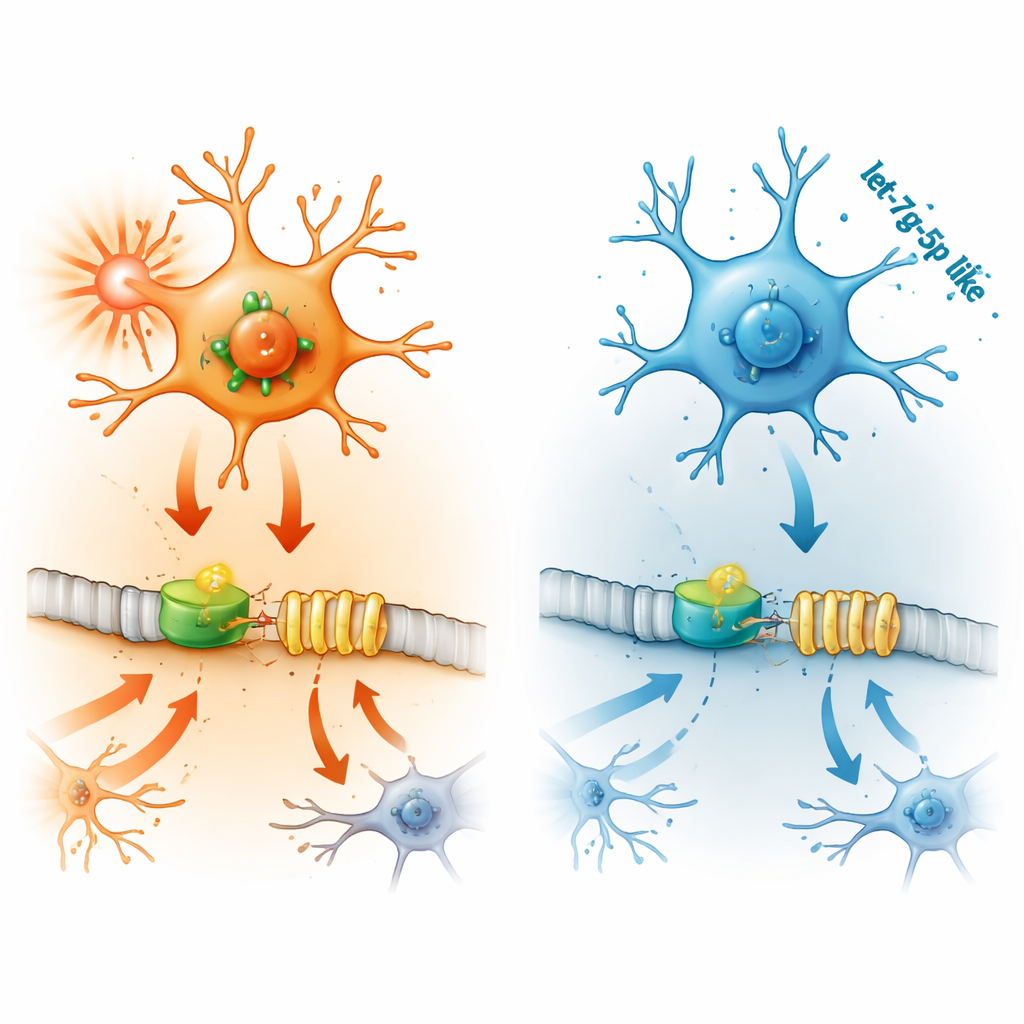
上游分子如何开启或关闭 IFITM3
接着,研究者追踪了 IFITM3 的上调机制。他们锁定了 STAT2——一种将干扰素(关键免疫分子)的信号传递到细胞 DNA 的蛋白。在小胶质细胞中,增强 STAT2 会提高 IFITM3 水平并加剧炎症与细胞死亡,而敲低 STAT2 则产生相反效果。使用 DNA 报告子构建的实验显示,STAT2 直接结合 IFITM3 基因的调控区以激活其表达。在癫痫小鼠中,STAT2 在易发生发作的大脑区域也升高,但关闭 IFITM3 并未改变 STAT2 本身,证实 STAT2 位于上游,作为主控开关。
施加刹车的小分子 RNA
链条中的最后一环是 let-7g-5p,一种微小的调控 RNA 分子。像 let-7g-5p 这样的微小 RNA 通过结合目标信使 RNA、阻止其翻译为蛋白,从而微调基因活性。在炎症小胶质细胞和癫痫小鼠脑中,let-7g-5p 的水平下降。体外实验显示,let-7g-5p 可直接结合 STAT2 信使 RNA 的 3' 非翻译区,降低 STAT2 的产生。当研究者向小胶质细胞中补充额外的 let-7g-5p 时,STAT2 与 IFITM3 水平下降,炎性信号减少,细胞死亡减缓。阻断 let-7g-5p 则产生相反效应——但同时沉默 STAT2 能够挽救该效应,证明 let-7g-5p 通过靶向 STAT2(进而影响 IFITM3)发挥保护作用。
这对癫痫患者可能意味着什么
总体而言,这些发现勾勒出一个简明而有力的故事:STAT2 在小胶质细胞中启动 IFITM3,进而加剧脑内炎症与细胞死亡,使癫痫恶化;而 let-7g-5p 则作为这一过程的天然刹车。在癫痫中,这一刹车似乎失效,导致炎症失控。尽管这些结果来自细胞和小鼠而非患者,但它们凸显了 let-7g-5p/STAT2/IFITM3 轴作为一个有前景的新靶点。未来的治疗策略可能旨在增强 let-7g-5p 或抑制 STAT2 或 IFITM3,其目的不是根治癫痫本身,而是冷却有助于发作持续并对常规药物产生抵抗的炎性环境。
引用: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
关键词: 癫痫, 神经炎症, 小胶质细胞, IFITM3, 微小RNA let-7g-5p