Clear Sky Science · nl
IFITM3-gemedieerde neuro-inflammatie bij epilepsie gereguleerd door de let-7g-5p/STAT2-as
Waarom ontsteking in de hersenen van belang is bij epilepsie
Epilepsie treft tientallen miljoenen mensen wereldwijd, en bij ongeveer één op de drie patiënten bieden de huidige medicijnen geen volledige controle over aanvallen. Wetenschappers vermoeden in toenemende mate dat chronische ontsteking binnen de hersenen bijdraagt aan frequentere en moeilijker behandelbare aanvallen. Deze studie onderzoekt een nieuw ontdekte keten van moleculen in de immuuncellen van de hersenen die de ontstekingsreactie bij epilepsie lijkt aan te wakkeren of juist te dempen. Inzicht in deze keten kan de deur openen naar toekomstige behandelingen die werken door de eigen immuunreactie van de hersenen te kalmeren in plaats van alleen de elektrische activiteit te onderdrukken.
De immuuncellen van de hersenen in de schijnwerper
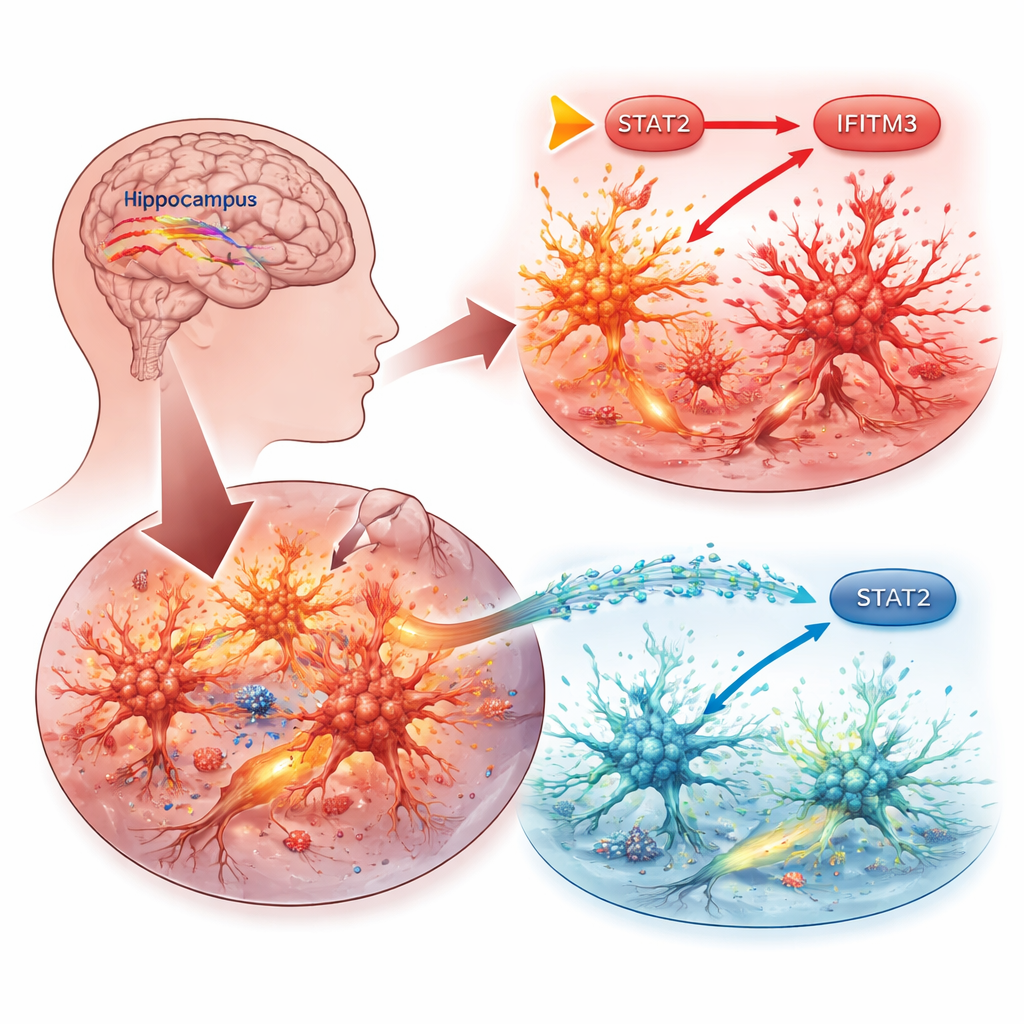
Het werk richt zich op microglia, de residentiële immuuncellen van de hersenen. Wanneer aanvallen of andere beschadigingen optreden, schakelen microglia over naar een geactiveerde staat en scheiden zij ontstekingsbevorderende stoffen uit die omliggende zenuwcellen kunnen beschadigen en de drempel voor nieuwe aanvallen verlagen. De onderzoekers vroegen welke specifieke moleculen binnen microglia deze schadelijke cyclus aansturen. Ze begonnen met het analyseren van openbare genetische databanken van muismodellen van epilepsie en ontstoken microglia, op zoek naar genen die consequent omhooggereguleerd waren. Eén kandidaat stak er bovenuit: IFITM3, een eiwit dat vooral bekend is vanwege zijn rol bij de bestrijding van virussen maar dat steeds vaker wordt gekoppeld aan hersenontsteking bij aandoeningen zoals de ziekte van Alzheimer en beroerte.
Een moleculaire schakel die aanvallen verergert
Om de rol van IFITM3 te testen, gebruikte het team muismicroglia die werden blootgesteld aan een bacterie-imitator die sterk ontstekingsreacties activeert. Bij hoge IFITM3-niveaus produceerden de cellen meer ontstekingsboodschappers zoals interleukine-1β, interleukine-6 en tumor necrose factor, en vertoonden ze meer tekenen van geprogrammeerde celdood, waaronder een vurige, porievormende vorm die pyroptose wordt genoemd. Het stilleggen van IFITM3 had het tegenovergestelde effect en verminderde de ontstekingssignalen en merkers voor celdood sterk. De onderzoekers gingen vervolgens naar levende dieren en creëerden een chronisch aanvalmodel bij muizen en gebruikten een virus om IFITM3 in de hersenen omlaag te brengen. Muizen met verlaagd IFITM3 vertoonden mildere aanvallen op gedragsbeoordelingsschalen, kalmere hersengolfopnames en lagere niveaus van ontstekings- en celdoodmerkers in hersenweefsel.
Hoe upstream-moleculen IFITM3 aan- en uitzetten
Vervolgens traceerden de onderzoekers hoe IFITM3 wordt aangezet. Ze richtten zich op STAT2, een eiwit dat signalen van interferonen — sleutelimmuunmoleculen — naar het DNA van de cel draagt. In microglia verhoogde versterking van STAT2 de IFITM3-niveaus en intensiveerde ontsteking en celdood, terwijl het onderdrukken van STAT2 het omgekeerde effect had. Experimenten met DNA-reporterconstructen toonden aan dat STAT2 zich rechtstreeks bindt aan het regulerende gebied van het IFITM3-gen om het te activeren. In epileptische muizen was STAT2 ook verhoogd in hersengebieden die gevoelig zijn voor aanvallen, maar het uitschakelen van IFITM3 veranderde STAT2 zelf niet, wat bevestigt dat STAT2 upstream staat als een hoofdschakelaar.
Een klein RNA dat de rem inknijpt
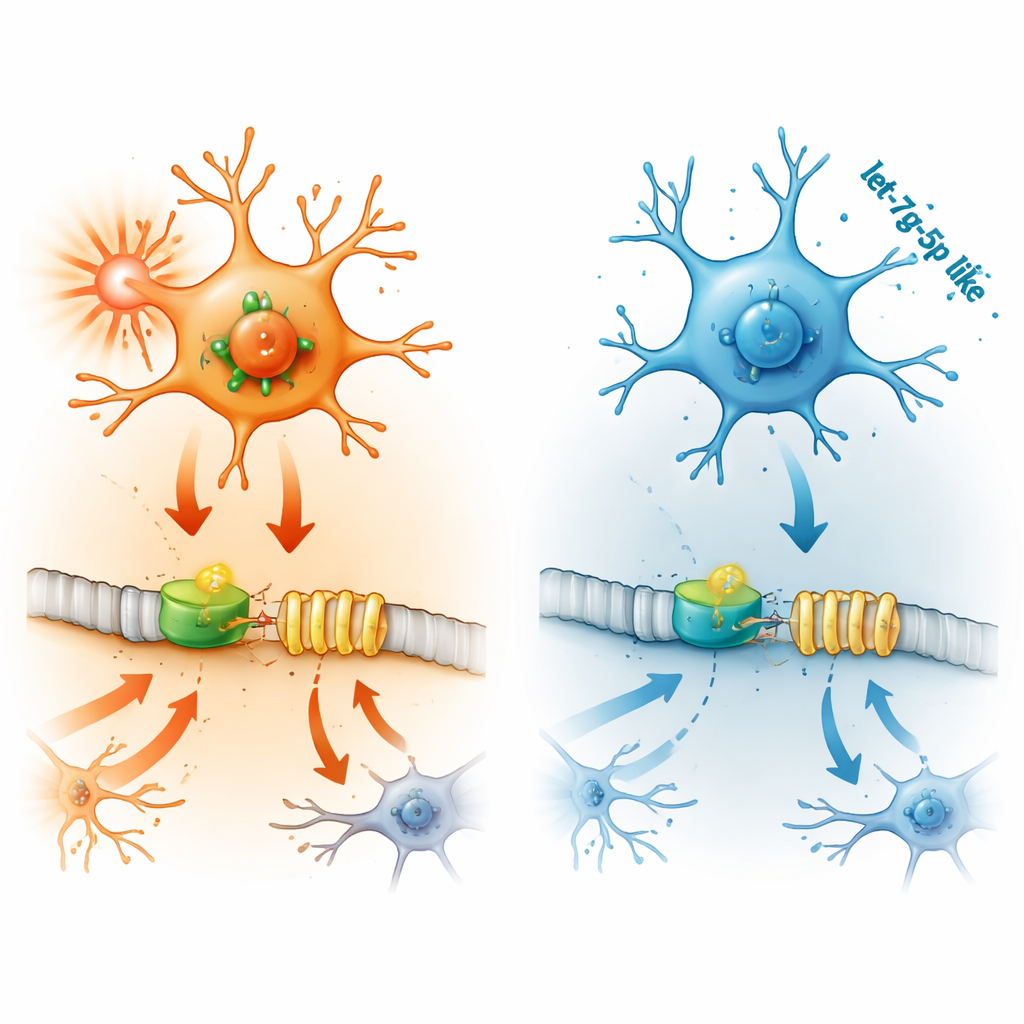
De laatste schakel in de keten is let-7g-5p, een klein regulerend RNA-molecuul. MicroRNA's zoals let-7g-5p fijnregelen genactiviteit door zich te hechten aan doelboodschappen en hun vertaling naar eiwit te blokkeren. In ontstoken microglia en in de hersenen van epileptische muizen daalden de niveaus van let-7g-5p. Laboratoriumtesten toonden aan dat let-7g-5p rechtstreeks bindt aan het staartgebied van de genetische boodschap van STAT2 en zo de productie van STAT2 verlaagt. Wanneer de onderzoekers extra let-7g-5p aan microglia toevoegden, daalden STAT2- en IFITM3-niveaus, namen de ontstekingssignalen af en vertraagde de celdood. Het blokkeren van let-7g-5p had het tegengestelde effect — maar dit kon worden hersteld door tegelijkertijd STAT2 te onderdrukken, wat bewijst dat let-7g-5p beschermt door STAT2 te richten en daarmee IFITM3 te beïnvloeden.
Wat dit voor mensen met epilepsie kan betekenen
Samen schetsen deze bevindingen een eenvoudig maar krachtig verhaal: STAT2 zet IFITM3 aan in microglia, wat de hersenontsteking en celdood opvoert en aanvallen verergert, terwijl let-7g-5p fungeert als een natuurlijke rem op dit proces. Bij epilepsie lijkt die rem te falen, waardoor ontsteking kan escaleren. Hoewel deze resultaten afkomstig zijn van cellen en muizen en niet van patiënten, benadrukken ze de let-7g-5p/STAT2/IFITM3-as als een veelbelovend nieuw doelwit. Toekomstige therapieën zouden kunnen proberen let-7g-5p te versterken of STAT2 of IFITM3 te blokkeren — niet om epilepsie volledig te genezen, maar om de ontstekingsomgeving te koelen die bijdraagt aan het aanhouden van aanvallen en hun resistentie tegen standaardmedicatie.
Bronvermelding: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Trefwoorden: epilepsie, neuro-inflammatie, microglia, IFITM3, microRNA let-7g-5p