Clear Sky Science · pl
Neurozapalenie związane z IFITM3 w epilepsji regulowane osią let-7g-5p/STAT2
Dlaczego zapalenie mózgu ma znaczenie w epilepsji
Epilepsja dotyka dziesiątki milionów osób na całym świecie, a u około jednej trzeciej chorych dostępne leki nie kontrolują napadów w pełni. Coraz więcej dowodów sugeruje, że przewlekłe zapalenie w obrębie mózgu przyczynia się do częstszych i trudniejszych do leczenia napadów. W tym badaniu zbadano nowo odkryty łańcuch cząsteczek w komórkach odpornościowych mózgu, który wydaje się podsycać — lub tłumić — towarzyszące epilepsji procesy zapalne. Zrozumienie tego łańcucha może otworzyć drogę do przyszłych terapii polegających na łagodzeniu odpowiedzi immunologicznej mózgu, a nie tylko tłumieniu aktywności elektrycznej.
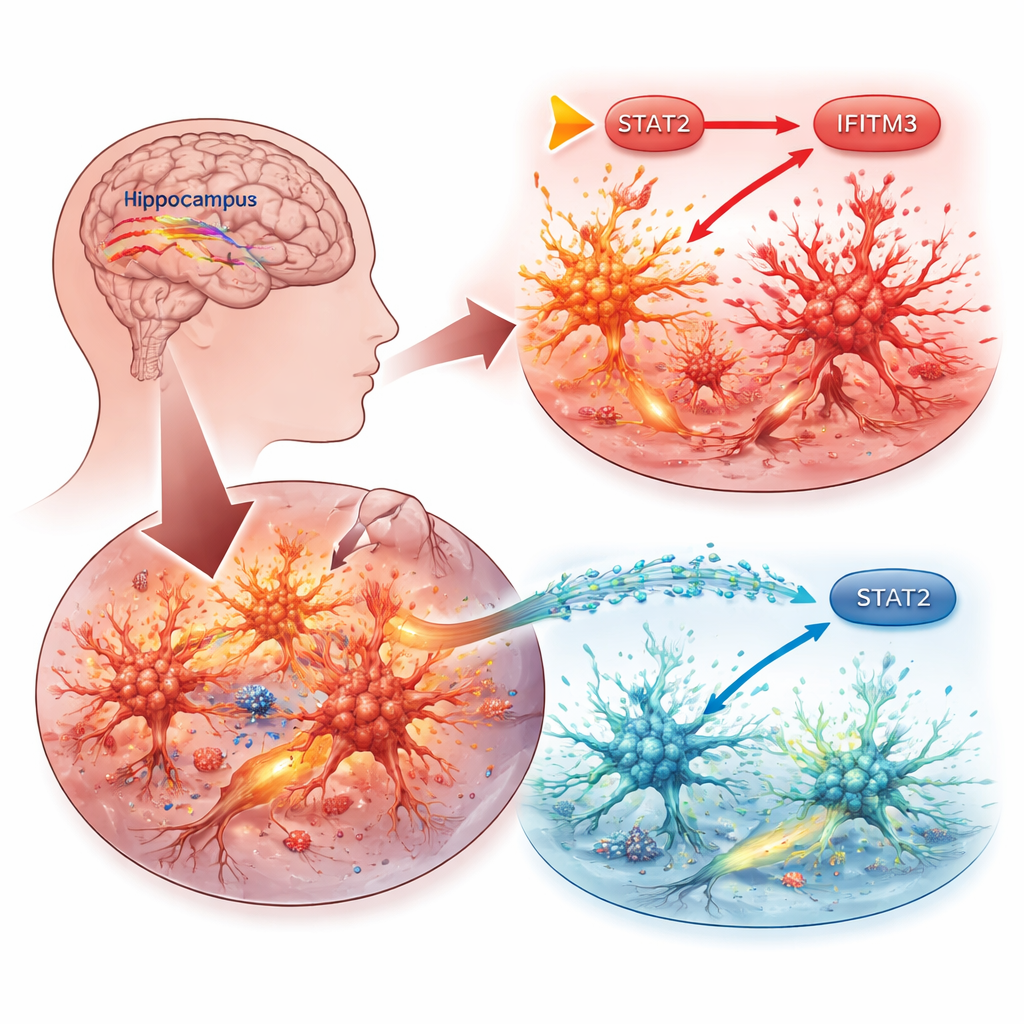
Komórki odpornościowe mózgu w centrum uwagi
Prace koncentrują się na mikrogleju, czyli komórkach odpornościowych rezydujących w mózgu. Gdy wystąpią napady lub inne urazy, mikroglej przechodzi w stan aktywacji, uwalniając związki zapalne, które mogą uszkadzać pobliskie neurony i obniżać próg kolejnych napadów. Badacze pytali, które konkretne cząsteczki wewnątrz mikrogleju napędzają ten szkodliwy cykl. Zaczęli od przeszukania publicznych baz genetycznych pochodzących z modeli mysich epilepsji i zapalonego mikrogleju, szukając genów konsekwentnie podwyższonych. Jeden kandydat wyróżniał się: IFITM3, białko znane przede wszystkim z udziału w obronie komórek przed wirusami, lecz coraz częściej powiązane z zapaleniem mózgu w chorobach takich jak choroba Alzheimera czy udar.
Cząsteczkowy przełącznik, który pogarsza napady
Aby przetestować rolę IFITM3, zespół użył mysich komórek mikrogleju narażonych na bakteryjny mimikant silnie aktywujący zapalenie. Gdy poziomy IFITM3 były wysokie, komórki wydzielały dużo przekaźników zapalnych, takich jak interleukina-1β, interleukina-6 i czynnik martwicy nowotworów, oraz wykazywały więcej oznak programowanej śmierci komórkowej, w tym efektowny, porotwórczy typ zwany pyroptozą. Wyciszenie IFITM3 dawało przeciwny skutek — wyraźne zmniejszenie sygnałów zapalnych i markerów śmierci komórek. Naukowcy przeszli następnie do badań in vivo, tworząc u myszy model przewlekłych napadów i używając wirusa do obniżenia poziomu IFITM3 w mózgu. Myszy z zredukowanym IFITM3 miały łagodniejsze napady w ocenach behawioralnych, spokojniejsze zapisy czynności bioelektrycznej mózgu oraz niższe poziomy markerów zapalenia i śmierci komórek w tkance mózgowej.
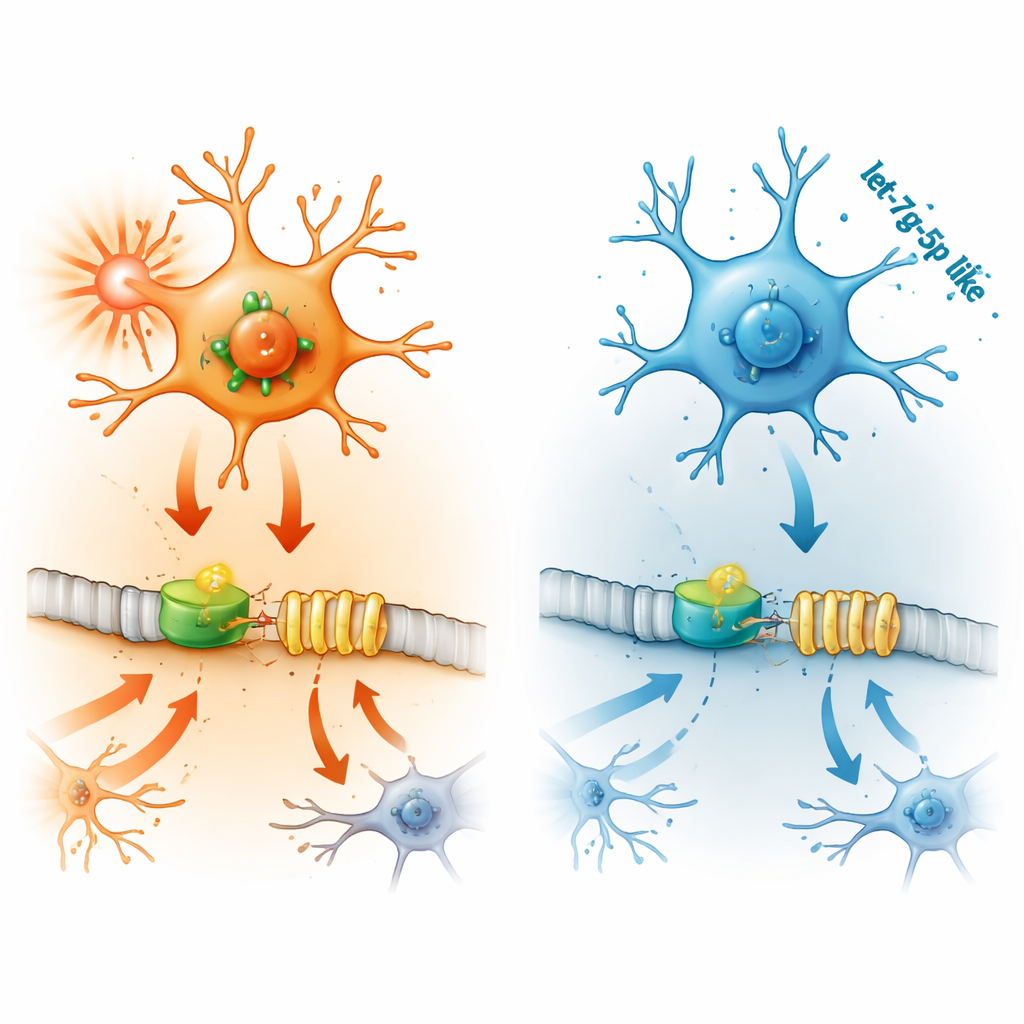
Jak cząsteczki nadrzędne włączają i wyłączają IFITM3
Dalej badacze prześledzili, jak IFITM3 jest włączany. Skupili się na STAT2, białku przekazującym sygnały od interferonów — kluczowych cząsteczek układu odpornościowego — do DNA komórki. W mikrogleju zwiększenie STAT2 podnosiło poziomy IFITM3 i nasilało zapalenie oraz śmierć komórek, podczas gdy obniżenie STAT2 działało odwrotnie. Eksperymenty z wykorzystaniem konstruków reporterowych DNA wykazały, że STAT2 wiąże się bezpośrednio z regionem kontrolnym genu IFITM3, aktywując go. U myszy z napadami STAT2 również był podwyższony w obszarach mózgu podatnych na napady, lecz wyłączenie IFITM3 nie zmieniało poziomu STAT2, co potwierdza, że STAT2 znajduje się powyżej w hierarchii jako główny przełącznik.
Małe RNA, które włącza hamulec
Ostatnim ogniwem łańcucha jest let-7g-5p, drobna regulatorowa cząsteczka RNA. Mikrorna, takie jak let-7g-5p, precyzyjnie modulują aktywność genów, przyczepiając się do docelowych komunikatów i blokując ich translację na białko. W zapalonym mikrogleju i mózgach myszy z epilepsją poziomy let-7g-5p spadały. Testy laboratoryjne wykazały, że let-7g-5p wiąże się bezpośrednio z końcowym odcinkiem informacyjnego RNA STAT2, obniżając produkcję STAT2. Gdy badacze dodali dodatkowe let-7g-5p do mikrogleju, poziomy STAT2 i IFITM3 spadły, sygnały zapalne zmalały, a śmierć komórek zwolniła. Zablokowanie let-7g-5p miało odwrotny skutek — który jednak można było odwrócić przez jednoczesne wyciszenie STAT2, dowodząc, że let-7g-5p chroni przez celowanie w STAT2, a pośrednio w IFITM3.
Co to może znaczyć dla osób z epilepsją
Razem te wyniki układają prostą, ale istotną opowieść: STAT2 włącza IFITM3 w mikrogleju, co zwiększa zapalenie mózgu i śmierć komórek, pogarszając napady, podczas gdy let-7g-5p działa jako naturalny hamulec tego procesu. W epilepsji ten hamulec wydaje się zawodzić, pozwalając zapaleniu wymknąć się spod kontroli. Choć wyniki pochodzą z badań komórkowych i na myszach, a nie bezpośrednio od pacjentów, wskazują oś let-7g-5p/STAT2/IFITM3 jako obiecujący nowy cel. Przyszłe terapie mogłyby dążyć do zwiększenia let-7g-5p albo zablokowania STAT2 lub IFITM3 — nie po to, by wyleczyć epilepsję raz na zawsze, lecz by ochłodzić środowisko zapalne, które sprzyja utrzymywaniu się napadów i oporności na standardowe leki.
Cytowanie: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Słowa kluczowe: epilepsja, neurozapalenie, mikroglej, IFITM3, microRNA let-7g-5p