Clear Sky Science · ru
Нейровоспаление при эпилепсии, опосредованное IFITM3, регулируется осью let-7g-5p/STAT2
Почему воспаление мозга важно при эпилепсии
Эпилепсией страдают десятки миллионов людей во всем мире, и примерно у каждого третьего современные препараты не полностью контролируют приступы. Всё больше ученых полагают, что хроническое воспаление внутри мозга способствует учащению приступов и усложняет их лечение. В этом исследовании изучается недавно обнаруженная цепочка молекул в иммунных клетках мозга, которая, по-видимому, либо разжигает, либо тушит воспалительный ответ, сопровождающий эпилепсию. Понимание этой цепочки может открыть путь к будущим методам лечения, направленным на успокоение собственного иммунного ответа мозга, а не только на подавление электрической активности.
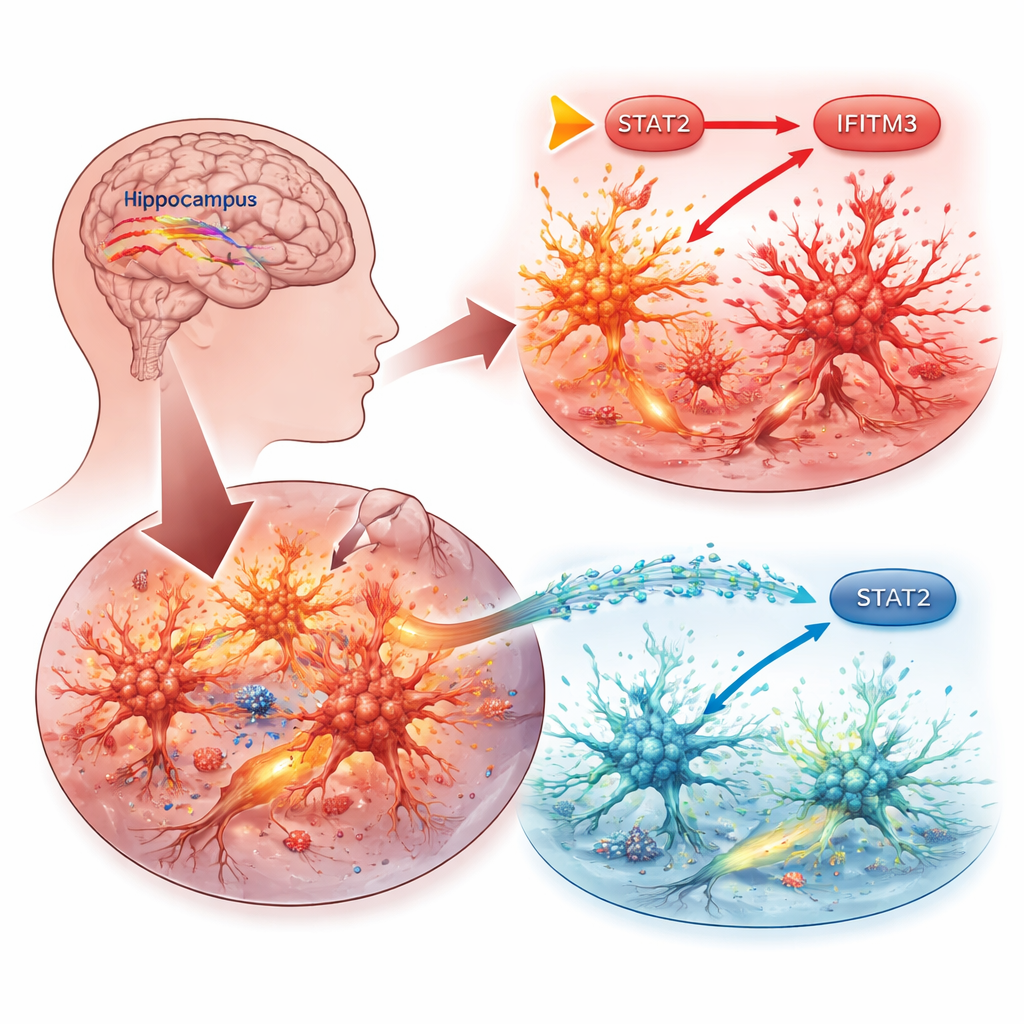
Иммунные клетки мозга в центре внимания
Работа сосредоточена на микроглии — постоянных иммунных клетках мозга. Когда происходят приступы или другие повреждения, микроглия переходит в активированное состояние и выделяет воспалительные вещества, которые могут повреждать соседние нейроны и снижать порог для новых приступов. Исследователи спросили, какие именно молекулы внутри микроглии приводят к этому вредному кругу. Они начали с анализа общедоступных генетических баз данных по экспериментальным моделям эпилепсии у мышей и воспаленной микроглии, ища гены, которые постоянно повышены. Одним из кандидатов оказался IFITM3 — белок, известный прежде всего как фактор анти- вирусной защиты клеток, но всё чаще связываемый с воспалением мозга при таких состояниях, как болезнь Альцгеймера и инсульт.
Молекулярный переключатель, усугубляющий приступы
Чтобы проверить роль IFITM3, команда использовала культуры микроглии мышей, обработанные бактериальным имитатором, который сильно активирует воспаление. При высоком уровне IFITM3 клетки выбрасывали многочисленные провоспалительные медиаторы, такие как интерлейкин-1β, интерлейкин-6 и фактор некроза опухоли, и демонстрировали больше признаков программируемой гибели клеток, включая пироптоз — огнеподобный вариант с образованием пор. Подавление IFITM3 давало обратный эффект: резко снижались как воспалительные сигналы, так и маркеры гибели клеток. Затем ученые перешли к исследованиям in vivo, создав хроническую модель судорог у мышей и применив вирус для снижения экспрессии IFITM3 в мозге. У мышей с пониженным IFITM3 приступы были мягче по поведенческим шкалам, ЭЭГ показывала более спокойную активность, а в тканях мозга снижались уровни воспалительных и маркеров гибели клеток.
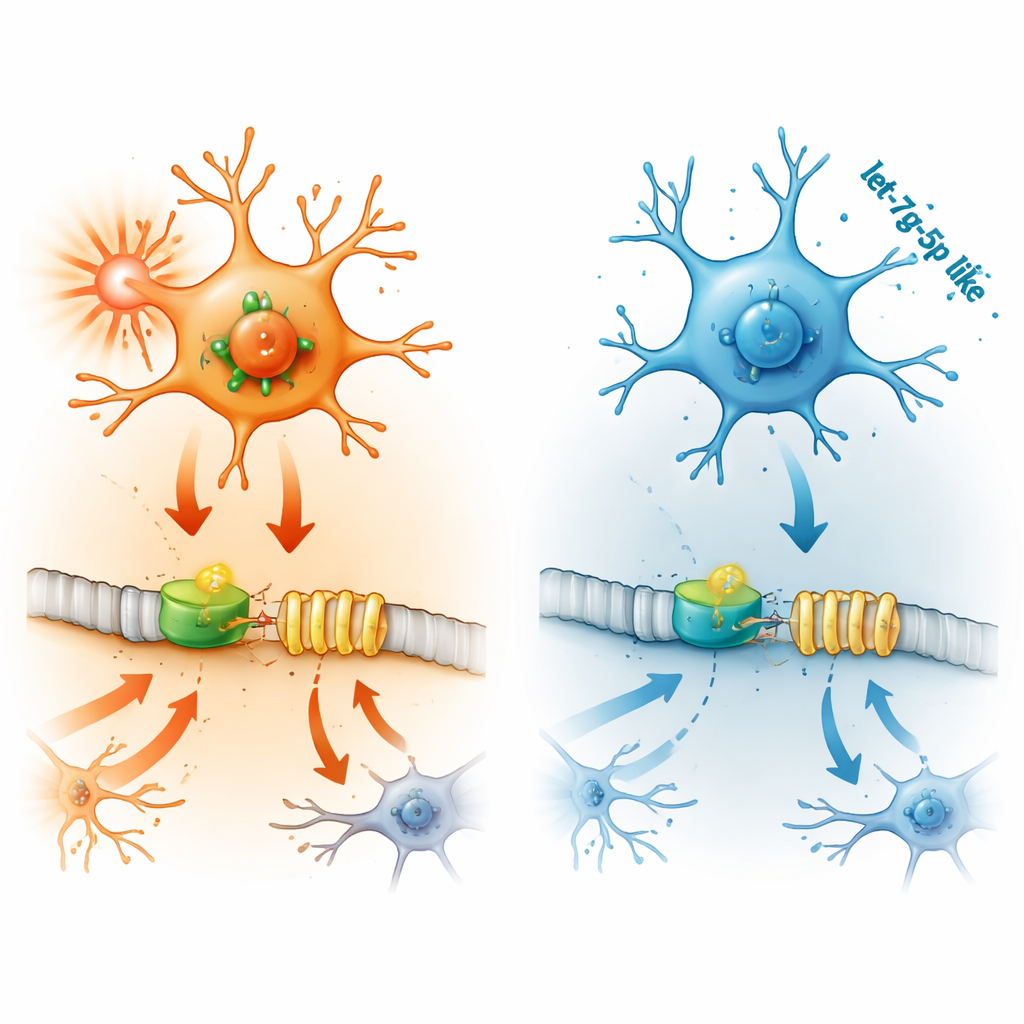
Как вышестоящие молекулы включают и выключают IFITM3
Далее исследователи проследили, как включается IFITM3. Они сосредоточились на STAT2 — белке, который передает сигналы от интерферонов, ключевых иммунных молекул, к ДНК клетки. В микроглии повышение STAT2 увеличивало уровень IFITM3 и усиливало воспаление и гибель клеток, тогда как снижение STAT2 давало противоположный эффект. Эксперименты с ДНК-репортерами показали, что STAT2 прямо связывается с регуляторной областью гена IFITM3 и активирует его. В мозге эпилептических мышей STAT2 также был повышен в областях, склонных к приступам, но подавление IFITM3 не влияло на уровень STAT2, что подтверждает положение STAT2 как вышестоящего «мастер-переключателя».
Маленькая РНК, которая нажимает на тормоза
Последнее звено цепочки — let-7g-5p, крошечная регуляторная РНК. МикроРНК вроде let-7g-5p тонко регулируют активность генов, связываясь с целевыми сообщениями и блокируя их трансляцию в белок. В воспаленной микроглии и в мозге эпилептических мышей уровни let-7g-5p снижались. Лабораторные тесты показали, что let-7g-5p прямо связывается с 3'-участком матрицы STAT2, снижая его синтез. При добавлении дополнительной let-7g-5p в микроглию уровни STAT2 и IFITM3 падали, воспалительные сигналы уменьшались, а гибель клеток замедлялась. Блокирование let-7g-5p давало противоположный эффект — но он устранялся одновременным подавлением STAT2, что доказывает: let-7g-5p защищает, нацеливаясь на STAT2 и, опосредованно, на IFITM3.
Что это может значить для людей с эпилепсией
В совокупности эти результаты рисуют простую, но убедительную картину: STAT2 включает IFITM3 в микроглии, что усиливает воспаление мозга и гибель клеток и тем самым усугубляет приступы, тогда как let-7g-5p действует как естественный тормоз этого процесса. При эпилепсии этот тормоз, по-видимому, ослабевает, позволяя воспалению разрастаться. Хотя данные получены на клетках и мышах, а не на пациентах, они выделяют ось let-7g-5p/STAT2/IFITM3 как перспективную мишень. Будущие терапии могли бы стремиться повысить let-7g-5p или блокировать STAT2 либо IFITM3 — не для того, чтобы полностью излечить эпилепсию, но чтобы охладить воспалительную среду, которая способствует сохранению приступов и их устойчивости к стандартным лекарствам.
Цитирование: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Ключевые слова: эпилепсия, нейровоспаление, микроглия, IFITM3, микроРНК let-7g-5p