Clear Sky Science · pt
Neuroinflamação mediada por IFITM3 na epilepsia regulada pelo eixo let-7g-5p/STAT2
Por que a inflamação cerebral importa na epilepsia
A epilepsia afeta dezenas de milhões de pessoas no mundo e, para cerca de um em cada três, os medicamentos atuais não controlam completamente as crises. Cientistas suspeitam cada vez mais que inflamação crônica dentro do cérebro contribui para tornar as crises mais frequentes e mais difíceis de tratar. Este estudo explora uma cadeia de moléculas recentemente descoberta nas células imunes do cérebro que parece amplificar — ou atenuar — as chamas inflamatórias que acompanham a epilepsia. Compreender essa cadeia pode abrir caminho para tratamentos futuros que atuem acalmando a resposta imune do próprio cérebro, em vez de apenas reduzir a atividade elétrica.
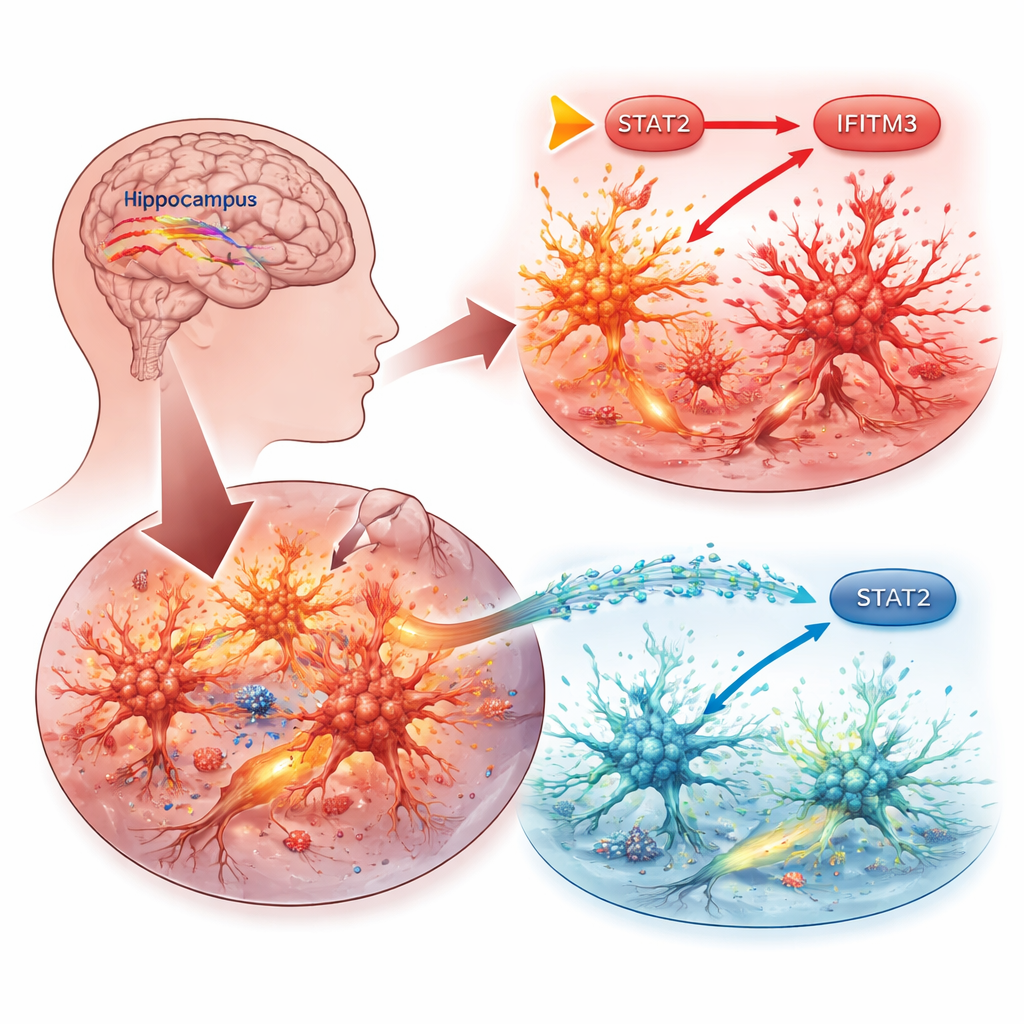
As células imunes do cérebro no centro das atenções
O trabalho foca nas microglias, as células imunes residentes do cérebro. Quando crises ou outras lesões ocorrem, as microglias entram em um estado ativado, liberando substâncias inflamatórias que podem danificar neurônios próximos e reduzir o limiar para novas crises. Os pesquisadores perguntaram quais moléculas específicas dentro das microglias impulsionam esse ciclo prejudicial. Começaram garimpando bancos de dados genéticos públicos de modelos animais de epilepsia e microglias inflamadas, buscando genes consistentemente aumentados. Um candidato se destacou: IFITM3, uma proteína mais conhecida por ajudar células a combater vírus, mas cada vez mais associada à inflamação cerebral em condições como Alzheimer e AVC.
Um interruptor molecular que piora as crises
Para testar o papel do IFITM3, a equipe usou células microgliais de camundongo expostas a um mimético bacteriano que ativa fortemente a inflamação. Quando os níveis de IFITM3 estavam elevados, as células liberaram mensageiros inflamatórios como interleucina-1β, interleucina-6 e fator de necrose tumoral, e mostraram mais sinais de morte celular programada, incluindo um tipo inflamado e por formação de poros chamado piroptose. Silenciar o IFITM3 teve o efeito oposto, reduzindo fortemente os sinais inflamatórios e os marcadores de morte celular. Os cientistas então avançaram para animais vivos, criando um modelo de convulsões crônicas em camundongos e usando um vírus para reduzir o IFITM3 no cérebro. Camundongos com IFITM3 reduzido apresentaram crises mais brandas em escalas comportamentais, registros eletroencefalográficos mais calmos e níveis mais baixos de marcadores inflamatórios e de morte celular no tecido cerebral.
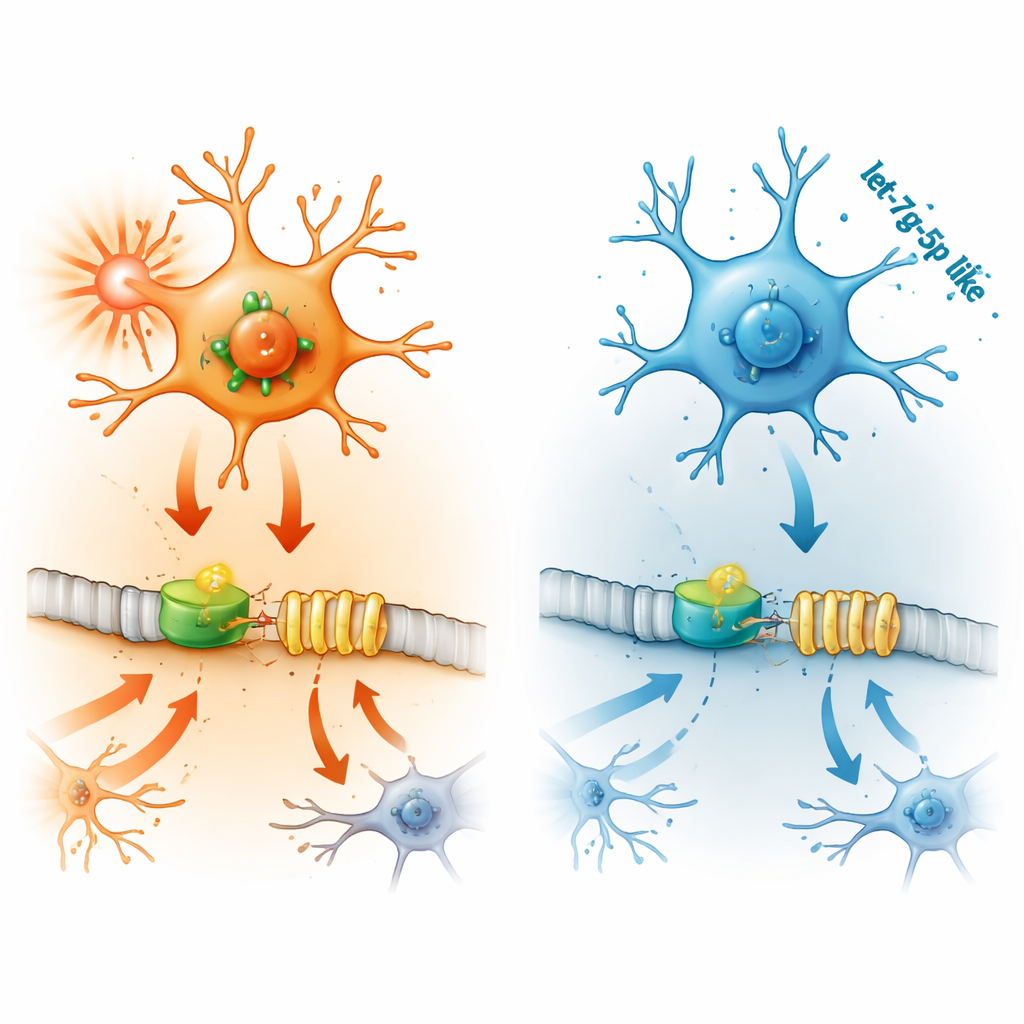
Como moléculas a montante ligam e desligam o IFITM3
Em seguida, os pesquisadores rastrearam como o IFITM3 é ativado. Eles se concentraram no STAT2, uma proteína que transmite sinais de interferons — moléculas-chave do sistema imune — ao DNA da célula. Nas microglias, aumentar o STAT2 elevou os níveis de IFITM3 e intensificou a inflamação e a morte celular, enquanto reduzir o STAT2 teve o efeito inverso. Experimentos usando construtos repórter de DNA mostraram que o STAT2 se liga diretamente à região de controle do gene IFITM3 para ativá-lo. Em camundongos epilépticos, o STAT2 também estava elevado em regiões cerebrais propensas a crises, mas desligar o IFITM3 não alterou o STAT2 em si, confirmando que o STAT2 está a montante como um interruptor mestre.
Um pequeno RNA que aciona os freios
O elo final na cadeia é o let-7g-5p, uma pequena molécula de RNA reguladora. MicroRNAs como o let-7g-5p ajustam finamente a atividade gênica ao se ligar a mensagens alvo e bloquear sua tradução em proteína. Em microglias inflamadas e em cérebros de camundongos epilépticos, os níveis de let-7g-5p caíram. Testes laboratoriais mostraram que o let-7g-5p se liga diretamente à região 3' da mensagem genética do STAT2, reduzindo sua produção. Quando os pesquisadores adicionaram let-7g-5p extra às microglias, os níveis de STAT2 e IFITM3 diminuíram, os sinais inflamatórios caíram e a morte celular desacelerou. Bloquear o let-7g-5p provocou o efeito oposto — mas isso pôde ser revertido silenciando-se simultaneamente o STAT2, provando que o let-7g-5p protege ao mirar no STAT2 e, em sequência, no IFITM3.
O que isso pode significar para pessoas com epilepsia
Em conjunto, esses achados delineiam uma história simples, porém poderosa: o STAT2 ativa o IFITM3 nas microglias, o que aumenta a inflamação cerebral e a morte celular, agravando as crises, enquanto o let-7g-5p atua como um freio natural nesse processo. Na epilepsia, esse freio parece falhar, permitindo que a inflamação se descontrole. Embora esses resultados venham de células e de modelos animais, e não de pacientes, eles destacam o eixo let-7g-5p/STAT2/IFITM3 como um novo alvo promissor. Terapias futuras poderiam visar aumentar o let-7g-5p ou bloquear o STAT2 ou o IFITM3 — não para curar a epilepsia por completo, mas para resfriar o ambiente inflamatório que ajuda as crises a persistirem e a resistirem aos medicamentos padrão.
Citação: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Palavras-chave: epilepsia, neuroinflamação, microglia, IFITM3, microRNA let-7g-5p