Clear Sky Science · sv
IFITM3-medierad neuroinflammation vid epilepsi reglerad av let-7g-5p/STAT2-axeln
Varför hjärnans inflammation spelar roll vid epilepsi
Epilepsi drabbar tiotals miljoner människor världen över, och för ungefär en av tre ger dagens läkemedel inte fullständig anfallsfrihet. Forskare misstänker i allt större utsträckning att kronisk inflammation i hjärnan bidrar till att göra anfallen både vanligare och svårare att behandla. Denna studie undersöker en nyligen upptäckt kedja av molekyler i hjärnans immunceller som verkar antingen elda på eller dämpa de inflammatoriska processer som följer med epilepsi. Att förstå denna kedja kan öppna för framtida behandlingar som verkar genom att lugna hjärnans egen immunreaktion snarare än att enbart dämpa elektrisk aktivitet.
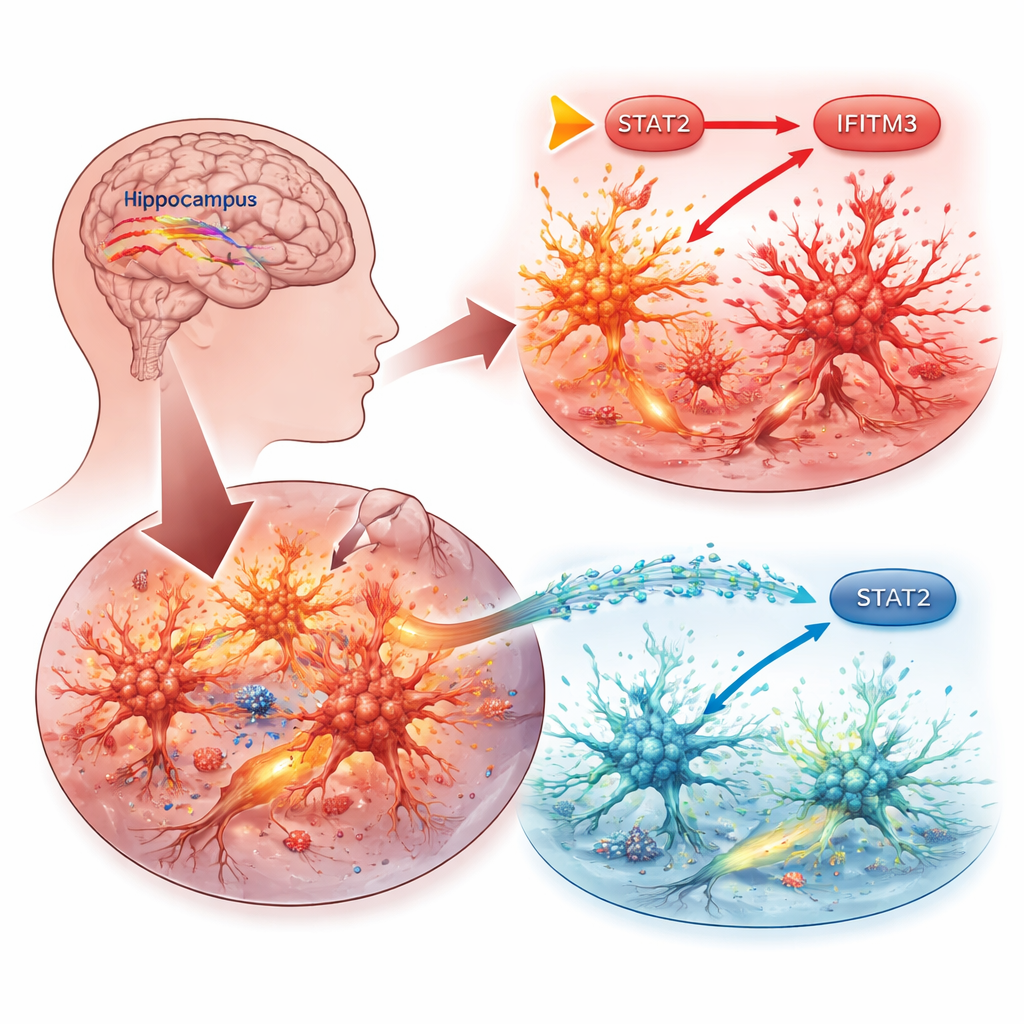
Hjärnans immunceller i rampljuset
Arbetet fokuserar på mikroglia, hjärnans egna immunceller. När anfall eller annan skada inträffar går mikroglia in i ett aktiverat tillstånd och släpper ut inflammatoriska ämnen som kan skada närliggande nervceller och sänka tröskeln för fler anfall. Forskarna frågade vilka specifika molekyler inne i mikroglia som driver denna skadliga cykel. De började med att undersöka offentliga genetiska databaser från musmodeller för epilepsi och inflammerad mikroglia för att hitta gener som konsekvent var uppreglerade. En kandidat stack ut: IFITM3, ett protein mest känt för att hjälpa celler att stå emot virus men som i ökande grad kopplas till hjärninflammation vid tillstånd som Alzheimers sjukdom och stroke.
En molekylär av/på-switch som förvärrar anfall
För att pröva IFITM3:s roll använde teamet musmikroglia som exponerades för en bakteriemimiker som kraftigt aktiverar inflammation. När IFITM3-nivåerna var höga släppte cellerna ut inflammatoriska budbärare som interleukin-1β, interleukin-6 och tumörnekrosfaktor, och visade fler tecken på programmerad celldöd, inklusive en het, porbildande form kallad pyroptos. Att tysta IFITM3 gav motsatt effekt och minskade kraftigt både inflammatoriska signaler och markörer för celldöd. Forskarna gick sedan vidare till levande djur genom att skapa en modell för kroniska anfall hos möss och använda ett virus för att sänka IFITM3 i hjärnan. Möss med reducerat IFITM3 uppvisade lindrigare anfall i beteendeskalor, lugnare hjärnvågsregistreringar och lägre nivåer av inflammations- och celldödsmarkörer i hjärnvävnad.
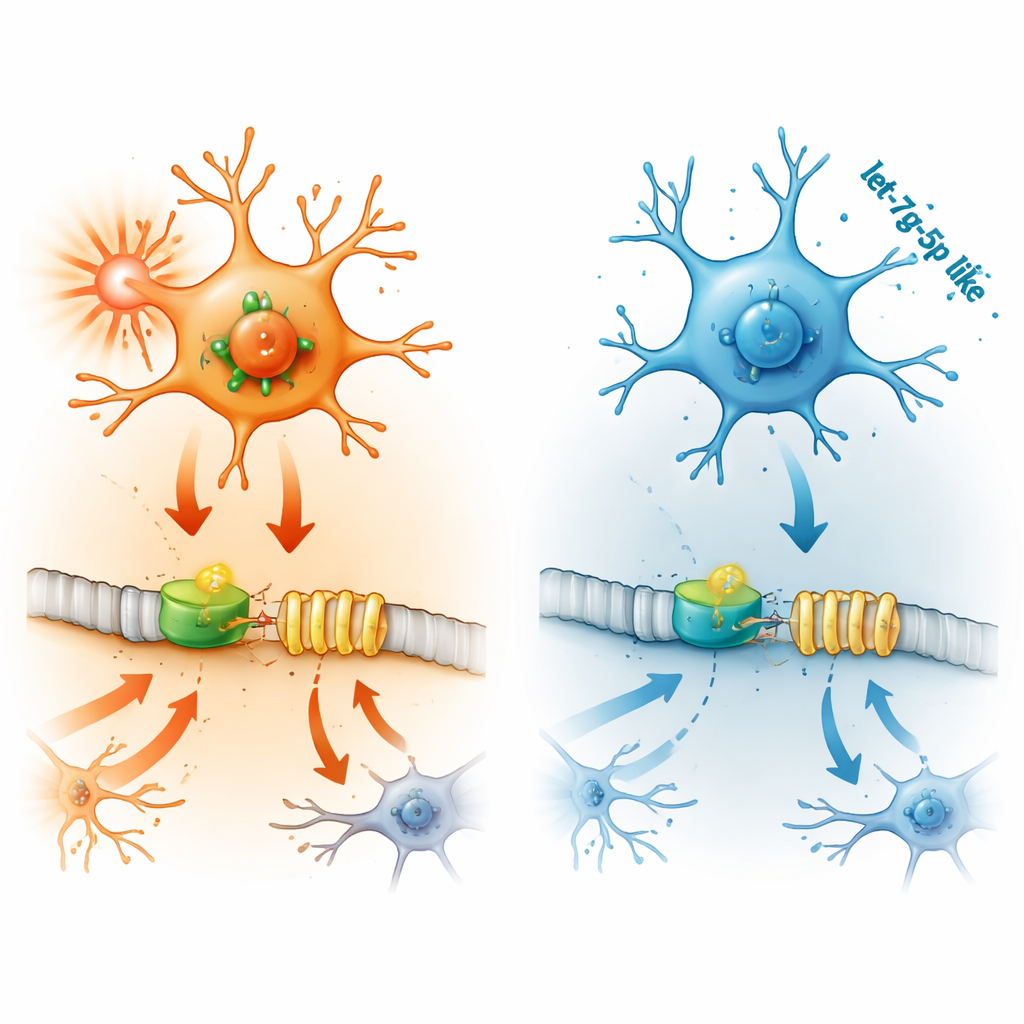
Hur upstream-molekyler slår på och av IFITM3
Nästa steg var att kartlägga hur IFITM3 aktiveras. Forskarna fokuserade på STAT2, ett protein som för signaler från interferoner — nyckelimmune molekyler — till cellens DNA. I mikroglia ökade STAT2 IFITM3-nivåerna och förvärrade inflammation och celldöd, medan nedreglering av STAT2 gav motsatt resultat. Experiment med DNA-rapportorkonstruktioner visade att STAT2 binder direkt till kontrollregionen för IFITM3-genen för att aktivera den. I epileptiska möss var STAT2 också förhöjt i hjärnregioner som är benägna att drabbas av anfall, men att stänga av IFITM3 ändrade inte STAT2 självt, vilket bekräftar att STAT2 ligger uppströms som en huvudomkopplare.
En liten RNA-molekyl som bromsar processen
Den sista länken i kedjan är let-7g-5p, ett litet reglerande RNA. MikroRNA som let-7g-5p finjusterar genaktivitet genom att binda till målmolekylernas budskap och blockera deras översättning till protein. I inflammerad mikroglia och i hjärnor från epileptiska möss sjönk nivåerna av let-7g-5p. Laboratorietester visade att let-7g-5p binder direkt till stjärtregionen av STAT2:s genetiska budskap och minskar STAT2-produktionen. När forskarna tillsatte extra let-7g-5p till mikroglia föll STAT2- och IFITM3-nivåerna, inflammationssignaler minskade och celldöd avtog. Att blockera let-7g-5p gav motsatt effekt — men detta kunde räddas genom samtidig nedtystning av STAT2, vilket bevisar att let-7g-5p skyddar genom att rikta in sig på STAT2 och därigenom IFITM3.
Vad detta kan innebära för personer med epilepsi
Tillsammans målar resultaten upp en enkel men kraftfull berättelse: STAT2 slår på IFITM3 i mikroglia, vilket ökar hjärninflammation och celldöd och förvärrar anfall, medan let-7g-5p fungerar som en naturlig broms på denna process. Vid epilepsi verkar den bromsen svikta, vilket tillåter inflammationen att skena. Även om dessa fynd kommer från celler och musmodeller snarare än från patienter, pekar de på let-7g-5p/STAT2/IFITM3-axeln som ett lovande nytt mål. Framtida terapier skulle kunna syfta till att öka let-7g-5p eller blockera STAT2 eller IFITM3, inte för att bota epilepsi helt, utan för att dämpa den inflammatoriska miljö som bidrar till att anfallen kvarstår och blir resistenta mot standardläkemedel.
Citering: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Nyckelord: epilepsi, neuroinflammation, mikroglia, IFITM3, mikroRNA let-7g-5p