Clear Sky Science · fr
Neuroinflammation médiée par IFITM3 dans l’épilepsie régulée par l’axe let-7g-5p/STAT2
Pourquoi l’inflammation cérébrale importe en épilepsie
L’épilepsie touche des dizaines de millions de personnes dans le monde et, pour environ un patient sur trois, les traitements actuels ne contrôlent pas complètement les crises. Les chercheurs suspectent de plus en plus qu’une inflammation chronique au sein du cerveau favorise une plus grande fréquence des crises et rend leur contrôle plus difficile. Cette étude explore une chaîne de molécules récemment identifiée dans les cellules immunitaires du cerveau qui semble attiser — ou apaiser — les feux inflammatoires associés à l’épilepsie. Mieux comprendre cette chaîne pourrait ouvrir la voie à des traitements futurs visant à calmer la réponse immunitaire cérébrale elle-même plutôt qu’à uniquement réduire l’activité électrique.
Les cellules immunitaires du cerveau sous les projecteurs
Le travail se concentre sur les microglies, les cellules immunitaires résidentes du cerveau. Lorsqu’une crise ou une lésion survient, les microglies passent à un état activé et libèrent des molécules inflammatoires qui peuvent endommager les neurones voisins et abaisser le seuil des crises ultérieures. Les chercheurs ont cherché quelles molécules spécifiques au sein des microglies alimentent ce cercle vicieux. Ils ont commencé par exploiter des bases de données génétiques publiques issues de modèles murins d’épilepsie et de microglies enflammées, à la recherche de gènes systématiquement surexprimés. Un candidat s’est distingué : IFITM3, une protéine surtout connue pour aider les cellules à se défendre contre les virus mais de plus en plus associée à l’inflammation cérébrale dans des affections comme la maladie d’Alzheimer et l’AVC.
Un interrupteur moléculaire qui aggrave les crises
Pour tester le rôle d’IFITM3, l’équipe a utilisé des microglies de souris exposées à un mimétique bactérien qui active fortement l’inflammation. Lorsque les niveaux d’IFITM3 étaient élevés, les cellules sécrétaient des médiateurs inflammatoires tels que l’interleukine‑1β, l’interleukine‑6 et le facteur de nécrose tumorale, et présentaient davantage de signes de mort cellulaire programmée, y compris un type pyrotechnique et poreux appelé pyroptose. Silencer IFITM3 avait l’effet inverse, réduisant nettement les signaux inflammatoires et les marqueurs de mort cellulaire. Les chercheurs sont ensuite passés à des animaux vivants, en créant un modèle de crises chroniques chez la souris et en utilisant un virus pour diminuer IFITM3 dans le cerveau. Les souris avec IFITM3 réduit présentaient des crises plus légères selon les échelles comportementales, des enregistrements électroencéphalographiques plus calmes et des niveaux plus faibles de marqueurs inflammatoires et de mort cellulaire dans le tissu cérébral.
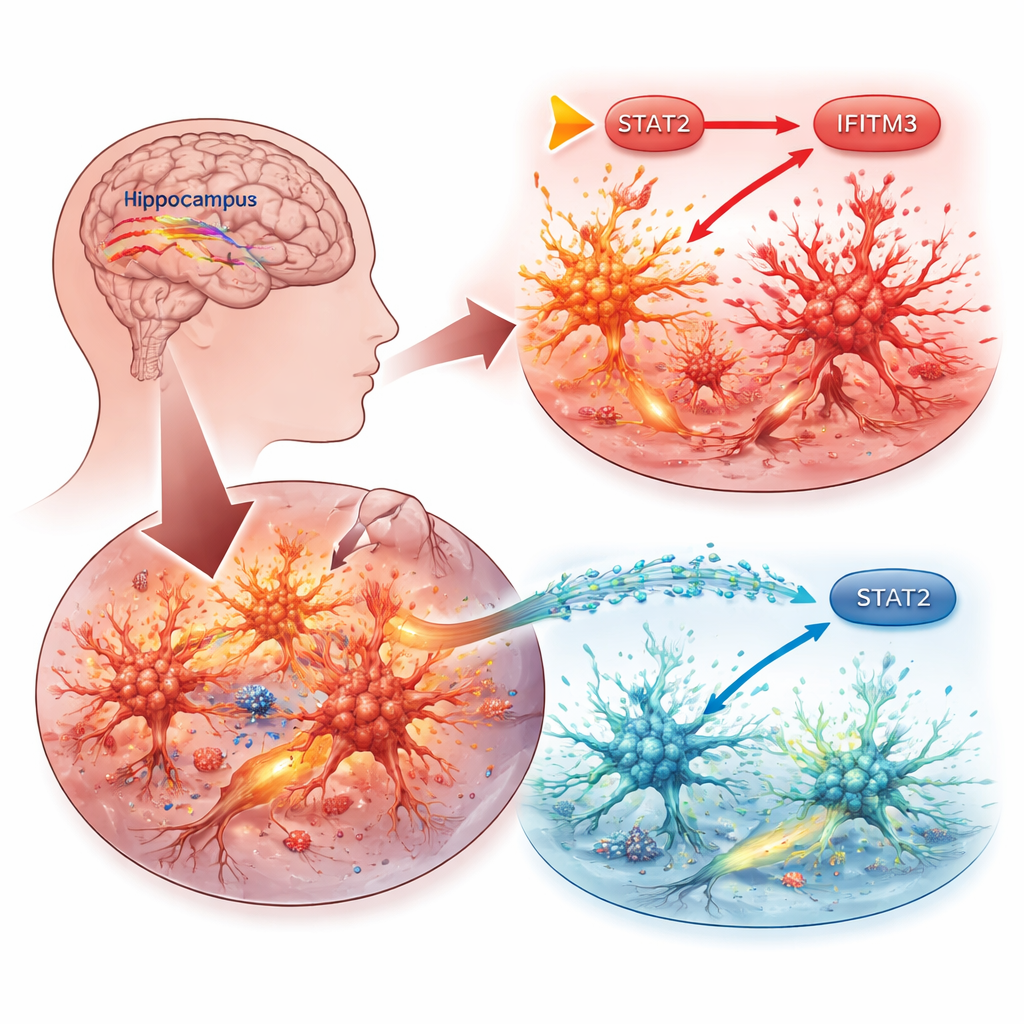
Comment des molécules en amont activent ou éteignent IFITM3
Ensuite, les chercheurs ont retracé comment IFITM3 est activé. Ils se sont focalisés sur STAT2, une protéine qui transmet les signaux des interférons — des molécules clés du système immunitaire — jusqu’à l’ADN de la cellule. Dans les microglies, l’augmentation de STAT2 élevait les niveaux d’IFITM3 et intensifiait l’inflammation et la mort cellulaire, tandis que l’inhibition de STAT2 produisait l’effet inverse. Des expériences utilisant des constructions rapporteurs d’ADN ont montré que STAT2 se lie directement à la région de contrôle du gène IFITM3 pour l’activer. Chez des souris épileptiques, STAT2 était également élevé dans les régions cérébrales sujettes aux crises, mais l’extinction d’IFITM3 n’affectait pas STAT2 lui‑même, confirmant que STAT2 se situe en amont en tant qu’interrupteur maître.
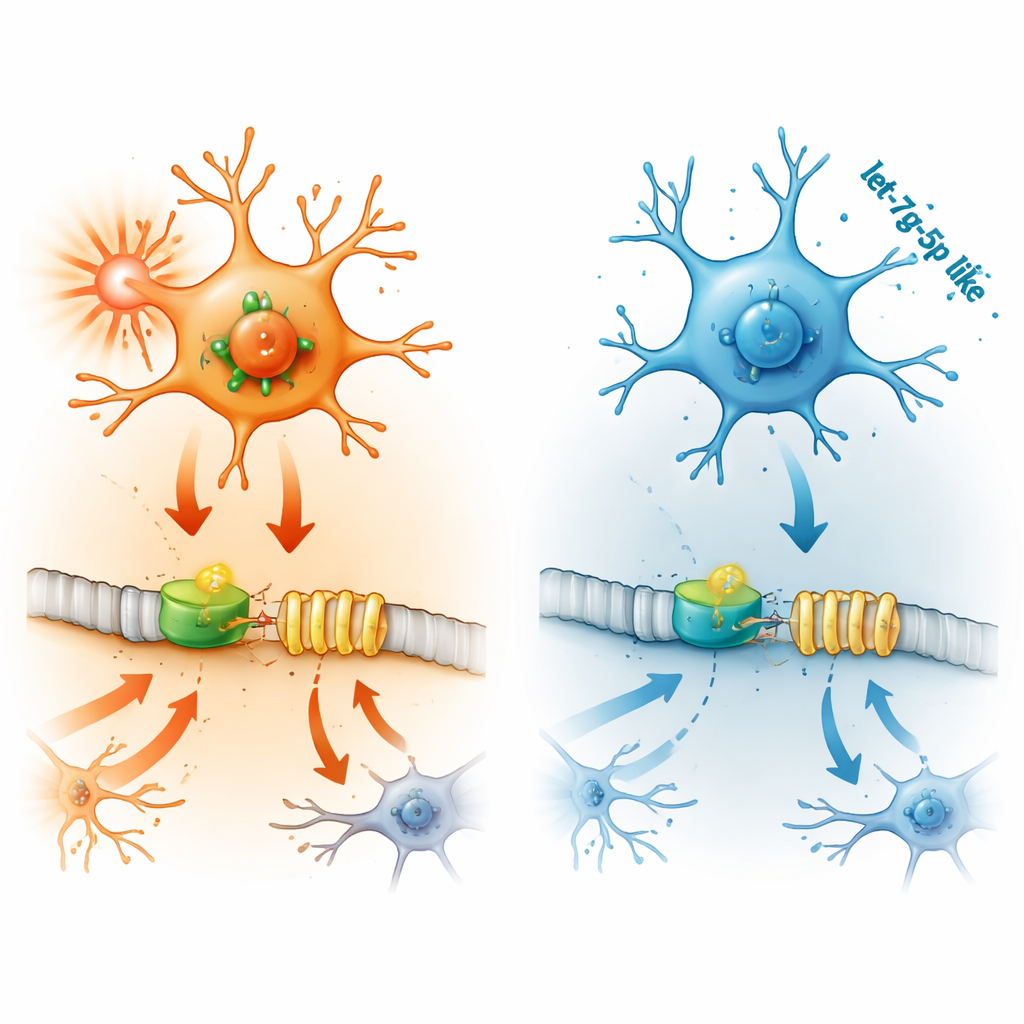
Un petit ARN qui freine le processus
Le dernier maillon de la chaîne est let-7g-5p, un petit ARN régulateur. Les microARN comme let-7g-5p ajustent finement l’activité génique en se liant aux messages ciblés et en bloquant leur traduction en protéines. Dans les microglies enflammées et les cerveaux de souris épileptiques, les niveaux de let-7g-5p diminuaient. Des tests en laboratoire ont montré que let-7g-5p se lie directement à la région terminale du messager de STAT2, réduisant la production de STAT2. Lorsque les chercheurs ont apporté un excès de let-7g-5p aux microglies, STAT2 et IFITM3 ont chuté, les signaux inflammatoires ont diminué et la mort cellulaire a ralenti. Bloquer let-7g-5p produisait l’effet inverse — mais ceci pouvait être compensé en silenceant simultanément STAT2, prouvant que let-7g-5p protège en ciblant STAT2 et, par conséquent, IFITM3.
Ce que cela pourrait signifier pour les personnes épileptiques
Ensemble, ces résultats tracent un récit simple mais puissant : STAT2 active IFITM3 dans les microglies, ce qui amplifie l’inflammation cérébrale et la mort cellulaire, aggravant les crises, tandis que let-7g-5p agit comme un frein naturel à ce processus. Dans l’épilepsie, ce frein semble défaillant, laissant l’inflammation s’emballer. Bien que ces résultats proviennent de cellules et de souris plutôt que de patients, ils mettent en lumière l’axe let-7g-5p/STAT2/IFITM3 comme une cible prometteuse. Des thérapies futures pourraient viser à augmenter let-7g-5p ou à bloquer STAT2 ou IFITM3, non pas pour guérir l’épilepsie de manière définitive, mais pour refroidir l’environnement inflammatoire qui favorise la persistance des crises et la résistance aux médicaments standards.
Citation: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Mots-clés: épilepsie, neuroinflammation, microglie, IFITM3, microARN let-7g-5p