Clear Sky Science · he
דלקת עצבית המתווכת על ידי IFITM3 באפילפסיה המווסתת באמצעות ציר let-7g-5p/STAT2
מדוע דלקת במוח חשובה באפילפסיה
אפילפסיה משפיעה על עשרות מיליוני אנשים ברחבי העולם, וכשאחד מכל שלושה חולים, התרופות הקיימות אינן שולטות לחלוטין בהתקפים. מדענים חושדים יותר ויותר כי דלקת כרונית בתוך המוח תורמת לכך שההתקפים הופכים תכופים וקשים יותר לטיפול. המחקר הזה בוחן שרשרת מולקולרית חדשה שהתגלתה בתאי החיסון של המוח ונראית כמזינה — או מרגיעה — את הלהבות הדלקתיות המלווים אפילפסיה. הבנת השרשרת הזו עשויה לפתוח דלת לטיפולים עתידיים שפועלים על ידי הרגעת תגובת החיסון העצמית של המוח במקום רק לדכא פעילות חשמלית.
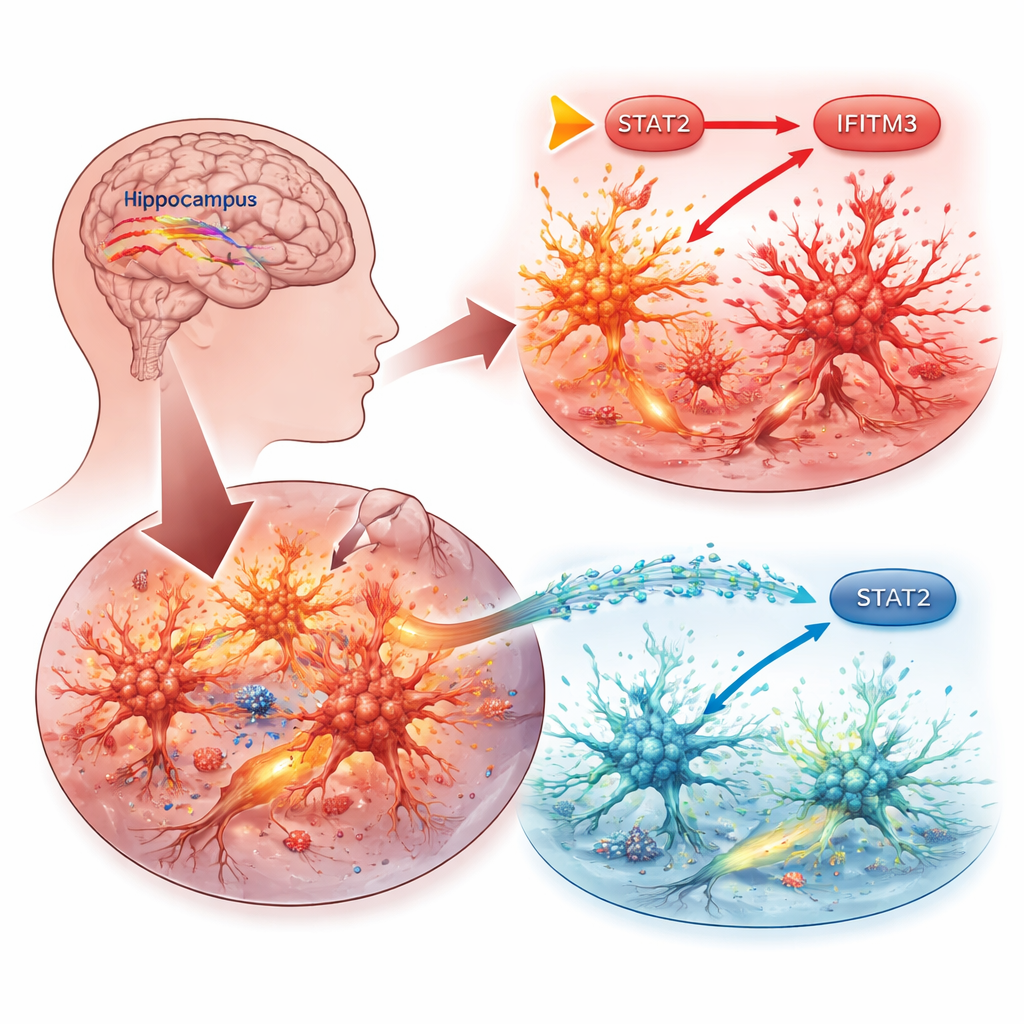
תאי החיסון של המוח בזירה
המחקר מתמקד במיקרוגליה, תאי החיסון המקומיים במוח. כשהתקפים או פגיעות אחרות פוגעים, המיקרוגליה עוברת למצב מזורז ומשחררת חומרים דלקתיים שיכולים לפגוע בתאי העצב הסמוכים ולהוריד את הסף להתקפים נוספים. החוקרים שאלו אילו מולקולות ספציפיות בתוך המיקרוגליה מניעות את המעגל המזיק הזה. הם התחילו בכריית מאגרי נתונים גנטיים ציבוריים ממודלים של עכברים עם אפילפסיה ומיקרוגליה דלקתית, בחיפוש גנים שהיו מופעלים בעקביות. מועמד אחד בלט: IFITM3, חלבון המוכר היטב בסיוע להגנה על תאים מפני וירוסים אך שנמצא יותר ויותר קשור לדלקת במוח במצבים כמו מחלת אלצהיימר ושבץ.
מנגנון מולקולרי שמחריף התקפים
כדי לבדוק את תפקידה של IFITM3, הצוות השתמש בתאי מיקרוגליה מעכברים שחושפו להם דמות חיידקית שמפעילה דלקת בעוצמה גבוהה. כאשר רמות IFITM3 היו גבוהות, התאים שחררו כמות גדולה של מוליכים דלקתיים כגון אינטרלוקין-1β, אינטרלוקין-6 והגורם הנפחי של הגידול, והראו סימנים מוגברים של מוות תאי מתוכנת, כולל סוג אלים היוצר נקבים בממברנה שנקרא פיירופטוזה. השתקת IFITM3 הביאה לאפקט ההפוך, וצמצמה באופן ניכר אותות דלקת וסימני מוות תאי. לאחר מכן המדענים עברו לחיות חיות, יצרו מודל התקפים כרוניים בעכברים והשתמשו בנגיף כדי להוריד את IFITM3 במוח. עכברים עם IFITM3 מופחת הפגינו התקפים מתונים יותר על סולמות התנהגותיים, הקלטות גל-מוח רגועות יותר ורמות נמוכות יותר של סמני דלקת ומוות תאי ברקמת המוח.
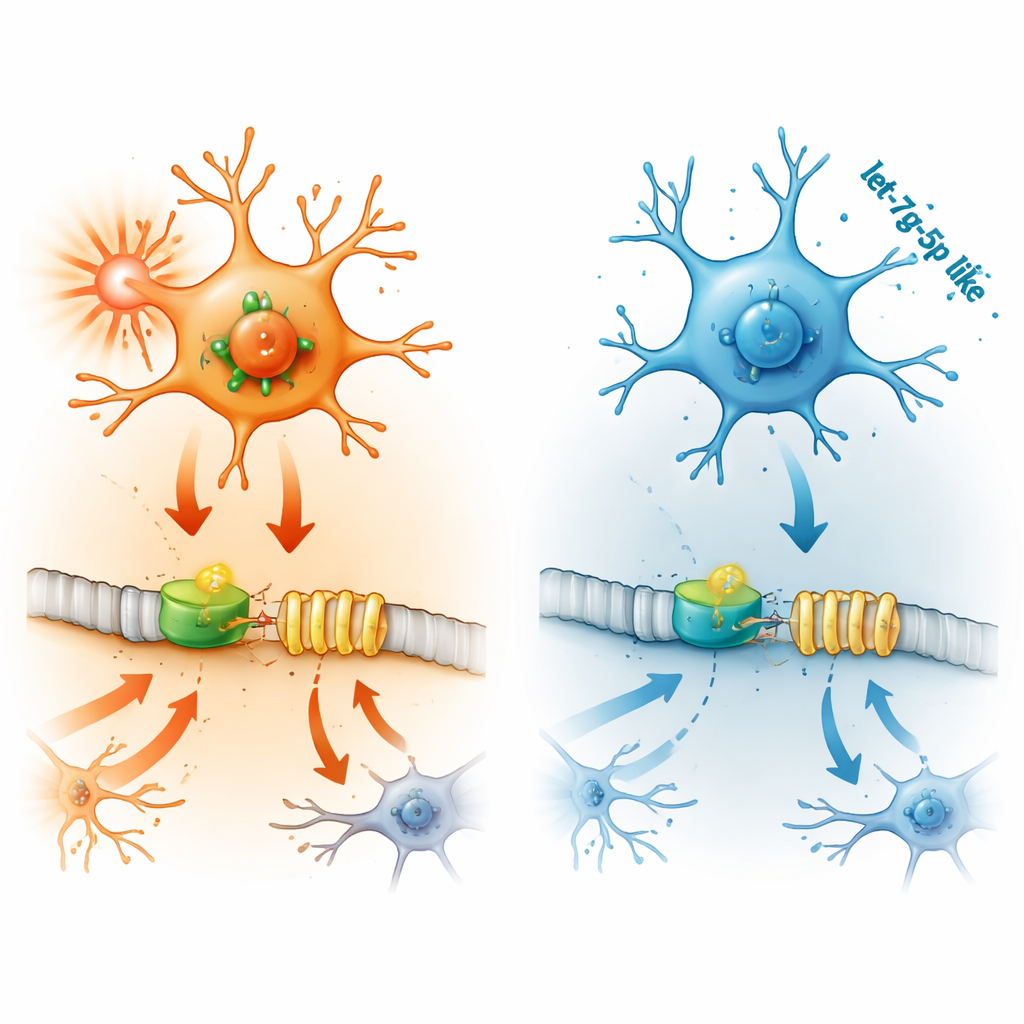
כיצד מולקולות עליונות מפעילות או מכבות את IFITM3
בהמשך עקבו החוקרים כיצד IFITM3 מועלה. הם התמקדו ב-STAT2, חלבון שמעביר אותות מאינטרפרונים — מולקולות מפתח במערכת החיסון — אל הדנ״א של התא. במיקרוגליה, הגברה של STAT2 העלתה את רמות IFITM3 והעצימה דלקת ומוות תאי, בעוד שהרדמת STAT2 הביאה לאפקט ההפוך. ניסויים באמצעות רצפי די-אן-איי מדווחים הראו כי STAT2 נקשר ישירות לאזור הבקרה של גן IFITM3 כדי להפעילו. בעכברים אפילפטיים, STAT2 היה גם מוגבר באזורים מוחיים הנוטים להתקפים, אך כיבוי IFITM3 לא שינה את STAT2 עצמו, מה שמאשר ש-STAT2 ממוקם מעלה בשרשרת כיורש-מפקח.
RNA קטן שמפעיל בלמים
הקישור האחרון בשרשרת הוא let-7g-5p, מולקולת RNA קטנה רגולטורית. מיקרו-רנ״א כמו let-7g-5p מכווננים את פעילות הגנים על ידי התקשרות להודעות יעד וחסימת תרגומן לחלבון. במיקרוגליה דלקתית ובמוחות של עכברים אפילפטיים, רמות let-7g-5p ירדו. ניסויים במעבדה הראו כי let-7g-5p נקשר ישירות לאזור הזנב של ההודעה הגנטית של STAT2 ומפחית את ייצורו. כאשר החוקרים הוסיפו כמות נוספת של let-7g-5p למיקרוגליה, רמות STAT2 ו-IFITM3 ירדו, האותות הדלקתיים פחתו ומחזור המוות התאי האט. חסימת let-7g-5p הביאה לאפקט ההפוך — אך ניתן היה להצילו על ידי השתקת STAT2 במקביל, מה שמוכיח ש-let-7g-5p מגן על ידי פגיעה ב-STAT2 ובאופן עקיף ב-IFITM3.
מה המשמעות עבור אנשים עם אפילפסיה
ביחד, הממצאים מסבירים סיפור פשוט אך עוצמתי: STAT2 מפעיל IFITM3 במיקרוגליה, מה שמגביר דלקת במוח ומוות תאי ומחמיר התקפים, בעוד let-7g-5p פועל כבלם טבעי בתהליך זה. באפילפסיה, נראה שהבלם הזה כושל, מה שמאפשר לדלקת להחריף. אף על פי שהתוצאות האלה מבוססות על תאים ועכברים ולא על מטופלים, הן מדגישות את ציר let-7g-5p/STAT2/IFITM3 כיעד מבטיח חדש. טיפולים עתידיים עשויים לשאוף להגביר את let-7g-5p או לחסום את STAT2 או IFITM3, לא כדי לרפא את האפילפסיה באופן מלא, אלא כדי לקרר את הסביבה הדלקתית שמסייעת להתקפים להתמיד ולהיות עמידים לתרופות סטנדרטיות.
ציטוט: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
מילות מפתח: אפילפסיה, דלקת עצבית, מיקרוגליה, IFITM3, microRNA let-7g-5p