Clear Sky Science · it
Neuroinfiammazione mediata da IFITM3 nell’epilessia regolata dall’asse let-7g-5p/STAT2
Perché l’infiammazione cerebrale conta nell’epilessia
L’epilessia colpisce decine di milioni di persone nel mondo e per circa un paziente su tre i farmaci attuali non controllano completamente le crisi. I ricercatori sospettano sempre più che un’infiammazione cronica all’interno del cervello contribuisca ad aumentare la frequenza delle crisi e a renderle più difficili da trattare. Questo studio esplora una catena molecolare recentemente individuata nelle cellule immunitarie del cervello che sembra alimentare — o attenuare — le fiamme infiammatorie associate all’epilessia. Capire questa catena potrebbe aprire la strada a trattamenti futuri che agiscono calmando la risposta immunitaria cerebrale anziché limitarsi a deprimere l’attività elettrica.
Le cellule immunitarie del cervello sotto i riflettori
Il lavoro si concentra sulle microglia, le cellule immunitarie residenti del cervello. Quando insorgono crisi o altri danni, le microglia passano a uno stato attivato rilasciando sostanze pro-infiammatorie che possono danneggiare i neuroni vicini e abbassare la soglia per ulteriori crisi. I ricercatori hanno cercato quali molecole specifiche all’interno delle microglia guidino questo ciclo dannoso. Hanno iniziato setacciando banche dati genetiche pubbliche tratte da modelli murini di epilessia e microglia infiammate, alla ricerca di geni costantemente up-regolati. Un candidato è emerso con forza: IFITM3, una proteina nota soprattutto per aiutare le cellule a difendersi dai virus ma sempre più implicata nell’infiammazione cerebrale in patologie come l’Alzheimer e l’ictus.
Un interruttore molecolare che peggiora le crisi
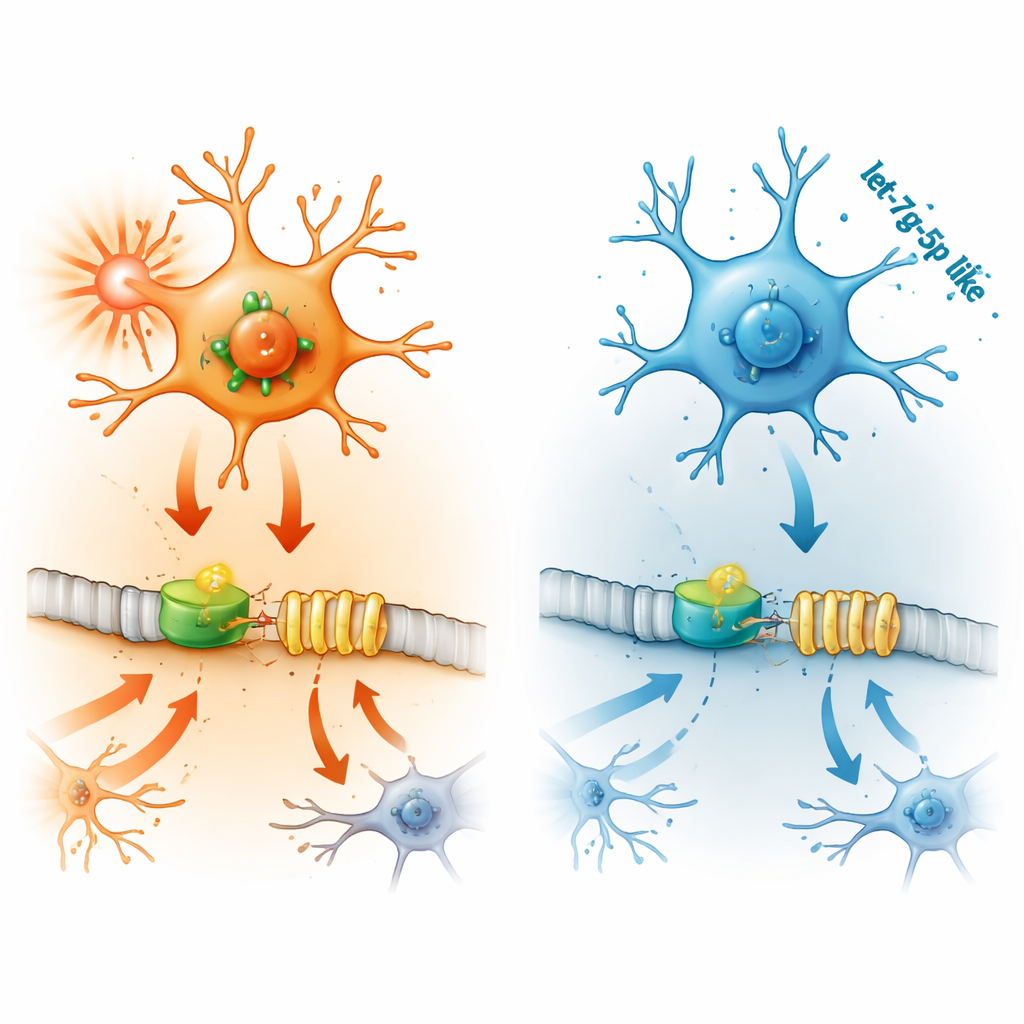
Per testare il ruolo di IFITM3, il gruppo ha usato microglia murine esposte a un simulatore batterico che attiva fortemente l’infiammazione. Quando i livelli di IFITM3 erano elevati, le cellule producevano grandi quantità di messaggeri infiammatori come interleuchina-1β, interleuchina-6 e fattore di necrosi tumorale, e mostravano più segnali di morte cellulare programmata, inclusa una forma infiammatoria e a pori detta piroptosi. Silenziare IFITM3 aveva l’effetto opposto, riducendo nettamente segnali infiammatori e marcatori di morte cellulare. I ricercatori hanno quindi esteso gli esperimenti agli animali viventi, creando un modello di crisi croniche nei topi e usando un virus per ridurre IFITM3 nel cervello. I topi con IFITM3 ridotto manifestavano crisi più lievi nelle valutazioni comportamentali, tracciati elettroencefalografici più tranquilli e livelli più bassi di marker infiammatori e di morte cellulare nel tessuto cerebrale.
Come le molecole a monte accendono o spengono IFITM3
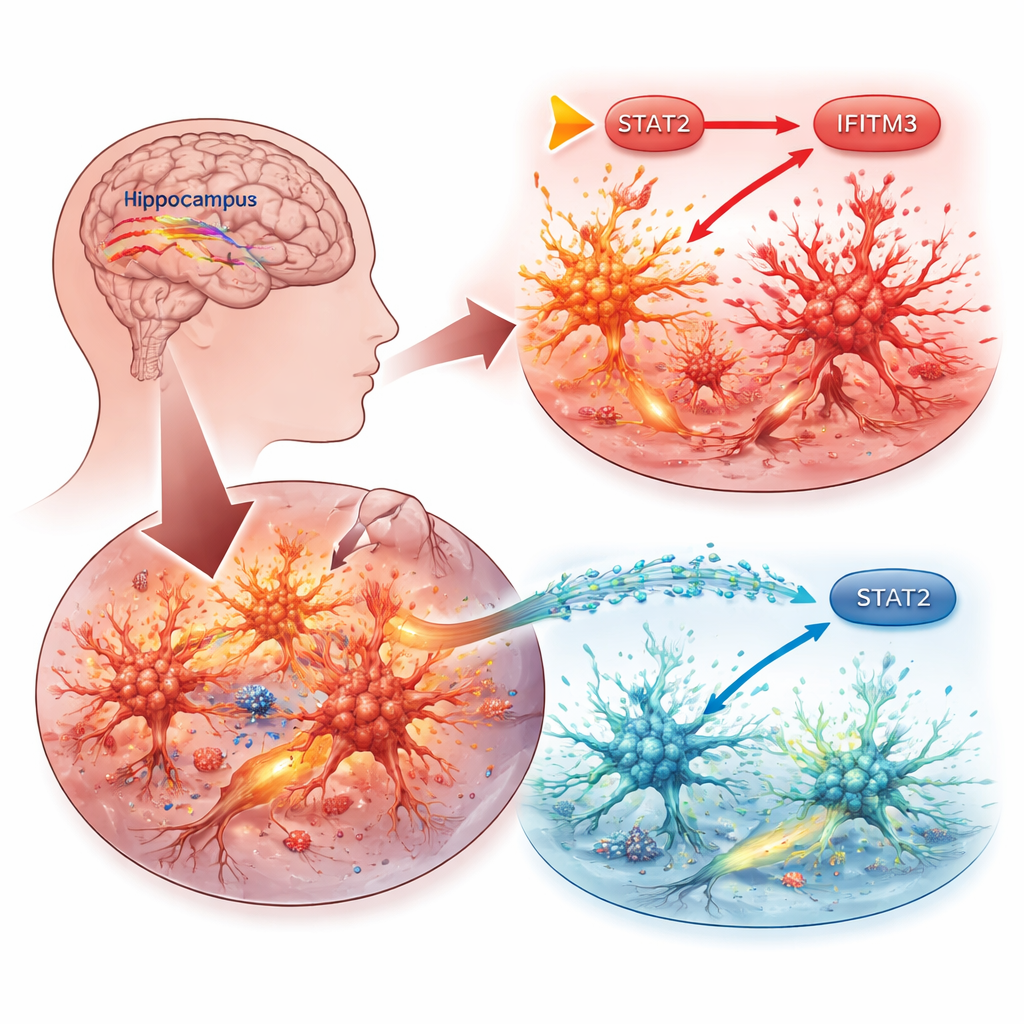
Successivamente, i ricercatori hanno tracciato come IFITM3 venga attivato. Si sono concentrati su STAT2, una proteina che trasmette segnali dagli interferoni — molecole chiave del sistema immunitario — al DNA della cellula. Nelle microglia, potenziare STAT2 aumentava i livelli di IFITM3 e intensificava infiammazione e morte cellulare, mentre ridurre STAT2 produceva l’effetto contrario. Esperimenti con costrutti reporter hanno mostrato che STAT2 si lega direttamente alla regione di controllo del gene IFITM3 per attivarlo. Nei topi epilettici, STAT2 risultava anch’esso elevato nelle regioni cerebrali soggette a crisi, ma spegnere IFITM3 non alterava STAT2, confermando che STAT2 sta a monte come interruttore principale.
Un piccolo RNA che mette il freno
L’anello finale della catena è let-7g-5p, una piccola molecola di RNA regolatoria. I microRNA come let-7g-5p modulano finemente l’attività genica legandosi ai messaggi bersaglio e bloccandone la traduzione in proteina. Nelle microglia infiammate e nei cervelli di topi epilettici, i livelli di let-7g-5p risultavano ridotti. Test in laboratorio hanno dimostrato che let-7g-5p si lega direttamente alla coda del messaggio genetico di STAT2, abbassandone la produzione. Quando i ricercatori hanno aggiunto let-7g-5p in eccesso alle microglia, STAT2 e IFITM3 sono diminuiti, i segnali infiammatori sono calati e la morte cellulare si è rallentata. Bloccare let-7g-5p produceva l’effetto opposto — ma questo poteva essere salvato silenziando contestualmente STAT2, dimostrando che let-7g-5p protegge prendendo di mira STAT2 e, di conseguenza, IFITM3.
Cosa potrebbe significare per le persone con epilessia
Nel complesso, questi risultati delineano una storia semplice ma potente: STAT2 attiva IFITM3 nelle microglia, aumentando l’infiammazione cerebrale e la morte cellulare e peggiorando le crisi, mentre let-7g-5p funge da freno naturale su questo processo. Nell’epilessia, quel freno sembra venir meno, permettendo all’infiammazione di spiralizzarsi. Sebbene i risultati derivino da cellule e modelli murini più che da pazienti, evidenziano l’asse let-7g-5p/STAT2/IFITM3 come un nuovo obiettivo promettente. Future terapie potrebbero mirare a potenziare let-7g-5p o a bloccare STAT2 o IFITM3, non per curare l’epilessia in modo definitivo, ma per raffreddare l’ambiente infiammatorio che favorisce la persistenza delle crisi e la resistenza ai farmaci standard.
Citazione: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Parole chiave: epilessia, neuroinfiammazione, microglia, IFITM3, microRNA let-7g-5p