Clear Sky Science · es
Neuroinflamación mediada por IFITM3 en la epilepsia regulada por el eje let-7g-5p/STAT2
Por qué importa la inflamación cerebral en la epilepsia
La epilepsia afecta a decenas de millones de personas en todo el mundo, y en aproximadamente uno de cada tres casos los fármacos actuales no controlan por completo las convulsiones. Cada vez son más los científicos que sospechan que la inflamación crónica dentro del cerebro contribuye a que las crisis sean más frecuentes y más difíciles de tratar. Este estudio explora una cadena de moléculas recién descubierta en las células inmunitarias del cerebro que parece avivar —o atenuar— las llamas inflamatorias que acompañan a la epilepsia. Comprender esta vía podría abrir la puerta a futuros tratamientos que actúen calmando la respuesta inmune cerebral en lugar de limitarse a atenuar la actividad eléctrica.
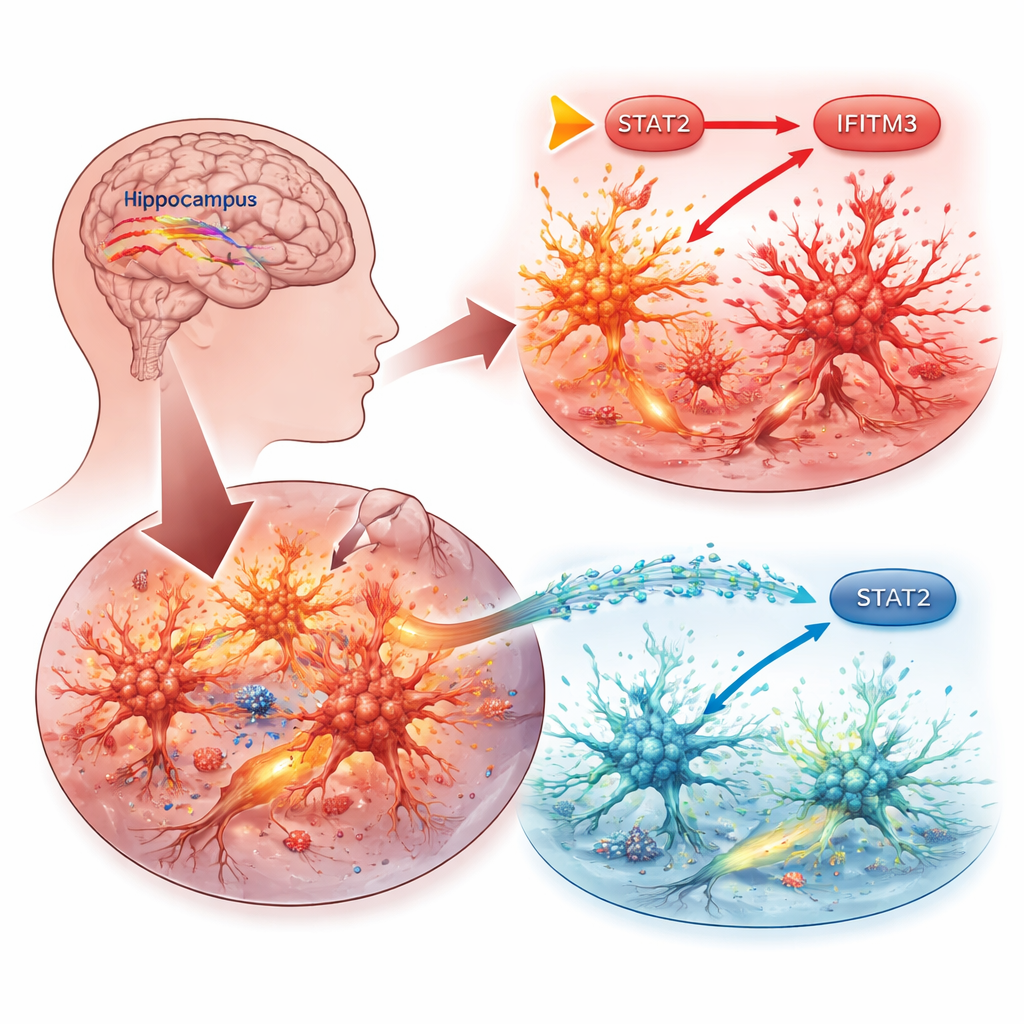
Las células inmunitarias del cerebro en el foco
El trabajo se centra en la microglía, las células inmunitarias residentes del cerebro. Cuando se producen convulsiones u otras lesiones, la microglía cambia a un estado activado, liberando sustancias inflamatorias que pueden dañar las neuronas cercanas y disminuir el umbral para nuevas convulsiones. Los investigadores se preguntaron qué moléculas específicas dentro de la microglía impulsan este ciclo dañino. Comenzaron sondeando bases de datos genéticos públicas de modelos murinos de epilepsia y microglía inflamada, buscando genes que se expresaran de forma consistente al alza. Surgió un candidato destacado: IFITM3, una proteína conocida sobre todo por ayudar a las células a defenderse de los virus, pero cada vez más vinculada a la inflamación cerebral en afecciones como el Alzheimer y el ictus.
Un interruptor molecular que empeora las convulsiones
Para probar el papel de IFITM3, el equipo utilizó células microgliales de ratón expuestas a un análogo bacteriano que activa fuertemente la inflamación. Cuando los niveles de IFITM3 eran altos, las células liberaban grandes cantidades de mediadores inflamatorios como la interleucina-1β, la interleucina-6 y el factor de necrosis tumoral, y mostraban más signos de muerte celular programada, incluido un tipo inflamatorio y formador de poros denominado piroptosis. Silenciar IFITM3 produjo el efecto contrario, reduciendo drásticamente las señales inflamatorias y los marcadores de muerte celular. Los científicos pasaron luego a modelos animales vivos, creando un modelo de convulsiones crónicas en ratones y usando un virus para reducir IFITM3 en el cerebro. Los ratones con IFITM3 reducido mostraron convulsiones más leves en las escalas de comportamiento, registros electroencefalográficos más tranquilos y niveles más bajos de marcadores inflamatorios y de muerte celular en el tejido cerebral.
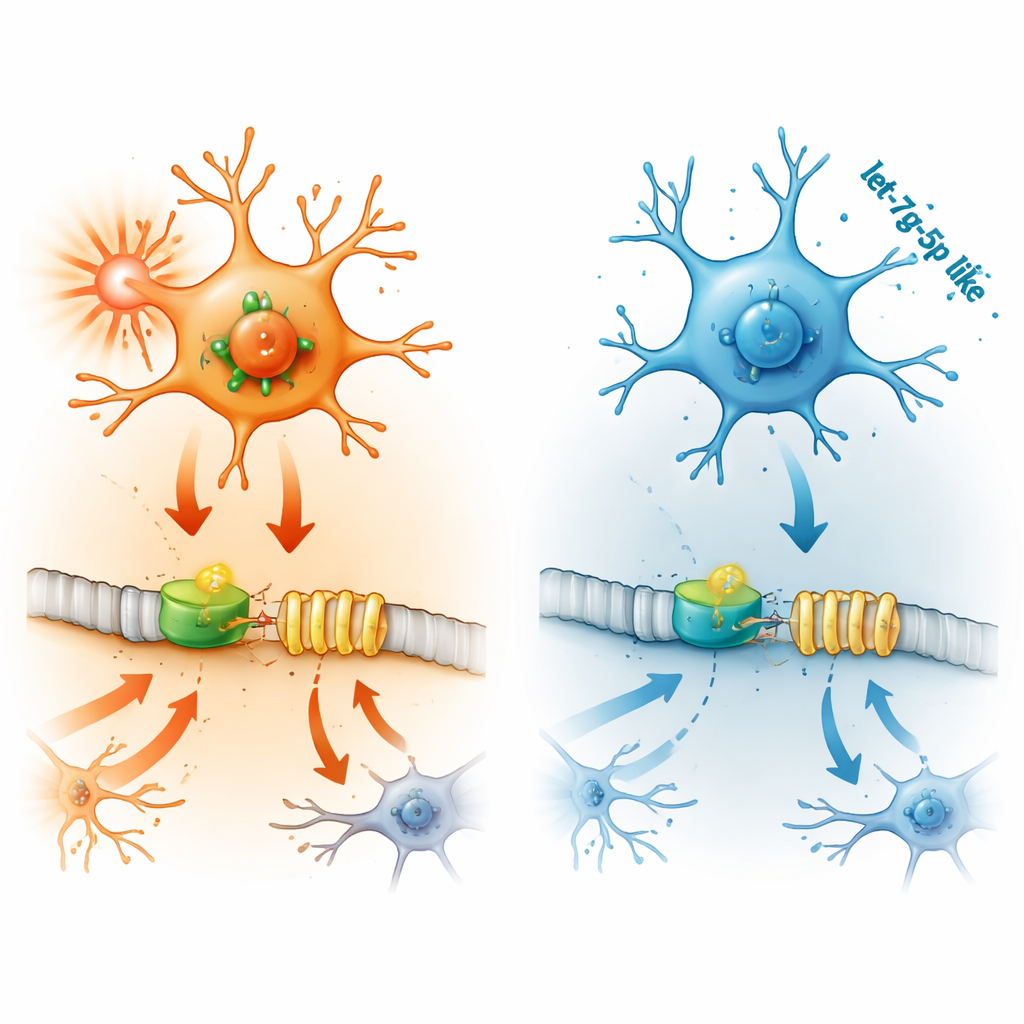
Cómo moléculas aguas arriba activan o desactivan IFITM3
A continuación, los investigadores rastrearon cómo se enciende IFITM3. Se centraron en STAT2, una proteína que transmite señales de las interferonas —moléculas clave del sistema inmune— al ADN de la célula. En microglía, aumentar STAT2 elevó los niveles de IFITM3 e intensificó la inflamación y la muerte celular, mientras que reducir STAT2 tuvo el efecto inverso. Experimentos con constructos reporteros de ADN mostraron que STAT2 se une directamente a la región reguladora del gen IFITM3 para activarlo. En ratones epilépticos, STAT2 también estaba aumentado en regiones cerebrales propensas a las convulsiones, pero apagar IFITM3 no cambió STAT2, lo que confirma que STAT2 actúa aguas arriba como un interruptor maestro.
Un pequeño ARN que frena el proceso
El eslabón final de la cadena es let-7g-5p, una diminuta molécula de ARN regulador. Los microARN como let-7g-5p afinan la actividad génica uniéndose a mensajes diana y bloqueando su traducción a proteína. En microglía inflamada y en cerebros de ratones epilépticos, los niveles de let-7g-5p disminuyeron. Ensayos de laboratorio mostraron que let-7g-5p se une directamente a la región terminal del mensaje genético de STAT2, reduciendo su producción. Cuando los investigadores añadieron let-7g-5p extra a la microglía, los niveles de STAT2 e IFITM3 cayeron, las señales inflamatorias descendieron y la muerte celular se ralentizó. Bloquear let-7g-5p produjo el efecto contrario, pero esto pudo revertirse al silenciar STAT2 simultáneamente, demostrando que let-7g-5p protege al dirigirse a STAT2 y, a su vez, a IFITM3.
Qué podría significar esto para las personas con epilepsia
En conjunto, estos hallazgos describen una historia sencilla pero potente: STAT2 activa IFITM3 en microglía, lo que aumenta la inflamación cerebral y la muerte celular, empeorando las convulsiones, mientras que let-7g-5p actúa como un freno natural de este proceso. En la epilepsia, ese freno parece fallar, permitiendo que la inflamación se descontrole. Aunque estos resultados provienen de células y ratones y no directamente de pacientes, ponen de relieve el eje let-7g-5p/STAT2/IFITM3 como un nuevo objetivo prometedor. Las terapias futuras podrían buscar potenciar let-7g-5p o bloquear STAT2 o IFITM3, no para curar la epilepsia por completo, sino para enfriar el entorno inflamatorio que ayuda a que las convulsiones persistan y resistan los fármacos estándar.
Cita: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Palabras clave: epilepsia, neuroinflamación, microglía, IFITM3, microARN let-7g-5p