Clear Sky Science · tr
let-7g-5p/STAT2 ekseniyle düzenlenen IFITM3 aracılı nöroenflamasyonun epilepsideki rolü
Neden beynin iltihabı epilepside önemli
Epilepsi dünya çapında on milyonlarca insanı etkiler ve yaklaşık üç kişiden birinde mevcut ilaçlar nöbetleri tam olarak kontrol edemez. Bilim insanları kronik beyin içi iltihabın nöbetleri daha sık ve tedaviye daha dirençli hale getirdiğine giderek daha çok şüpheyle bakıyor. Bu çalışma, epilepsiyle birlikte görülen iltihabı körükleyen veya yatıştıran gibi görünen, beynin bağışıklık hücreleri içinde yeni keşfedilmiş bir moleküler zinciri araştırıyor. Bu zinciri anlamak, yalnızca elektriksel aktiviteyi bastırmak yerine beynin kendi bağışıklık tepkisini yatıştırmayı hedefleyen gelecekteki tedavilere kapı aralayabilir.
Spot ışığında beynin bağışıklık hücreleri
Çalışma, beynin yerel bağışıklık hücreleri olan mikroglialara odaklanıyor. Nöbetler veya diğer yaralanmalar meydana geldiğinde, mikroglialar aktive bir duruma geçer ve yakınlardaki sinir hücrelerine zarar verebilen ve daha fazla nöbet için eşiği düşürebilen iltihaplı kimyasallar salar. Araştırmacılar, mikroglialarda bu zararlı döngüyü hangi spesifik moleküllerin yönlendirdiğini sordular. Fare modellerindeki epilepsi ve inflamasyonlu mikroglia verilerini içeren kamuya açık genetik veritabanlarını tarayarak tutarlı şekilde artmış genleri aradılar. Bir aday öne çıktı: IFITM3, hücrelerin virüslere karşı savunmasına yardımcı olmasıyla bilinen ama Alzheimer hastalığı ve inme gibi durumlarda beyin iltihabıyla giderek daha çok ilişkilendirilen bir protein.
Nöbetleri kötüleştiren bir moleküler anahtar
IFITM3’ün rolünü test etmek için ekip, güçlü şekilde iltihabı tetikleyen bir bakteri taklidiyle muamele edilmiş fare mikroglia hücreleri kullandı. IFITM3 seviyeleri yüksek olduğunda, hücreler interlökin-1β, interlökin-6 ve tümör nekroz faktörü gibi iltihap habercilerini bolca salgıladı ve piroptoza benzer, gözenek açıcı ateşli bir tür dahil olmak üzere programlı hücre ölümü belirtileri arttı. IFITM3 susturulduğunda ters etki görüldü; iltihap sinyalleri ve hücre ölümü belirteçleri belirgin şekilde azaldı. Araştırmacılar daha sonra canlı hayvanlara geçti, farelerde kronik nöbet modeli oluşturdular ve beyindeki IFITM3’ü azaltmak için bir virüs kullandılar. IFITM3 azaltılmış farelerde davranışsal puanlama ölçeklerine göre daha hafif nöbetler, daha sakin beyin dalgası kayıtları ve beyin dokusunda daha düşük iltihap ve hücre ölümü belirteçleri görüldü.
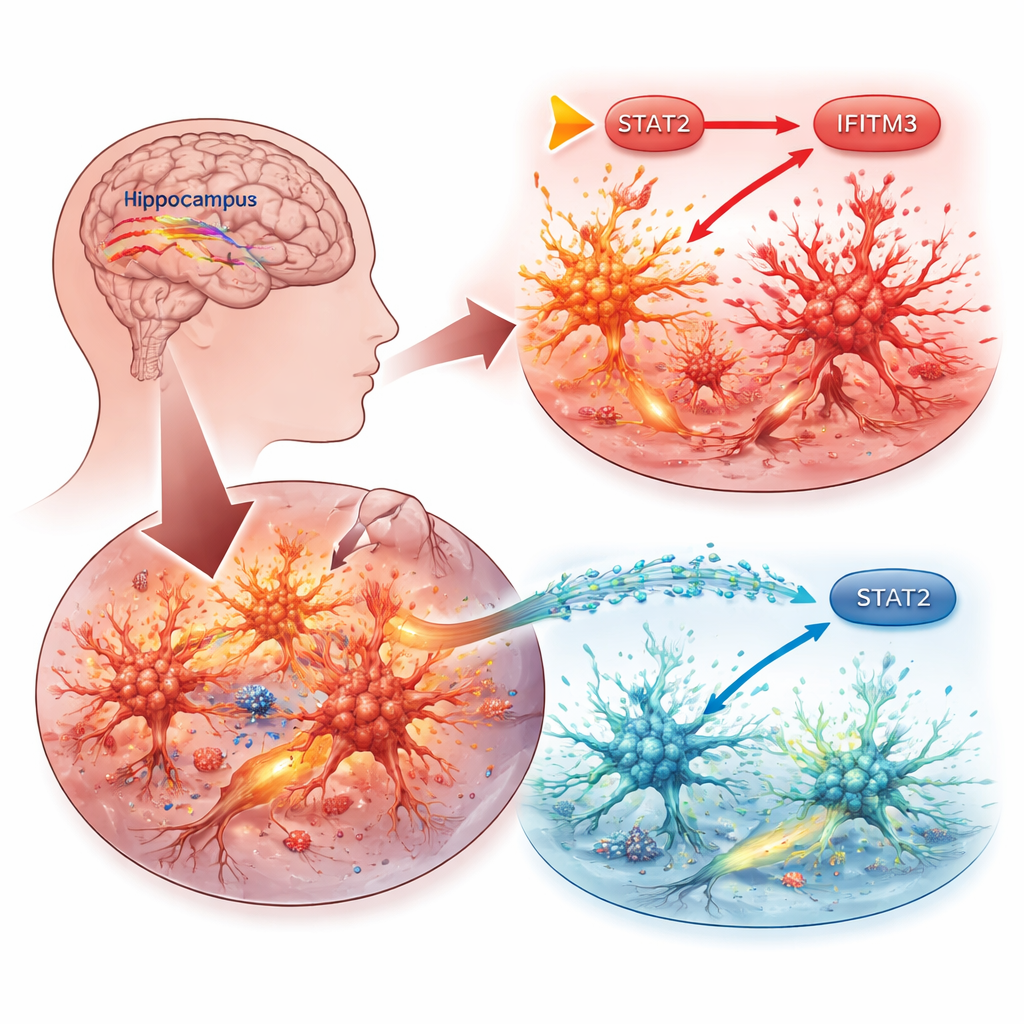
Üst akış moleküller IFITM3’ü nasıl açıp kapatıyor
Sonraki adımda araştırmacılar IFITM3’ün nasıl açıldığını izledi. Interferonlardan—temel bağışıklık moleküllerinden—sinyalleri hücrenin DNA’sına taşıyan bir protein olan STAT2’ye odaklandılar. Mikroglialarda STAT2’yi artırmak IFITM3 seviyelerini yükseltti ve iltihap ile hücre ölümünü şiddetlendirdi; STAT2’yi düşürmek ise ters etki gösterdi. DNA raporlayıcı yapıların kullanıldığı deneyler, STAT2’nin IFITM3 geninin kontrol bölgesine doğrudan bağlanıp onu aktive ettiğini gösterdi. Epileptik farelerde STAT2, nöbetlere yatkın beyin bölgelerinde de yükselmişti; ancak IFITM3 kapatıldığında STAT2 değişmedi, bu da STAT2’nin yukarıda yer alan bir anahtar olduğunu doğruluyor.
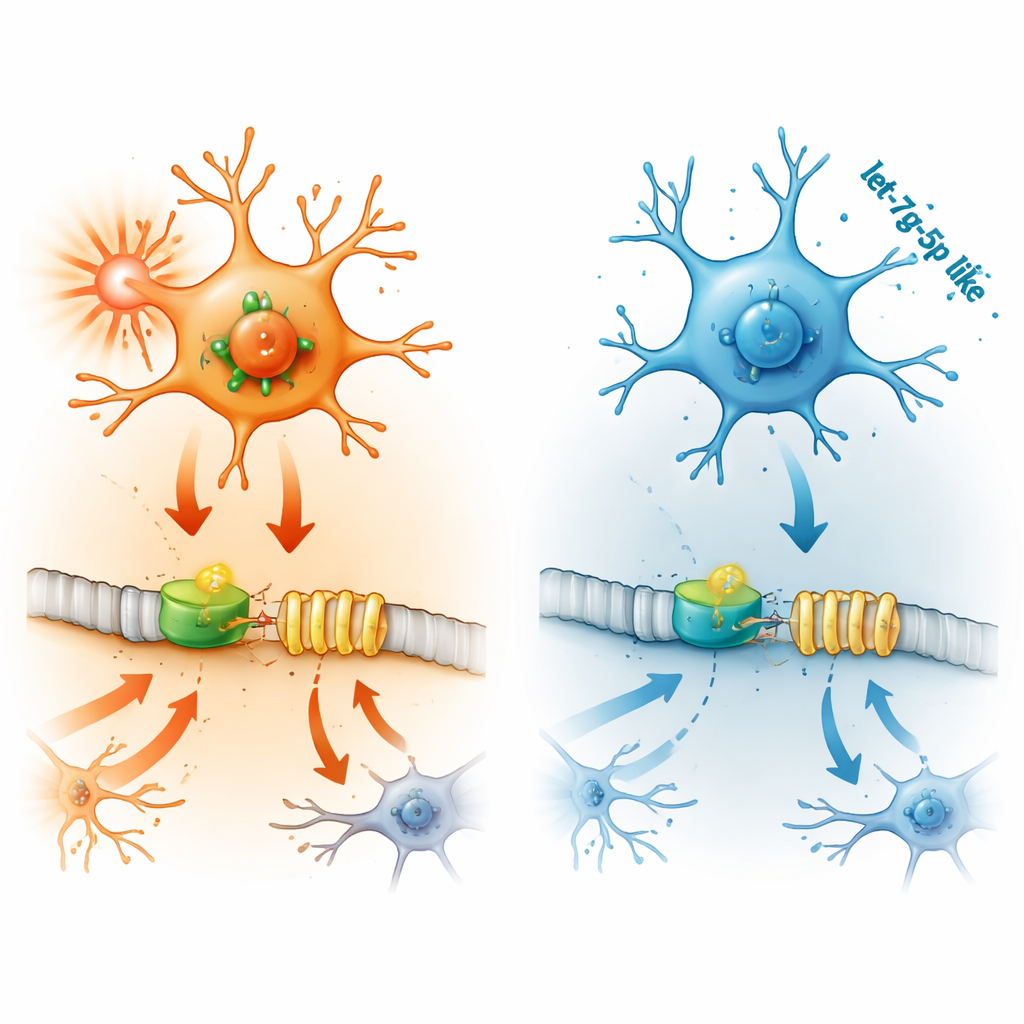
Fren rolü oynayan küçük bir RNA
Zincirin son halkası let-7g-5p adında küçük bir düzenleyici RNA molekülü. let-7g-5p gibi mikroRNA’lar hedef mesajlara bağlanarak onların proteine çevrilmesini engelleyip gen aktivitesini ince ayarlar. İnflamasyonlu mikroglialarda ve epileptik fare beyinlerinde let-7g-5p seviyeleri düştü. Laboratuvar testleri let-7g-5p’nin STAT2’nin genetik mesajının kuyruk bölgesine doğrudan bağlanıp STAT2 üretimini düşürdüğünü gösterdi. Araştırmacılar mikroglialara ekstra let-7g-5p eklediklerinde STAT2 ve IFITM3 seviyeleri düştü, iltihap sinyalleri azaldı ve hücre ölümü yavaşladı. let-7g-5p’yi bloke etmek ters etki yarattı—ancak bu, aynı anda STAT2 susturularak düzeltilebildi; bu da let-7g-5p’nin STAT2’yi hedefleyerek ve dolayısıyla IFITM3’ü etkileyerek koruma sağladığını kanıtlıyor.
Bu, epilepsili insanlar için ne anlama gelebilir
Bu bulgular birlikte basit ama güçlü bir hikâye çiziyor: STAT2 mikroglialarda IFITM3’ü açar, bu da beyin iltihabını ve hücre ölümünü artırır, nöbetleri kötüleştirir; let-7g-5p ise bu sürece doğal bir fren uygular. Epilepside bu fren başarısız oluyor gibi görünüyor ve iltihabın kontrolden çıkmasına izin veriyor. Bu sonuçlar hücreler ve farelerden elde edilmiş olsa da let-7g-5p/STAT2/IFITM3 eksenini umut verici yeni bir hedef olarak öne çıkarıyor. Gelecekteki tedaviler let-7g-5p’yi artırmayı veya STAT2 ya da IFITM3’ü engellemeyi amaçlayabilir; amaç epilepsiyi tamamen iyileştirmek değil, nöbetlerin sürmesine ve standart ilaçlara direnç göstermesine yardımcı olan iltihaplı ortamı soğutmaktır.
Atıf: Liu, J., Sheng, D., Li, X. et al. IFITM3-mediated neuroinflammation in epilepsy regulated by the let-7g-5p/STAT2 axis. Sci Rep 16, 14077 (2026). https://doi.org/10.1038/s41598-026-44357-z
Anahtar kelimeler: epilepsi, nöroenflamasyon, mikroglia, IFITM3, microRNA let-7g-5p