Clear Sky Science · zh
肠道代谢物TMAO及其结构类似物与纤维蛋白原结合从而增强血栓形成:解释动脉粥样硬化风险的理论依据
从肠道化学物到血栓
肠道中的事情并不会只留在肠道。该研究探讨了一种由肠道细菌产生的微小分子——TMAO——如何改变血栓的形成与裂解过程。由于异常血栓是心肌梗死和中风的基础,理解饮食、肠道微生物、常用药物与凝血之间这种隐蔽联系,有助于解释为何部分人群承受更高的心血管风险,并指明可能的干预方向。
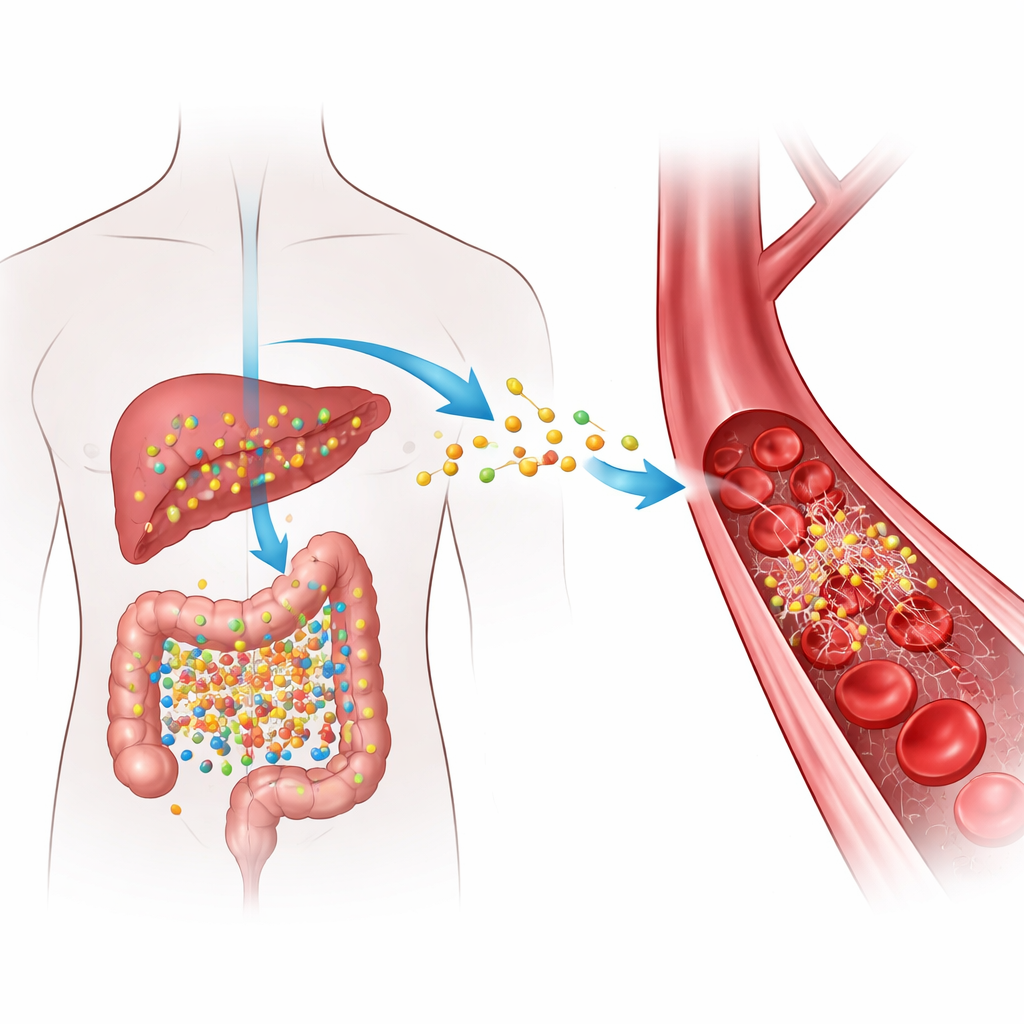
日常食物如何成为风险信号
当我们摄入富含某些营养成分的食物(如红肉、鸡蛋和高脂乳制品)时,肠道细菌会将这些成分转化为一种中间化合物,随后肝脏将其转变为TMAO。血液中高水平的TMAO已多次与动脉堵塞和更高的危险血栓发生率相关,但具体的机制尚不清楚。作者将注意力集中在纤维蛋白原上——一种可溶性循环蛋白,受凝血酶切割后形成纤维蛋白,即通过形成血栓封堵损伤的丝状物质。他们探究TMAO是否以物理方式与纤维蛋白原相互作用,从而使血栓形成更快或更难被溶解。
使血栓形成更快且难以清除
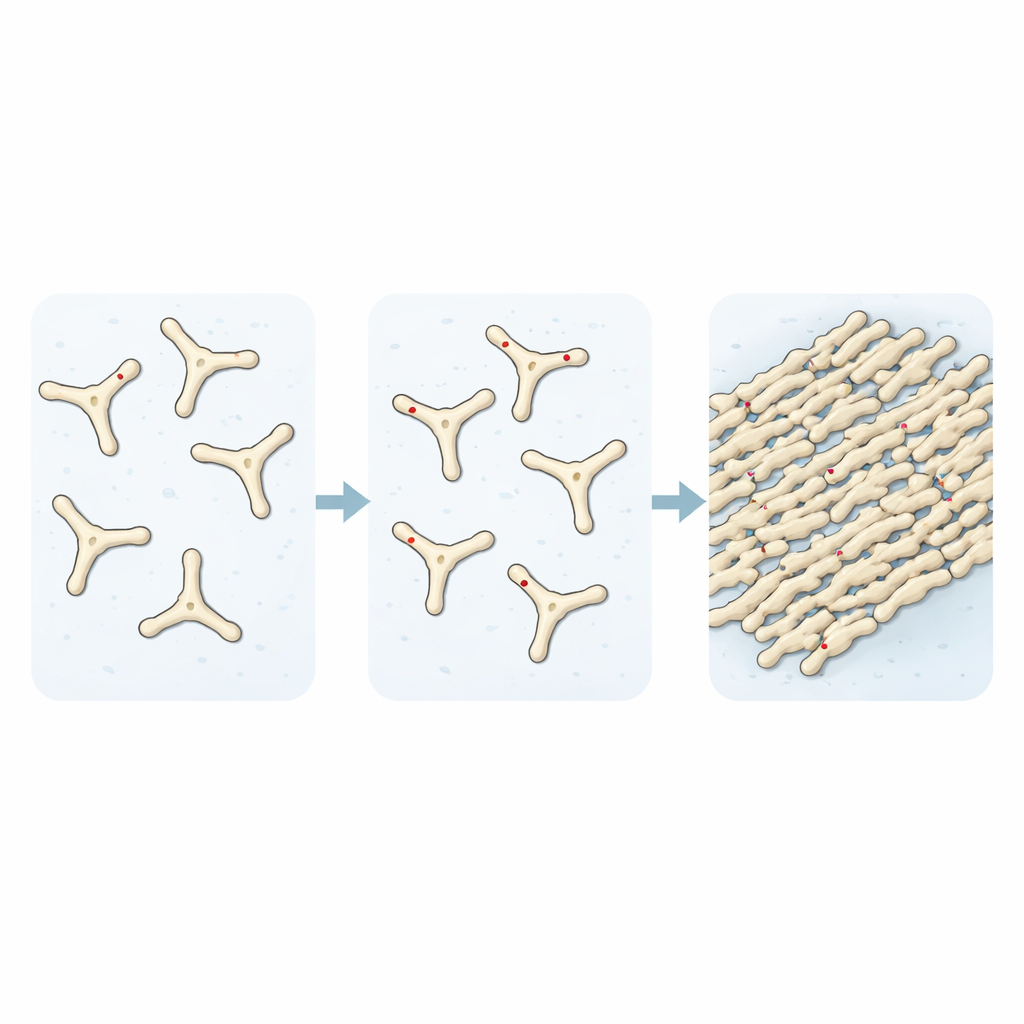
通过追踪纤维蛋白原溶液随时间转变为纤维蛋白的过程,研究者表明加入TMAO会加速血栓早期组装单元的形成。光散射和荧光染料实验证实,在没有TMAO的情况下,设定时间后约只有三分之一的蛋白质参与形成纤维。而随着TMAO浓度上升,这一比例趋向完全转化,显微图像显示出更为致密的纤维网络。在检验这些血栓的降解情况时,他们发现另一个令人担忧的特征:在TMAO存在下形成的血栓对蛋白酶切割极为耐受,保持紧凑并大体完整,而正常血栓几乎被完全降解。
凝血蛋白上的精确对接位点
为确定此效应是否源于直接结合,团队在将TMAO与纤维蛋白原混合时测量了热变化,发现二者在接近心脏病患者血中见到的浓度下具有中等强度的相互作用。光谱学方法表明,纤维蛋白原的构象略微松动,暴露出更多有利于蛋白-蛋白接触的黏性区域。计算机建模和长时间模拟描绘了TMAO在纤维蛋白原上的结合位置,突出一个被称为beta1钙结合位点的特定区域。当该位点被天然的钙离子占据时,TMAO便无法发挥作用,血栓形成在有无TMAO时无显著差别。这表明beta1位点是调节纤维蛋白原分子易于互相锁定的控制点。
药物代谢物也加入了这一故事
接着,作者询问其他与TMAO相似的小分子是否也可能具有相同作用。通过化学数据库检索和对接软件筛选,他们挑选出两种作为广泛使用的抗抑郁药和尼古丁相关药物N-氧化物分解产物的化合物。在试管实验中,这些代谢物同样加速并增强了纤维的组装,产生更粗、更致密的纤维蛋白网络,表现与TMAO相似。这一发现提出了一个可能性:某些药物在体内代谢后,可能通过作用于纤维蛋白原的同一热点,悄然推动血栓形成更稳固。
对心脏病和中风风险的意义
综合所有证据,这项工作揭示了一条从肠源或药物来源的N-氧化物分子到血栓结构改变的直接链路。通过结合纤维蛋白原的特定位点,TMAO及其化学近亲促使该蛋白进入一种有利于快速纤维形成的构象,并产生更难被降解的血栓。对普通读者而言,这意味着某些微生物代谢产物和药物代谢物可能在不显山露水中加固血栓的“骨架”,帮助解释为何TMAO升高与更高的动脉堵塞事件风险相关。纤维蛋白原上的beta1位点因此成为一个有前景的治疗靶点,旨在在不完全抑制凝血的情况下软化血栓并减少动脉粥样硬化并发症。
引用: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
关键词: 肠道微生物组, 血栓, TMAO, 动脉粥样硬化, 纤维蛋白原