Clear Sky Science · pt
O metabólito intestinal TMAO e seus análogos estruturais ligam-se à fibrinogênio, aumentando assim a formação de coágulos: uma justificativa para o risco de aterosclerose
De químicos intestinais a coágulos sanguíneos
O que acontece no seu intestino não fica apenas no intestino. Este estudo investiga como uma molécula pequena produzida por bactérias intestinais, chamada TMAO, pode alterar a forma como os coágulos sanguíneos se formam e se desfazem. Como coágulos anormais são a base de ataques cardíacos e acidentes vasculares cerebrais, compreender esse elo oculto entre dieta, micróbios intestinais, medicamentos comuns e coagulação ajuda a explicar por que algumas pessoas apresentam maior risco cardiovascular — e onde novos tratamentos podem intervir.
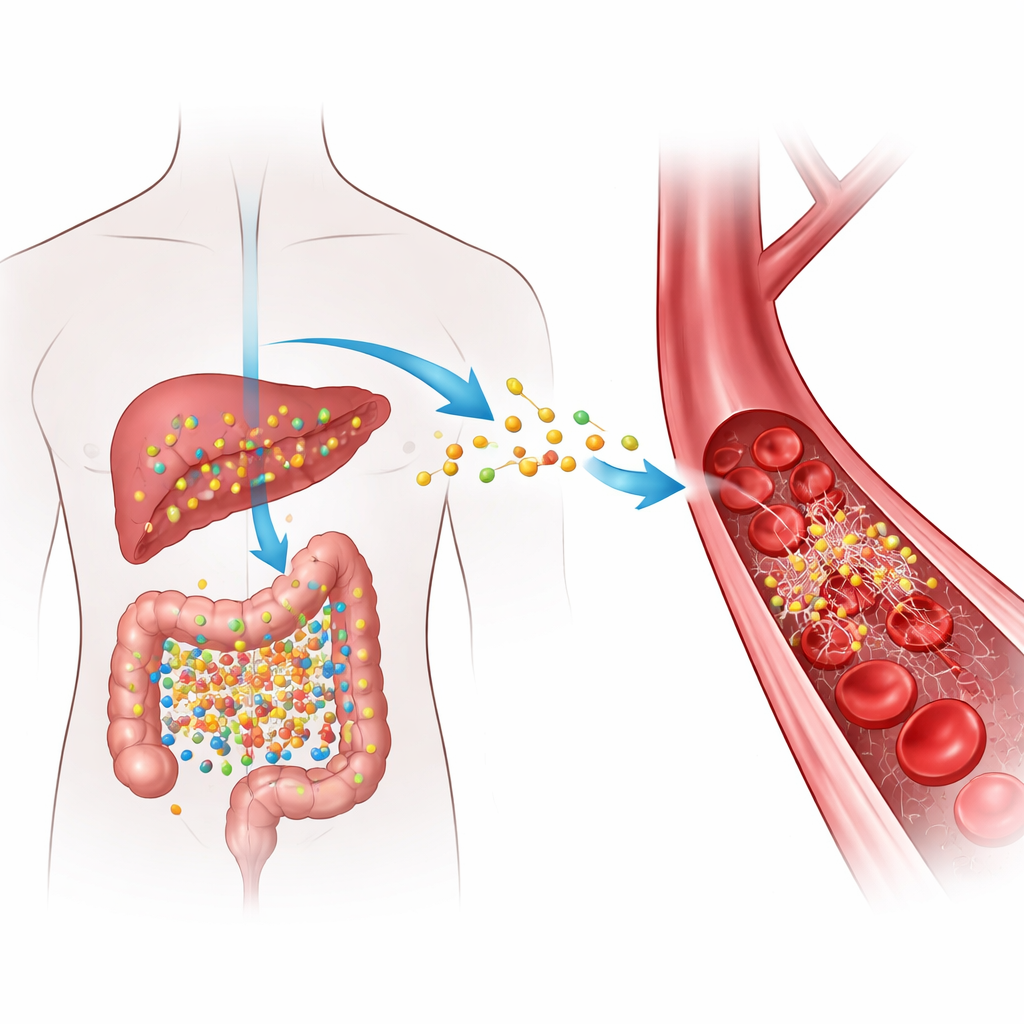
Como alimentos do dia a dia se tornam um sinal de risco
Quando comemos alimentos ricos em certos nutrientes encontrados na carne vermelha, ovos e laticínios gordurosos, as bactérias intestinais convertem esses componentes em um composto intermediário que o fígado então transforma em TMAO. Níveis elevados de TMAO no sangue têm sido repetidamente associados a artérias obstruídas e a uma maior probabilidade de coágulos perigosos, mas o “como” exato permaneceu obscuro. Os autores concentraram-se na fibrinogênio, uma proteína solúvel que circula no sangue e, quando cortada pela enzima trombina, se transforma em fibrina — o material filamentoso que ajuda a selar ferimentos formando coágulos. Eles perguntaram se o TMAO interage fisicamente com a fibrinogênio de um modo que possa fazer com que os coágulos se formem mais rápido ou se tornem mais difíceis de dissolver.
Fazendo coágulos mais rápido e mais difíceis de remover
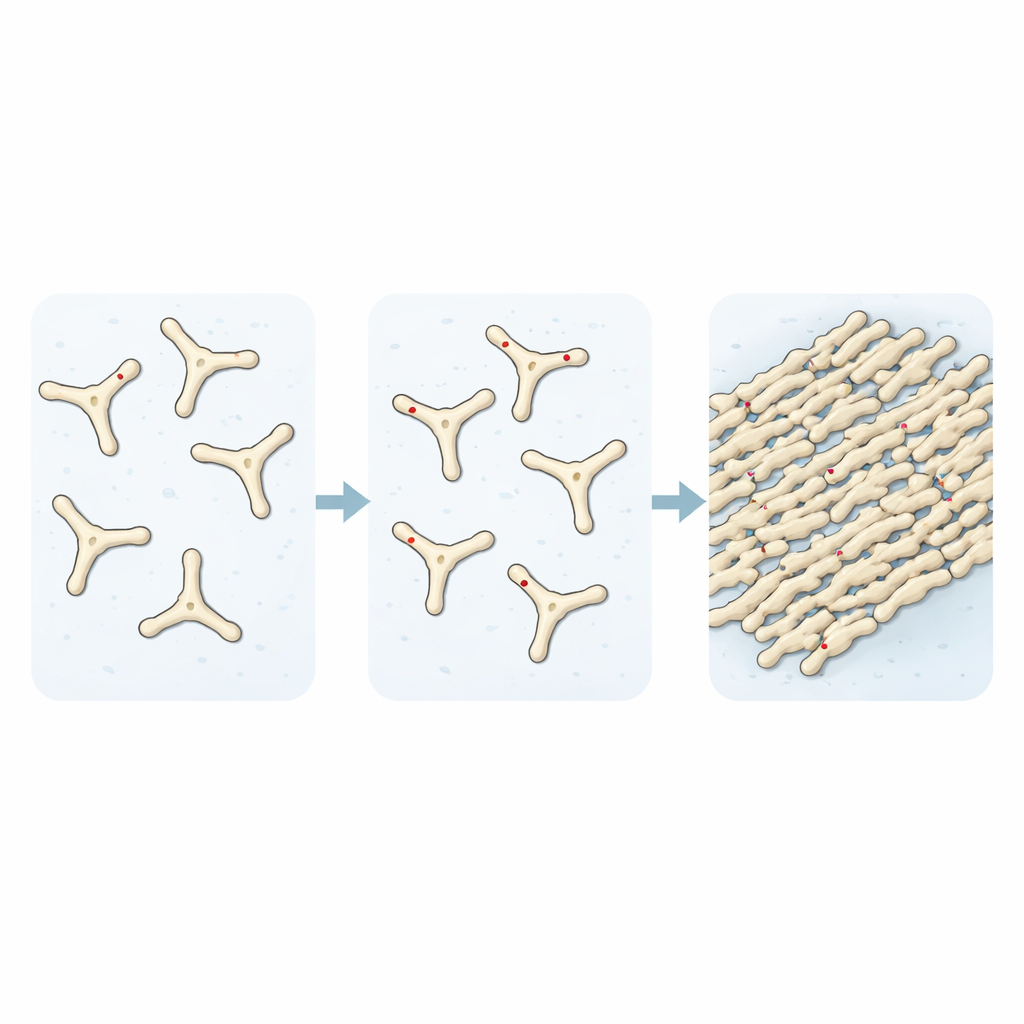
Ao acompanhar como soluções de fibrinogênio se transformam em fibrina ao longo do tempo, os pesquisadores mostraram que a adição de TMAO acelera a montagem dos blocos iniciais dos coágulos. Experimentos de espalhamento de luz e com corantes fluorescentes revelaram que, sem TMAO, apenas cerca de um terço da proteína havia se juntado em fibrilas após um período determinado. Com níveis crescentes de TMAO, essa fração subiu em direção à conversão completa, e imagens ao microscópio mostraram uma teia de fibras muito mais densa. Quando examinaram como esses coágulos se degradavam, encontraram outra característica preocupante: coágulos formados na presença de TMAO eram altamente resistentes à digestão por uma enzima que corta proteínas, permanecendo compactos e em grande parte intactos enquanto coágulos normais eram quase completamente degradados.
Um local de encaixe preciso na proteína de coagulação
Para verificar se esse efeito advinha de uma ligação direta, a equipe mediu alterações de calor quando TMAO foi misturado com fibrinogênio e encontrou evidências claras de que os dois interagem com força moderada em concentrações semelhantes às vistas em pessoas com doença cardíaca. Métodos espectroscópicos indicaram que a forma da fibrinogênio ficava ligeiramente afrouxada, expondo mais áreas pegajosas que favorecem o contato proteína–proteína. Modelagem computacional e simulações longas mapearam onde o TMAO se acomoda na fibrinogênio e destacaram uma região específica conhecida como sítio beta1 de ligação ao cálcio. Quando esse sítio estava ocupado por íons cálcio naturais, o TMAO não conseguia mais exercer seu efeito, e a formação do coágulo parecia a mesma com ou sem TMAO. Isso aponta para o sítio beta1 como um ponto de controle que ajusta quão facilmente as moléculas de fibrinogênio se travam umas nas outras.
Metabólitos de medicamentos entram na história
Os autores então perguntaram se outras pequenas moléculas que se assemelham ao TMAO poderiam se comportar de forma semelhante. Usando bancos de dados químicos e software de docking, eles triaram um conjunto de compostos relacionados e selecionaram dois que são produtos de degradação N-óxido de medicamentos antidepressivos amplamente usados e fármacos relacionados à nicotina. Em experimentos em tubo de ensaio, esses metabólitos também aumentaram a velocidade e a extensão da montagem de fibrina, e produziram redes de fibrina mais espessas e densas, muito parecidas com as causadas pelo TMAO. Essa descoberta levanta a possibilidade de que alguns medicamentos, uma vez processados pelo corpo, possam sutilmente deslocar o equilíbrio em direção à formação de coágulos mais robustos agindo sobre o mesmo ponto crítico na fibrinogênio.
O que isso significa para o risco de ataque cardíaco e AVC
Reunindo todas as evidências, o trabalho revela uma cadeia direta de eventos desde moléculas N-óxido derivadas do intestino ou de drogas até alterações na estrutura dos coágulos sanguíneos. Ao se ligarem a um sítio específico na fibrinogênio, o TMAO e seus parentes químicos empurram a proteína para uma conformação que incentiva a formação rápida de fibras e produz coágulos mais difíceis de degradar. Para leigos, isso significa que certos subprodutos microbianos e metabólitos de medicamentos podem endurecer silenciosamente a “estrutura” dos coágulos, ajudando a explicar por que níveis elevados de TMAO se correlacionam com maior probabilidade de eventos que bloqueiam artérias. O sítio beta1 na fibrinogênio surge como um alvo promissor para terapias destinadas a amaciar coágulos e reduzir complicações da aterosclerose sem bloquear completamente a coagulação.
Citação: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Palavras-chave: microbioma intestinal, coágulos sanguíneos, TMAO, aterosclerose, fibrinogênio