Clear Sky Science · pl
Metabolit jelitowy TMAO i jego analogi strukturalne wiążą się z fibrynogenem, zwiększając tworzenie skrzepów: uzasadnienie ryzyka miażdżycy
Od chemikaliów w jelitach do skrzepów krwi
To, co dzieje się w jelitach, nie zostaje w jelitach. Badanie to analizuje, jak niewielka cząsteczka wytwarzana przez bakterie jelitowe, nazywana TMAO, może zmieniać sposób powstawania i rozkładu skrzepów krwi. Ponieważ nieprawidłowe skrzepy leżą u podłoża zawałów serca i udarów, zrozumienie tego ukrytego związku między dietą, mikrobiotą jelitową, powszechnymi lekami a krzepnięciem pomaga wyjaśnić, dlaczego niektórzy ludzie mają wyższe ryzyko chorób sercowo-naczyniowych — i gdzie można by wprowadzić nowe terapie.
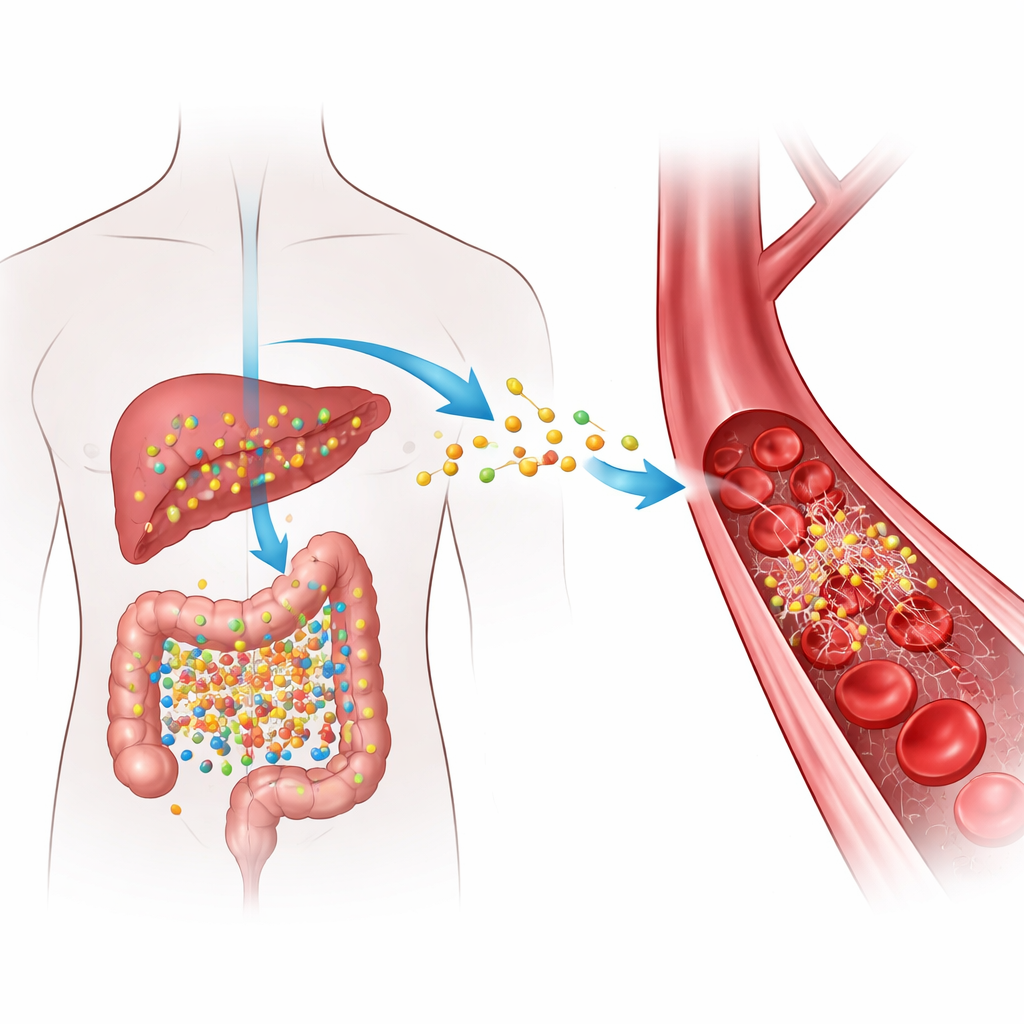
Jak codzienne jedzenie staje się sygnałem ryzyka
Gdy spożywamy pokarmy bogate w pewne składniki występujące w czerwonym mięsie, jajach i tłustych produktach mlecznych, bakterie jelitowe przekształcają te związki w pośredni związek, który w wątrobie przekształcany jest następnie w TMAO. Wysokie stężenia TMAO we krwi wielokrotnie wiązano ze zwężeniem tętnic i większym prawdopodobieństwem niebezpiecznych skrzepów, ale dokładny mechanizm był niejasny. Autorzy skupili się na fibrynogenie — rozpuszczalnym białku krążącym we krwi, które po przecięciu przez enzym trombinę przekształca się w fibrynę — włóknisty materiał pomagający uszczelnić uszkodzenia przez tworzenie skrzepów. Zastanawiali się, czy TMAO fizycznie oddziałuje z fibrynogenem w sposób, który mógłby powodować szybsze tworzenie skrzepów lub ich trudniejsze rozpuszczanie.
Przyspieszanie tworzenia skrzepów i utrudnianie ich rozkładu
Śledząc, jak roztwory fibrynogenu z czasem przechodzą w fibrynę, badacze wykazali, że dodanie TMAO przyspiesza składanie wczesnych elementów budulcowych skrzepów. Eksperymenty z rozpraszaniem światła i barwnikami fluorescencyjnymi ujawniły, że bez TMAO tylko około jednej trzeciej białka dołączyło do włókien po określonym czasie. Wraz ze wzrostem stężenia TMAO ten udział rósł aż do niemal pełnej konwersji, a obrazy mikroskopowe ukazały znacznie gęstszą sieć włókien. Przy badaniu rozkładu tych skrzepów odkryto kolejny niepokojący element: skrzepy utworzone w obecności TMAO były wysoce oporne na trawienie przez enzymy rozcinające białka, pozostając zwarte i w dużej mierze nienaruszone, podczas gdy normalne skrzepy były niemal całkowicie rozkładane.
Precyzyjne miejsce dokowania na białku krzepnięcia
Aby sprawdzić, czy efekt wynika z bezpośredniego wiązania, zespół zmierzył zmiany ciepła przy mieszaniu TMAO z fibrynogenem i znalazł wyraźne dowody na interakcję o umiarkowanej sile przy stężeniach podobnych do tych obserwowanych u osób z chorobami serca. Metody spektroskopowe wskazały, że kształt fibrynogenu nieco się poluzowuje, odsłaniając więcej lepionych powierzchni sprzyjających kontaktom białko–białko. Modelowanie komputerowe i długie symulacje odwzorowały miejsce, gdzie TMAO lokuje się na fibrynogenie, i wyróżniły konkretny obszar znany jako miejsce wiązania wapnia beta1. Gdy miejsce to było zajęte przez naturalne jony wapnia, TMAO nie mogło już wywierać swojego efektu, a tworzenie skrzepów wyglądało tak samo, niezależnie od obecności TMAO. Wskazuje to na miejsce beta1 jako punkt kontrolny, który reguluje, jak łatwo cząsteczki fibrynogenu łączą się ze sobą.
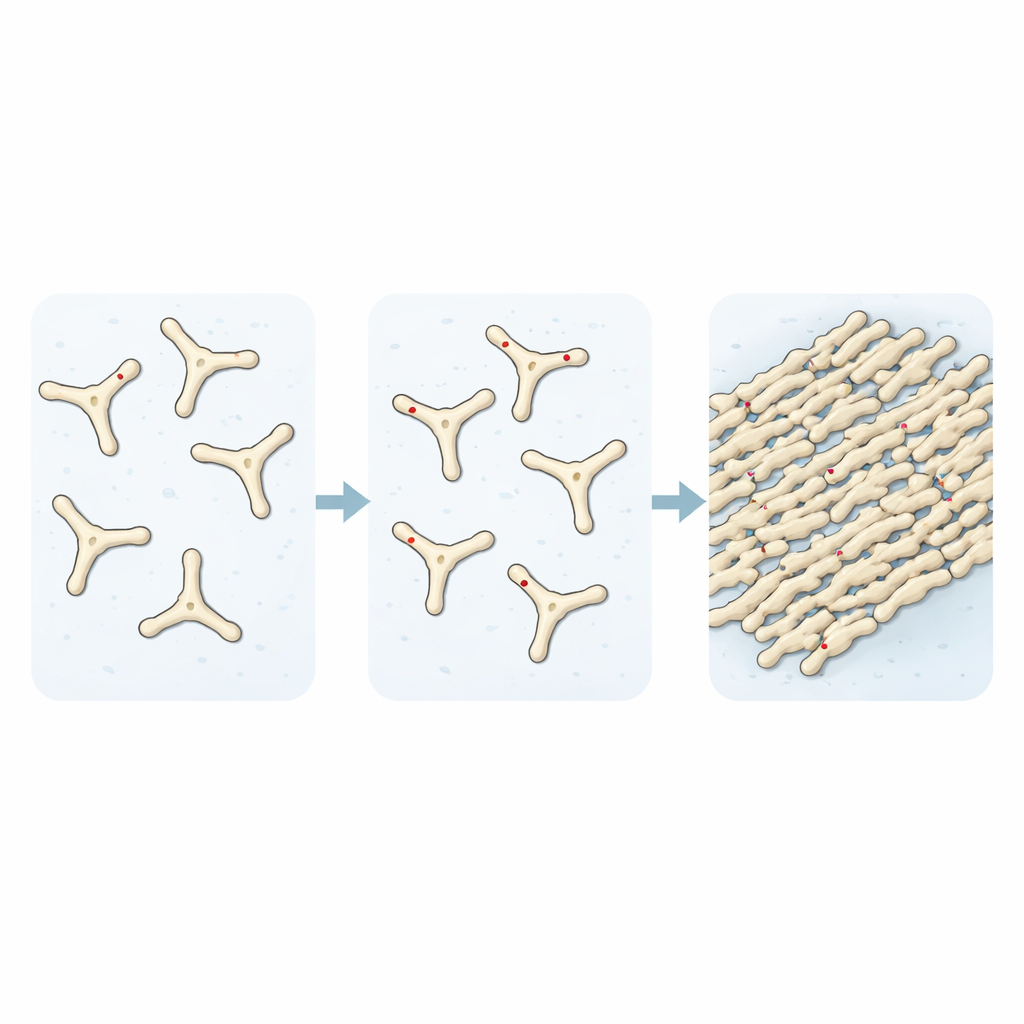
Do historii dołączają metabolity leków
Autorzy zapytali następnie, czy inne małe cząsteczki przypominające TMAO mogą zachowywać się podobnie. Korzystając z baz chemicznych i oprogramowania do dokowania, przeskanowali zestaw pokrewnych związków i wybrali dwa, które są produktami rozpadu N-tlenków powszechnie stosowanych leków przeciwdepresyjnych i związków związanych z nikotyną. W eksperymentach probówkowych te metabolity również zwiększały szybkość i zakres składania fibryny oraz tworzyły grubsze, gęstsze sieci fibrynowe, podobnie jak TMAO. Odkrycie to sugeruje możliwość, że niektóre leki, po przetworzeniu przez organizm, mogą subtelnie przechylić równowagę w stronę bardziej odpornego tworzenia skrzepów działając na ten sam punkt na fibrynogenie.
Co to oznacza dla ryzyka zawału i udaru
Składając wszystkie dowody razem, praca ujawnia bezpośredni łańcuch zdarzeń od pochodnych jelitowych lub leków cząsteczek N-tlenkowych do zmian w strukturze skrzepu krwi. Poprzez wiązanie się z konkretnym miejscem na fibrynogenie, TMAO i jego chemiczne kuzyny zmuszają białko do konformacji sprzyjającej szybkiemu formowaniu włókien i powstawaniu skrzepów trudniejszych do rozłożenia. Dla laika oznacza to, że pewne produkty metabolizmu mikrobiologicznego i metabolity leków mogą niepostrzeżenie wzmacniać „rusztowanie” skrzepów, co pomaga wyjaśnić, dlaczego podwyższone stężenia TMAO korelują z większym ryzykiem zdarzeń zatorowo-naczyniowych. Miejsce beta1 na fibrynogenie wyłania się jako obiecujący cel terapeutyczny, mający na celu zmiękczenie skrzepów i zmniejszenie powikłań miażdżycy bez całkowitego blokowania krzepnięcia.
Cytowanie: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Słowa kluczowe: mikrobiom jelitowy, zakrzepy krwi, TMAO, miażdżyca, fibrynogen