Clear Sky Science · sv
Tarmsubstansen TMAO och dess strukturella analoger binder till fibrinogen och ökar därigenom blodproppsbildning: en förklaring till risk för ateroskleros
Från tarmkemikalier till blodproppar
Det som händer i din tarm stannar inte i tarmen. Denna studie undersöker hur en liten molekyl som tillverkas av tarmbakterier, kallad TMAO, kan förändra hur blodproppar bildas och bryts ned. Eftersom onormala proppar ligger bakom hjärtinfarkter och stroke, bidrar förståelsen av denna dolda länk mellan kost, tarmmikrober, vanliga läkemedel och koagulation till att förklara varför vissa personer har högre kardiovaskulär risk — och var nya behandlingar kan ingripa.
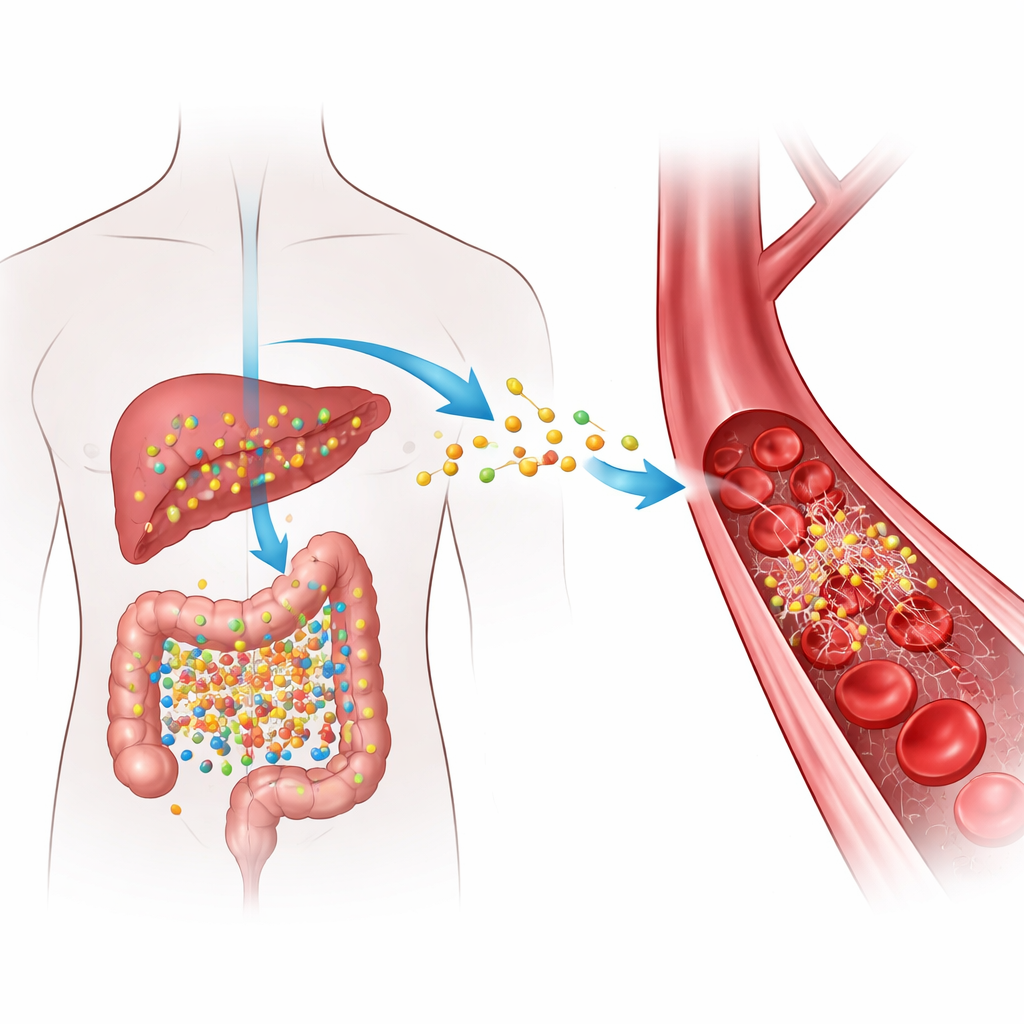
Hur vardagsmat blir en risksignal
När vi äter livsmedel rika på vissa näringsämnen som finns i rött kött, ägg och fettrika mejeriprodukter, omvandlar tarmbakterier dessa komponenter till en mellanprodukt som levern sedan gör om till TMAO. Höga nivåer av TMAO i blodet har upprepade gånger kopplats till tilltäppta artärer och en ökad risk för farliga proppar, men det exakta ”hur” har varit oklart. Författarna fokuserade på fibrinogen, ett lösligt protein som cirkulerar i blodet och som, när det klipps av enzymet trombin, omvandlas till fibrin — det trådiga materialet som hjälper till att täppa igen skador genom att bilda proppar. De frågade om TMAO fysiskt interagerar med fibrinogen på ett sätt som kan få proppar att bildas snabbare eller bli svårare att lösa upp.
Gör proppar snabbare och svårare att rensa bort
Genom att följa hur lösningar av fibrinogen övergår till fibrin över tid visade forskarna att tillsats av TMAO snabbar upp sammansättningen av tidiga byggstenar i propparna. Ljus-spridnings- och fluorescerande färgexperiment visade att utan TMAO hade bara omkring en tredjedel av proteinet gått med i fibriller efter en given period. Med stigande TMAO-nivåer steg denna andel mot fullständig omvandling, och mikroskopbilder visade ett mycket tätare nätverk av fibrer. När de undersökte hur dessa proppar bröts ner fann de ytterligare en oroande egenskap: proppar bildade i närvaro av TMAO var starkt motståndskraftiga mot nedbrytning av ett proteinnedbrytande enzym, och förblev kompakta och till stora delar intakta medan normala proppar nästan helt degraderades.
En precis dockningsplats på koagulationsproteinet
För att se om denna effekt kom från direkt bindning mätte teamet värmeförändringar när TMAO blandades med fibrinogen och fann tydliga bevis för att de två interagerar med måttlig styrka vid koncentrationer liknande dem som ses hos personer med hjärtsjukdom. Spektroskopiska metoder indikerade att fibrinogens form blev något lösare, vilket exponerade fler klibbiga ytor som gynnar protein–protein-kontakt. Datorbaserad modellering och långa simuleringar kartlade var TMAO sitter på fibrinogen och framhöll en specifik region känd som beta1-kalciumbindingsstället. När denna plats var upptagen av naturliga kalciumjoner kunde TMAO inte längre utöva sin verkan, och proppsbildningen såg likadan ut oavsett om TMAO fanns närvarande eller inte. Detta pekar på beta1-platsen som en kontrollpunkt som reglerar hur lätt fibrinogenmolekyler låser ihop sig.
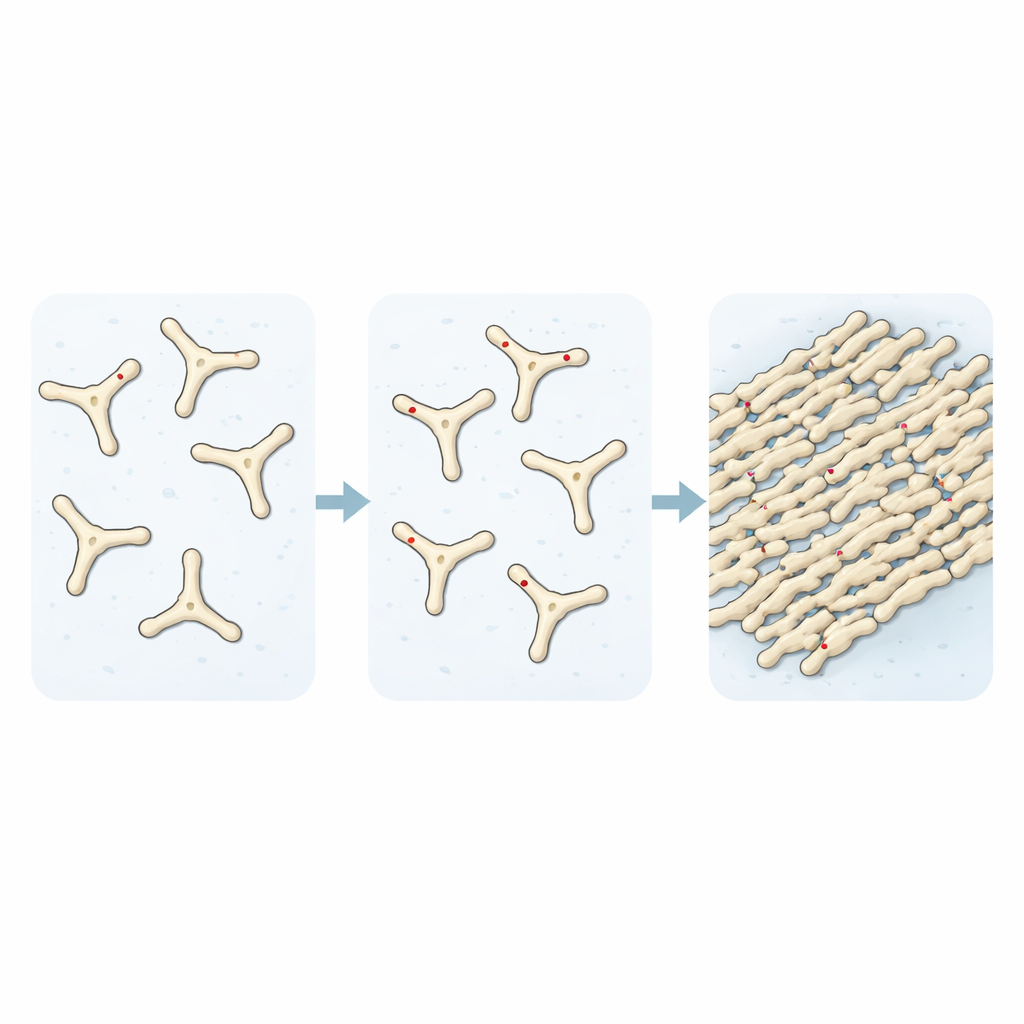
Läkemedelsmetaboliter blir en del av berättelsen
Författarna frågade sedan om andra små molekyler som liknar TMAO kunde bete sig på ett liknande sätt. Genom att använda kemiska databaser och dockningsprogram skannade de uppsättningar av besläktade föreningar och valde ut två som är N-oxid-nedbrytningsprodukter av allmänt använda antidepressiva och nikotinrelaterade läkemedel. I provrörsexperiment ökade dessa metaboliter också hastigheten och omfattningen av fibrinsammansättningen och producerade tjockare, tätare fibrinnätverk, mycket likt TMAO. Denna upptäckt väcker möjligheten att vissa läkemedel, när de väl bearbetats av kroppen, subtilt kan förskjuta balansen mot mer robust proppsbildning genom att verka på samma hetpunkt i fibrinogen.
Vad detta betyder för hjärt- och strokerisk
Sammantaget visar arbetet en direkt kedja av händelser från tarm- eller läkemedelsderiveda N-oxidmolekyler till förändringar i blodproppars struktur. Genom att binda till en specifik plats på fibrinogen skjuter TMAO och dess kemiska släktingar proteinet i en konformation som uppmuntrar snabb fiberbildning och ger proppar som är svårare att bryta ned. För en lekmann innebär detta att vissa mikrobiala biprodukter och läkemedelsmetaboliter tyst kan förhärda propparnas ”stomme”, vilket hjälper till att förklara varför förhöjda TMAO-nivåer följer med en ökad sannolikhet för artärblockerande händelser. Beta1-platsen på fibrinogen framstår som ett lovande mål för behandlingar som syftar till att göra proppar mjukare och minska komplikationer från ateroskleros utan att helt blockera koagulationen.
Citering: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Nyckelord: tarmmikrobiom, blodproppar, TMAO, ateroskleros, fibrinogen