Clear Sky Science · de
Darmmetabolit TMAO und seine strukturellen Analoga binden an Fibrinogen und verstärken so die Blutgerinnung: eine Erklärung für das Atheroskleroserisiko
Von Darmchemikalien zu Blutgerinnseln
Was im Darm geschieht, bleibt nicht im Darm. Diese Studie untersucht, wie ein winziges Molekül, das von Darmbakterien gebildet wird und TMAO genannt wird, die Art und Weise verändern kann, wie sich Blutgerinnsel bilden und wieder auflösen. Da fehlerhafte Gerinnsel Herzinfarkte und Schlaganfälle zugrunde liegen, trägt das Verständnis dieser versteckten Verbindung zwischen Ernährung, Darmmikroben, gängigen Medikamenten und der Gerinnung dazu bei, zu erklären, warum manche Menschen ein höheres kardiovaskuläres Risiko haben — und wo neue Behandlungsansätze ansetzen könnten.
Wie alltägliche Nahrung zu einem Risikosignal wird
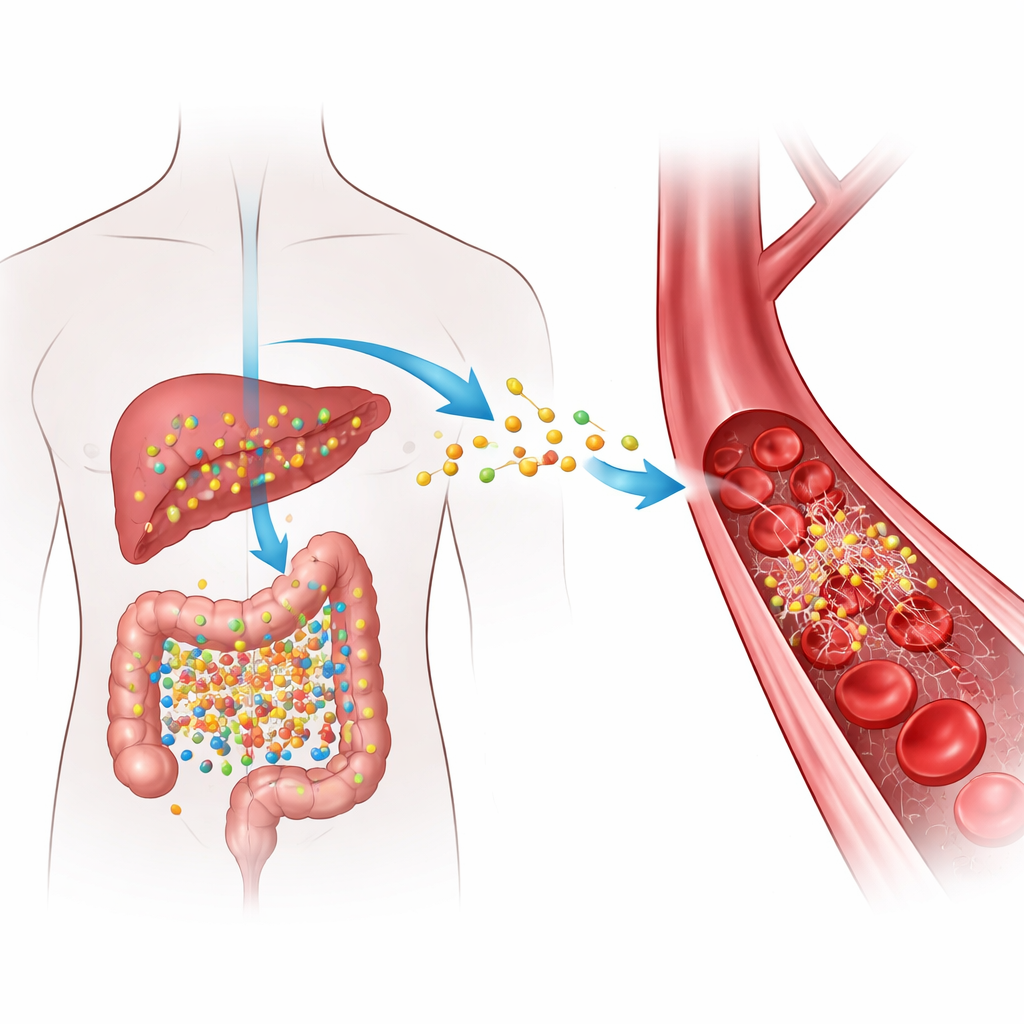
Wenn wir Nahrungsmittel zu uns nehmen, die reich an bestimmten Nährstoffen sind, wie sie in rotem Fleisch, Eiern und fettreichen Milchprodukten vorkommen, wandeln Darmbakterien diese Komponenten in eine Zwischenverbindung um, die die Leber dann in TMAO umsetzt. Hohe TMAO-Werte im Blut wurden wiederholt mit verengten Arterien und einer höheren Wahrscheinlichkeit gefährlicher Gerinnsel in Verbindung gebracht, doch das genaue „Wie“ war unklar. Die Autorinnen und Autoren konzentrierten sich auf Fibrinogen, ein lösliches Protein im Blut, das durch das Enzym Thrombin in Fibrin geschnitten wird — das faserige Material, das Verletzungen abdichtet, indem es Gerinnsel bildet. Sie fragten, ob TMAO physisch mit Fibrinogen interagiert und dadurch die Gerinnselbildung beschleunigen oder die Auflösung erschweren könnte.
Gerinnsel bilden sich schneller und lassen sich schlechter entfernen
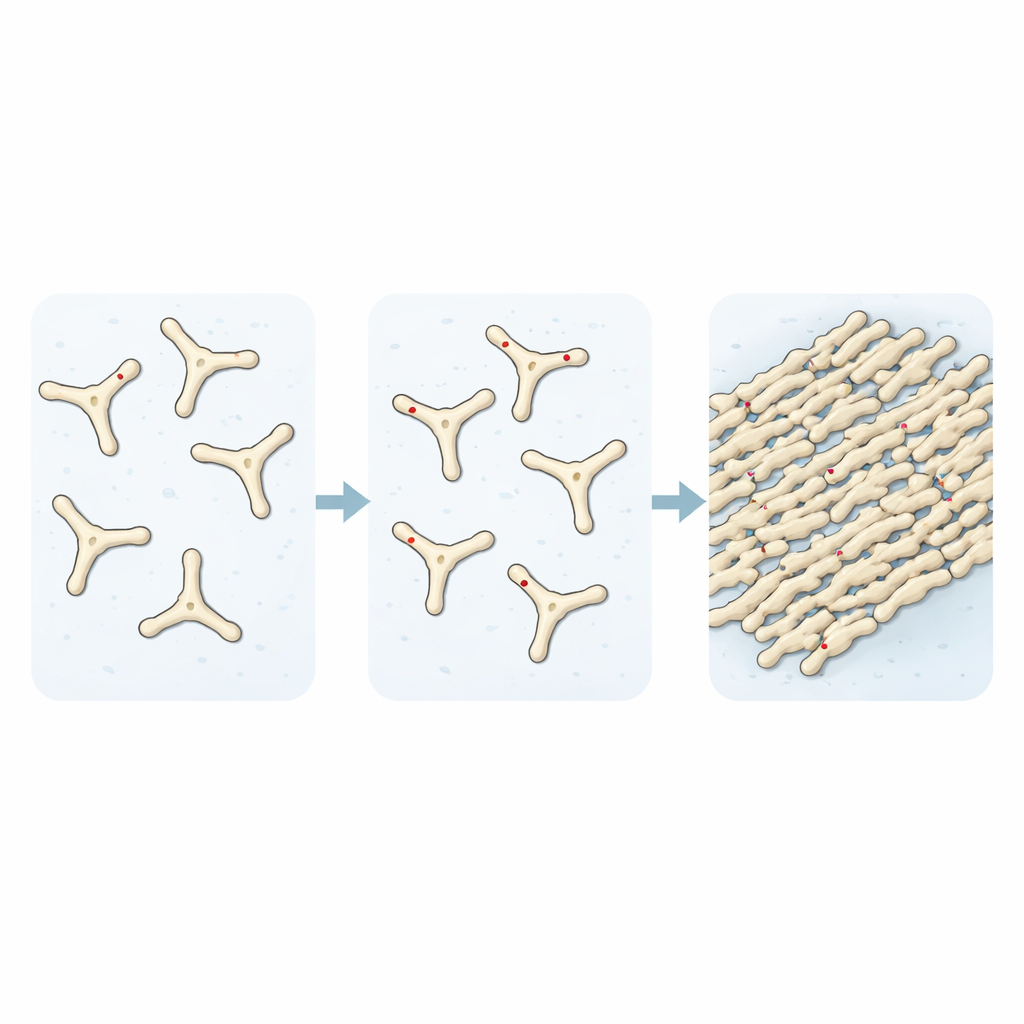
Indem sie verfolgten, wie sich Lösungen von Fibrinogen im Laufe der Zeit zu Fibrin umwandeln, zeigten die Forschenden, dass das Hinzufügen von TMAO die Assemblierung der frühen Bausteine von Gerinnseln beschleunigt. Lichtstreuungs- und Fluoreszenzfarbstoff-Experimente zeigten, dass ohne TMAO nach einer bestimmten Zeit nur etwa ein Drittel des Proteins in Fibrillen eingebaut war. Mit steigenden TMAO-Werten stieg dieser Anteil gegen eine vollständige Umwandlung, und Mikroskopaufnahmen zeigten ein deutlich dichteres Netz von Fasern. Bei der Untersuchung, wie sich diese Gerinnsel abbauen, fanden sie ein weiteres beunruhigendes Merkmal: In Gegenwart von TMAO gebildete Gerinnsel waren stark resistent gegenüber dem Abbau durch proteolytische Enzyme, blieben kompakt und weitgehend intakt, während normale Gerinnsel fast vollständig zerstört wurden.
Eine präzise Andockstelle am Gerinnungsprotein
Um zu prüfen, ob dieser Effekt durch direkte Bindung verursacht wird, maßen die Forscherinnen und Forscher Wärmeänderungen, wenn TMAO mit Fibrinogen vermischt wurde, und fanden klare Hinweise darauf, dass die beiden mit moderater Stärke bei Konzentrationen interagieren, wie sie bei Menschen mit Herzerkrankungen beobachtet werden. Spektroskopische Methoden zeigten, dass sich die Gestalt von Fibrinogen leicht lockerte und mehr klebrige Stellen freilegte, die Protein–Protein-Kontakte begünstigen. Computermodelle und lange Simulationen kartierten, wo TMAO auf Fibrinogen sitzt, und hoben eine bestimmte Region hervor, die als Beta1-Calciumbindungsstelle bekannt ist. Wenn diese Stelle von natürlichen Calciumionen besetzt war, konnte TMAO seine Wirkung nicht mehr entfalten, und die Gerinnselbildung sah gleich aus, unabhängig davon, ob TMAO vorhanden war oder nicht. Das deutet darauf hin, dass die Beta1-Stelle ein Steuerpunkt ist, der beeinflusst, wie leicht sich Fibrinogenmoleküle miteinander verbinden.
Auch Arzneimittelmetaboliten spielen eine Rolle
Die Autorinnen und Autoren fragten dann, ob andere kleine Moleküle, die TMAO ähneln, sich ähnlich verhalten könnten. Mit Hilfe chemischer Datenbanken und Docking-Software screeneten sie eine Reihe verwandter Verbindungen und wählten zwei aus, die N‑oxid-Abbauprodukte weitverbreiteter Antidepressiva und nikotinbezogener Wirkstoffe sind. In Reagenzglasversuchen beschleunigten diese Metaboliten ebenfalls die Geschwindigkeit und das Ausmaß der Fibrinassemblierung und erzeugten dickere, dichtere Fibrinnetzwerke, ganz ähnlich wie TMAO. Dieser Befund legt die Möglichkeit nahe, dass einige Medikamente, nachdem sie im Körper verarbeitet wurden, das Gleichgewicht leicht zugunsten robusterer Gerinnselbildung verschieben könnten, indem sie an derselben Hotspot‑Stelle im Fibrinogen wirken.
Was das für Herz‑ und Schlaganfallrisiko bedeutet
Setzt man alle Befunde zusammen, zeigt die Arbeit eine direkte Kette von Ereignissen von darm- oder medikamentenabgeleiteten N‑oxid‑Molekülen bis hin zu Veränderungen der Struktur von Blutgerinnseln. Durch die Bindung an eine spezifische Stelle auf Fibrinogen drängen TMAO und seine chemischen Verwandten das Protein in eine Konformation, die schnelle Faserbildung begünstigt und Gerinnsel erzeugt, die schwerer abzubauen sind. Für Laien bedeutet das: Bestimmte mikrobielle Abbauprodukte und Arzneimittelmetaboliten können still und heimlich das „Gerüst“ von Gerinnseln verhärten und helfen so, zu erklären, warum erhöhte TMAO‑Werte mit einem höheren Risiko für arterienverengende Ereignisse einhergehen. Die Beta1‑Stelle auf Fibrinogen erweist sich als vielversprechendes Ziel für Therapien, die Gerinnsel aufweichen und Komplikationen durch Atherosklerose verringern sollen, ohne die Blutgerinnung vollständig zu blockieren.
Zitation: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Schlüsselwörter: Darmmikrobiom, Blutgerinnsel, TMAO, Atherosklerose, Fibrinogen