Clear Sky Science · it
Il metabolita intestinale TMAO e i suoi analoghi strutturali si legano al fibrinogeno aumentando così la formazione del coagulo: una giustificazione per il rischio di aterosclerosi
Dai chimici intestinali ai coaguli di sangue
Quello che avviene nell’intestino non resta confinato nell’intestino. Questo studio esplora come una piccola molecola prodotta dai batteri intestinali, chiamata TMAO, possa modificare il modo in cui i coaguli di sangue si formano e si degradano. Poiché i coaguli anomali sono alla base di infarti e ictus, comprendere questo collegamento nascosto tra dieta, microbiota intestinale, farmaci comuni e coagulazione aiuta a spiegare perché alcune persone presentano un rischio cardiovascolare maggiore — e dove potrebbero intervenire nuove terapie.
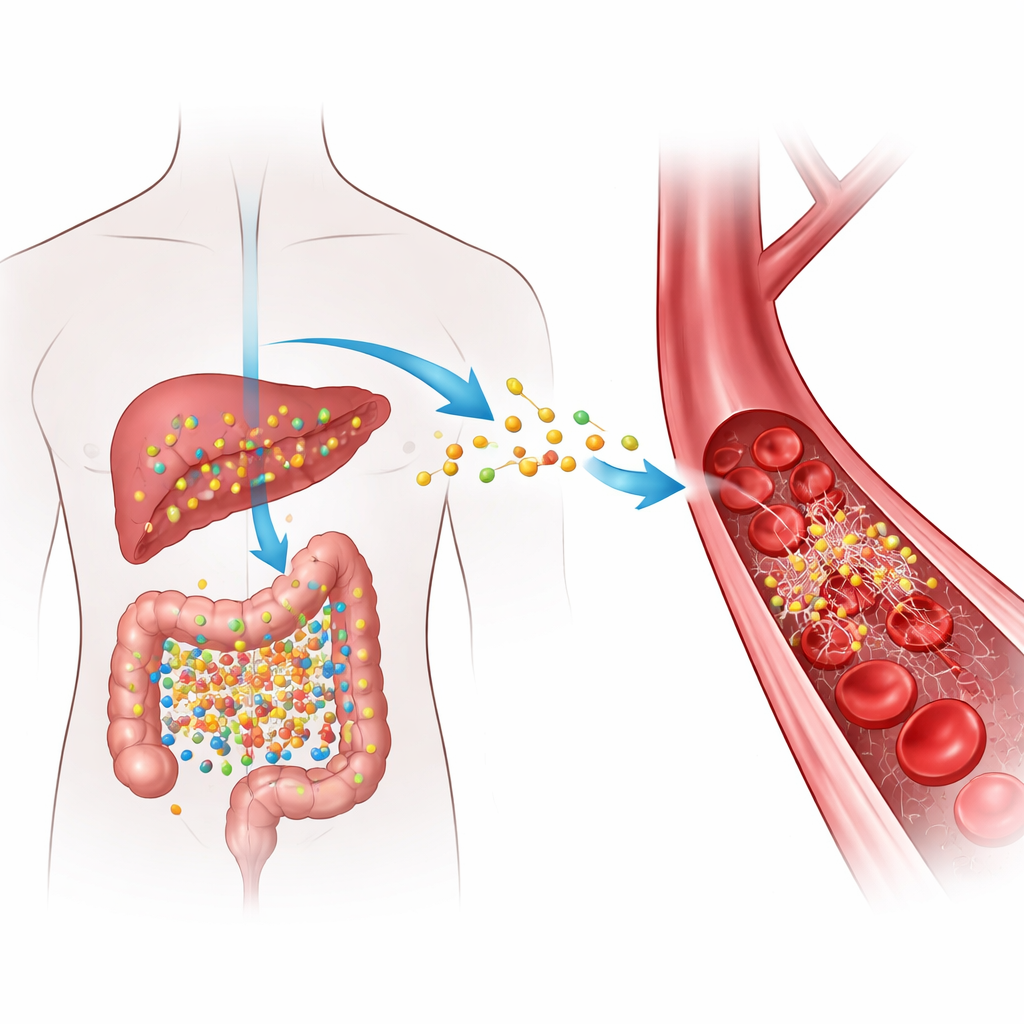
Come il cibo quotidiano diventa un segnale di rischio
Quando consumiamo alimenti ricchi di determinati nutrienti presenti nella carne rossa, nelle uova e nei latticini ad alto contenuto di grassi, i batteri intestinali trasformano questi componenti in un composto intermedio che il fegato converte poi in TMAO. Alti livelli di TMAO nel sangue sono stati ripetutamente associati ad arterie occluse e a una maggiore probabilità di coaguli pericolosi, ma il “come” preciso è rimasto poco chiaro. Gli autori si sono concentrati sul fibrinogeno, una proteina solubile che circola nel sangue e che, quando viene tagliata dall’enzima trombina, si trasforma in fibrina — il materiale filamentoso che aiuta a sigillare le lesioni formando i coaguli. Hanno chiesto se il TMAO interagisca fisicamente con il fibrinogeno in modo tale da rendere i coaguli più rapidi a formarsi o più difficili da dissolvere.
Formare coaguli più velocemente e più difficili da eliminare
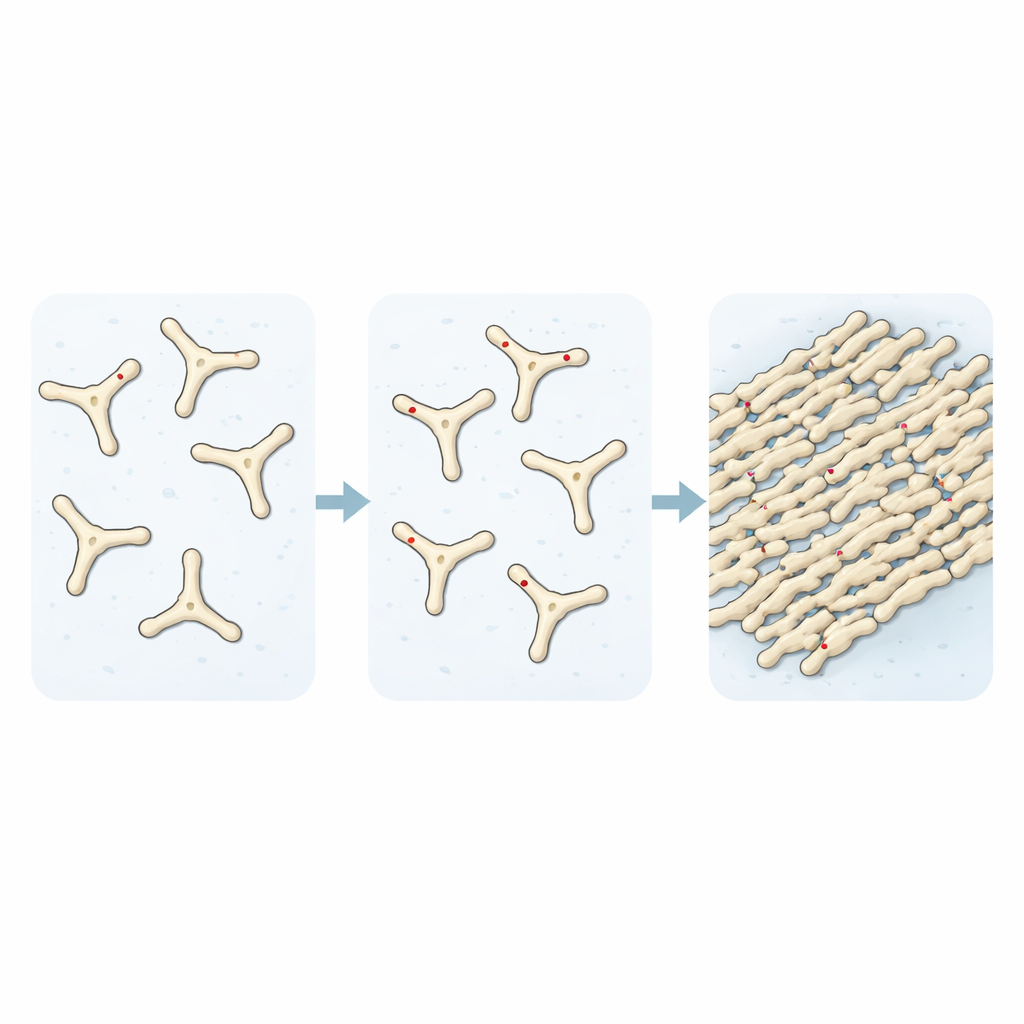
Seguendo la trasformazione delle soluzioni di fibrinogeno in fibrina nel tempo, i ricercatori hanno dimostrato che l’aggiunta di TMAO accelera l’assemblaggio dei primi mattoni dei coaguli. Esperimenti di diffusione della luce e con coloranti fluorescenti hanno rivelato che, senza TMAO, solo circa un terzo della proteina si era unito in fibrille dopo un dato intervallo. Con l’aumentare dei livelli di TMAO, quella frazione si avvicinava alla conversione completa, e le immagini al microscopio mostravano una rete di fibre molto più densa. Quando hanno esaminato come questi coaguli si degradavano, hanno riscontrato un altro elemento preoccupante: i coaguli formati in presenza di TMAO erano altamente resistenti alla digestione da parte di un enzima proteolitico, rimanendo compatti e in gran parte intatti mentre i coaguli normali venivano quasi completamente degradati.
Un sito di aggancio preciso sulla proteina della coagulazione
Per capire se questo effetto derivasse da un legame diretto, il gruppo ha misurato le variazioni di calore mentre il TMAO veniva mescolato con il fibrinogeno e ha trovato prove chiare che i due interagiscono con forza moderata a concentrazioni simili a quelle osservate in persone con malattie cardiache. Metodi spettroscopici hanno indicato che la conformazione del fibrinogeno si allentava leggermente, esponendo più superfici adesive che favoriscono il contatto proteina–proteina. Modellizzazione al computer e lunghe simulazioni hanno mappato dove si posiziona il TMAO sul fibrinogeno e hanno evidenziato una regione specifica nota come sito beta1 legante il calcio. Quando questo sito era occupato dagli ioni calcio naturali, il TMAO non poteva più esercitare il suo effetto, e la formazione del coagulo appariva la stessa indipendentemente dalla presenza di TMAO. Ciò indica il sito beta1 come un punto di controllo che regola quanto facilmente le molecole di fibrinogeno si incastrano tra loro.
I metaboliti dei farmaci entrano in gioco
Gli autori si sono poi chiesti se altre piccole molecole simili al TMAO potessero comportarsi allo stesso modo. Utilizzando banche dati chimiche e software di docking, hanno selezionato un insieme di composti correlati e individuato due prodotti di degradazione N-ossido di farmaci antidepressivi e di sostanze correlate alla nicotina ampiamente usati. In esperimenti in provetta, questi metaboliti hanno anch’essi aumentato la velocità e l’estensione dell’assemblaggio della fibrina, generando reti fibriniche più spesse e dense, molto simili a quelle indotte dal TMAO. Questo risultato solleva la possibilità che alcuni farmaci, una volta metabolizzati dall’organismo, possano inclinare sottilmente l’equilibrio verso una formazione di coaguli più robusta agendo sullo stesso punto critico del fibrinogeno.
Cosa significa questo per il rischio di infarto e ictus
Mettendo insieme tutte le evidenze, il lavoro rivela una catena diretta di eventi che va da molecole N-ossido di origine intestinale o farmacologica a cambiamenti nella struttura del coagulo. Legandosi a un sito specifico sul fibrinogeno, il TMAO e i suoi cugini chimici spingono la proteina verso una conformazione che favorisce la rapida formazione di fibre e produce coaguli più difficili da smontare. Per il lettore non specialista, ciò significa che alcuni sottoprodotti microbici e metaboliti farmacologici possono indurire silenziosamente l’“impalcatura” dei coaguli, contribuendo a spiegare perché livelli elevati di TMAO si associano a una maggiore probabilità di eventi occlusivi arteriosi. Il sito beta1 sul fibrinogeno emerge come un promettente bersaglio per terapie volte ad ammorbidire i coaguli e ridurre le complicanze dell’aterosclerosi senza bloccare del tutto la coagulazione.
Citazione: Singh, K., Kumari, A., Bakhshi, R. et al. Gut metabolite TMAO and its structural analogs bind to fibrinogen thereby enhancing clot formation: a rationale for atherosclerosis risk. Sci Rep 16, 13676 (2026). https://doi.org/10.1038/s41598-026-43910-0
Parole chiave: microbioma intestinale, coaguli di sangue, TMAO, aterosclerosi, fibrinogeno